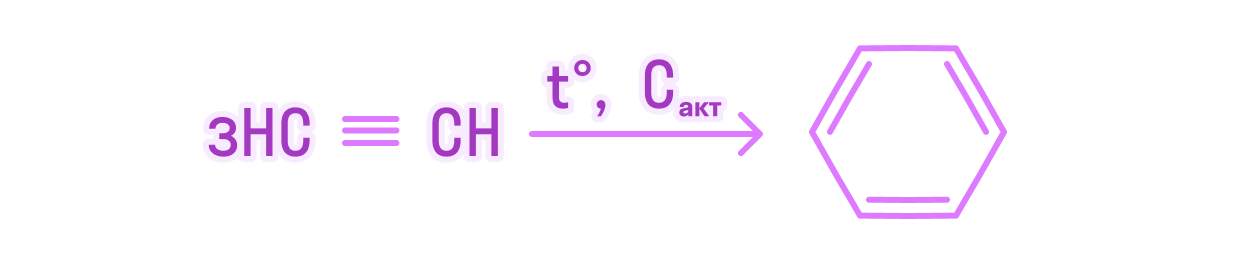Муниципальное общеобразовательное учреждение
«Общеобразовательная средняя (полная) школа № 14»
Проект
«Формирование учебных компетенций учащихся старшей ступени общеобразовательной школы при подготовке к ЕГЭ по химии через электронное пособие».
Автор проекта:
учитель химии
Т.Е. Суранова
г. Нягань
2014г.
ОГЛАВЛЕНИЕ
Краткая аннотация проекта
Обоснование необходимости проекта………………………………………3
Цели и задачи проекта…………………………………………………….….5
Основное содержание проекта……………………………………………….6
Ресурсы………………………………………………………………………..16
Партнеры………………………………………………………………………17
Целевая аудитория…………………………………………………………….17
План реализации проекта……………………………………………………..18
Ожидаемые результаты и социальный эффект……………………………..19
Перспективы дальнейшего развития проекта………………………….……24
Литература………………………………………………………………….…24
Приложение 1. Электронное пособие для учащихся 11 классов для подготовки к ЕГЭ.
ОБОСНОВАНИЕ НЕОБХОДИМОСТИ ПРОЕКТА
Президент Российской Федерации Д.А. Медведев в национальной образовательной инициативе «Наша новая школа» сформулировал следующие требования к современной школе: «у выпускника современной школы должны быть сформированы готовность и способность творчески мыслить, находить нестандартные решения, проявлять инициативу; готовность к продолжению профессионального образования, т.е. выпускник должен быть конкурентоспособным». В соответствии с новыми Стандартами современной школы содержание основных и дополнительных образовательных программ, учебной и внеучебной деятельности направлено на достижение стратегической цели образования — раскрытие и развитие потенциала каждого ученика в соответствии с его возможностями и способностями.
Анализ документов Министерства образования и науки Российской Федерации, Правительства ХМАО – Югры по модернизации образования до 2020 года, научно – педагогической, психолого-педагогической литературы по вопросам модернизации и инновационного развития современной школы, повышения профессиональных педагогических компетентностей педагогов, методики обучения и организации образовательного процесса позволил выявить противоречия:
— противоречие между необходимостью повышения квалификации педагогов общего образования по применению новых, в том числе информационных, образовательных технологий, по внедрению прогрессивных методов организации образовательного процесса, а также учебно-методических материалов, в части применения современных методик преподавания, теории обучения и практик по естественнонаучному циклу и недостаточностью учебной, учебно-методической литературы;
— противоречие между необходимостью создания условий для эффективной реализации и освоения обучающимися основной образовательной программы среднего (полного) образования, в том числе для обеспечения условий индивидуального развития каждого обучающегося и недостаточностью практических пособий, методических разработок для педагогов по формированию мотивированной компетентной личности учащегося общеобразовательной школы;
— противоречие между необходимостью методических разработок вариативного содержания и недостаточностью разработок методических указаний и методических рекомендаций для преподавателей естественнонаучного цикла.
Анализ показал, что, к сожалению, среди имеющихся на сегодняшний день методических пособий педагогу трудно найти такие, которые бы позволяли в полной мере за короткий период с максимальной эффективностью повторить теоретический материал по всем разделам школьного курса химии, закрепить знания, умения, навыки и провести контроль и оценку результатов освоения программ обучения.
Опираясь на научные труды и педагогический опыт кандидатов химических наук, доцентов химического факультета МГУ, имеющих большой опыт подготовки школьников к сдаче выпускных вступительных экзаменов по химии, Дроздова А.А., Еремина Е.А., автора рабочей программы по химии для 8 – 11 классов О.С. Габриеляна, с 2014 года по 2015 год мною было разработано электронное пособие по химии для подготовки учащихся к ЕГЭ.
В проекте «Формирование учебных компетенций учащихся старшей ступени общеобразовательной школы при подготовке к ЕГЭ через электронное пособие» представлена педагогическая методика по подготовке выпускника 11 класса к государственной итоговой аттестации в форме Единого государственного экзамена по предмету химия.
ЦЕЛИ И ЗАДАЧИ
Цель проекта: разработка, апробация, внедрение электронного пособия по химии для учащихся XI классов.
Задачи:
- Провести анализ типичных ошибок по результатам Единого государственного экзамена по предмету химия.
- Выявить и обосновать комплекс педагогических условий, обеспечивающих качество результатов Единого государственного экзамена.
- Разработать электронное пособие по химии для учащихся XI классов как средства по формированию учебных компетенций.
- Провести апробацию электронного пособия в муниципальном общеобразовательном учреждении «Средняя общеобразовательная школа № 14» и распространить педагогический опыт в общеобразовательных учреждениях города.
ОСНОВНОЕ СОДЕРЖАНИЕ ПРОЕКТА
Методологической основой проектирования являются компетентностный подход, научный и системно–деятельностный подход, модульный подход, индивидуальный и дифференцированный подходы, педагогические технологии. Содержание проекта построено на практическом опыте работы учителя химии Т.Е. Сурановой по результатам апробации электронного пособия по химии для учащихся XI классов в муниципальном общеобразовательном учреждении «Средняя общеобразовательная школа № 14».
Программа электронного пособия разработана на основе требований Государственного стандарта в образовательной области «химия» и включает разделы: пояснительная записка, содержание электронного пособия, список используемой литературы, приложение.
Пояснительная записка включает:
-обоснование актуальности создания электронного пособия (электронное пособие разработано в связи с необходимостью обеспечения учащихся возможностью глубокого системного повторения, устранения пробелов по основным разделам содержания школьного курса химии и профильной подготовки по естественнонаучному направлению);
-цель пособия: систематизация и закрепление химических знаний, формирование систематизированных представлений о химических процессах, явлениях, закономерностях, овладение понятийным аппаратом курса химии;
-задачи пособия: сформировать умения обосновывать место и роль химических знаний в практической деятельности человека, в развитии современных технологий; находить и анализировать информацию о веществах разных классов и их свойствах, сформировать умения осуществлять разнообразные виды самостоятельной деятельности; развивать познавательные интересы, интеллектуальные и творческие способности в процессе изучения химии в ходе работы с различными источниками информации; развивать самоконтроль и самооценку знаний с помощью различных форм тестирования; сформировать умения использовать приобретенные знания и умения в практической деятельности;
-методы и формы (методы обучения: словесный (лекция, объяснение алгоритмов решения заданий, беседа, дискуссия); наглядный (демонстрация презентаций уроков, видеофильмов, фотографий, таблиц, схем в цифровом формате); частично-поисковый, поисковый, практический (решение уравнений реакций, генетических цепочек превращений, задач, составление схем строения атомов, и т.д.); формы обучения: самостоятельная работа;
— структура пособия: представлена тестами по основным разделам курса общей химии, что соответствует кодификатору элементов содержания контрольно-измерительных материалов ЕГЭ. Тесты состоят из двух частей, включающих различные типы заданий. Часть 1 включает задания с выбором ответа. Часть 2 содержит задания с выбором нескольких ответов: задания с выбором трех верных ответов из пяти, задачи на вычисление массовой доли растворенного вещества и массы, объема вещества по уравнению реакции. В ходе решения тесов учащиеся имеют возможность сами проконтролировать знания по количеству полученных баллов;
-компетенции на базовом уровне (владение химической терминологией и символикой; знание основных методов изучения веществ; понимание основных законов, правил, закономерностей химических процессов, умение называть вещества, составлять их формулы, уравнения реакций, определять окислители и восстановители, проводить вычисления по химическим формулам и уравнениям, использовать химические знания в практической деятельности);
-на повышенном уровне (овладение учащимися более сложными и разнообразными видами учебной деятельности: — знание сущности химических процессов, явлений, общехимических закономерностей; умения определять, сравнивать, классифицировать, умения устанавливать взаимосвязи между классами веществ; выявлять общие и отличительные признаки; составлять схемы окислительно-восстановительных процессов, решать генетические цепочки превращений веществ, знать применение веществ и обращение с веществами);
-на высоком уровне (формирование умений самостоятельно оперировать химическими понятиями, обосновывать и объяснять химические процессы и явления, грамотно формулировать свой ответ; применять знания при решении задач повышенного уровня; устанавливать причинно-следственные связи; анализировать, систематизировать и интегрировать знания; обобщать и формулировать выводы; оценивать и прогнозировать биологические процессы, применять теоретические знания на практике).
Тематический план пособия состоит из блоков, соответствующих кодификатору элементов содержания контрольно-измерительных материалов ЕГЭ: «Химический элемент», «Вещество», «Химическая реакция», «Познание и применение веществ и химических реакций».
Содержание электронного пособия представлено тестами по определенным темам общей химии: тест №1 «Строение атома. Периодический закон и периодическая система Д.И. Менделеева»; тест №2 «Химическая связь»; тест №3 «Типы химических реакций и закономерности их протекания»; тест №4 «Классы неорганических веществ», тест №5 «Свойства неорганических веществ», тест №6 «Электролитическая диссоциация. Гидролиз»; тест №7 «Генетическая связь между классами неорганических веществ», тест №8 «Свойства веществ и их применение», тест №9 «Получение веществ», работа №10 «Решение задач на вычисление массовой доли растворенного вещества».
Формы контроля представлены тематическим контролем (рейтинговая оценка результатов выполнения тематических тестов) и итоговым контролем (суммарная оценка результатов выполнения тестов). Оценка результатов проводится по рейтинговой шкале с учетом объема, качества и уровня сложности выполненных работ.
Список используемой литературы включает: дополнительную и научно-популярную литературу для учителя; литературу для учащихся; мультимедийные пособия; адреса сайтов в Интернете.
Приложение 1. Тесты, состоящие из двух частей, включающих различные типы заданий. Часть 1 включает задания с выбором ответа. Часть 2 содержит задания с кратким ответом: задания с выбором трех верных ответов из пяти, расчетные задачи.
СИСТЕМА УПРАВЛЕНИЯ И МЕХАНИЗМ РЕАЛИЗАЦИИ ПРОЕКТА
Обучение учащихся с применением электронного пособия по химии для учащихся XI классов создает условия для формирования активной учебно — познавательной деятельности учащихся, повышения положительной мотивации учения, развития познавательного интереса; способствует эффективному усвоению и повторению курса химии общеобразовательной школы, формированию профессиональных намерений и способностей учащихся старшей ступени общеобразовательной школы; повышает уровень подготовки выпускника 3 ступени обучения к итоговой (государственной) аттестации в форме Единого государственного экзамена по предмету химия.
Рис.1. Структура электронного пособия.
РЕСУРСЫ
Материально — технические ресурсы: кабинет химии; технические средства обучения: интерактивная доска «Hitachi FX-DUO-77», компьютер сборки ПК Formoza D4400+, монитор Samsung 740, мультимедиа-проектор NEC-NP 200.
Кадровое обеспечение: учитель химии.
Информационно – методическое обеспечение: учебно-методические пособия: О.С. Габриелян. «Химия, 11 класс»: учебник для общеобразовательных учреждений. М.: Дрофа, 2003г.; О.С. Габриелян, Ф.Н. Маскаев, С.Ю. Пономарев, В.И. Теренин «Химия, 10 класс»: учебник для общеобразовательных учреждений. М.: Дрофа, 2005г.; А.А. Дроздов, Е.А. Еремина «Репетитор: эффективная методика для подготовки к ЕГЭ». М.: «Экзамен», 2005г.; О.С. Габриелян, И.Г. Остроумова, А.Г. Введенская «Общая химия в тестах, задачах, упражнениях»-учебное пособие для общеобразовательных учреждений. М.: Дрофа, 2003г.
Медиа ресурсы: http://metodik.bryanskedu.net/?id=777 — Экзаменационные материалы для подготовки к единому государственному экзамену. Химия; http://down.ctege.org/ege/ — сайт вариантов ЕГЭ; http://www.fipi.ru/view/sections/91/docs/ — демоверсии на сайте ФИПИ
ПАРТНЕРЫ
Педагоги, учащиеся базовых и профильных классов муниципального общеобразовательного учреждения «Общеобразовательная средняя (полная) школа № 14»,
ЦЕЛЕВАЯ АУДИТОРИЯ
В реализации педагогического опыта участвовали учащиеся базовых и профильных классов муниципального общеобразовательного учреждения «Средняя общеобразовательная школа № 14».
Инновационные разработки: Тесты по основным разделам неорганической химии, являющиеся составной частью электронного пособия.
ПЛАН РЕАЛИЗАЦИИ ПРОЕКТА
|
№ п/п |
Мероприятия |
Сроки |
Результат |
|
I |
I этап — Организационно-исследовательский (сентябрь 2013г.- январь 2014г.) |
||
|
1 |
Изучение научной литературы по педагогике, методологии, психологии, документов Министерства образования и науки РФ, Департамента образования и науки ХМАО-Югры. |
Сентябрь 2013г. |
Определение методологической базы проектирования педагогической разработки. |
|
2 |
Накопление тестового материала для электронного пособия |
октябрь 2013г. –декабрь 2013г. |
Разработка электронного пособия для подготовки учащихся 11 классов к ЕГЭ по химии: неорганическая химия |
|
3 |
Разработка электронного пособия для подготовки учащихся 11 классов к ЕГЭ |
декабрь 2013г. — январь 2014г. |
|
|
II |
II этап — Практический этап (февраль 2014г. сентябрь 2017г.) |
||
|
1 |
Освоение и внедрение ИКТ-технологий |
февраль 2014г. – май 2014г. |
Участие в методических мероприятиях по организации деятельности в рамках реализации проекта. |
|
2 |
Апробация и внедрение электронного пособия в учебно-воспитательный процесс, как инструментария по формированию активной учебно-познавательной деятельности учащихся. |
май 2014г. – май 2017г. |
Внедрение инструментария по формированию активной учебно-познавательной деятельности учащихся старшей ступени обучения общеобразовательной школы. |
|
III |
III этап – аналитико — рефлексивный (май 2017г.- сентябрь 2017г.) |
||
|
1 |
Обобщение педагогического опыта по реализации проекта |
май 2017г. — сентябрь 2017г. |
Создание электронного пособия для учащихся 11 классов. Создание условий для подготовки выпускника старшей ступени обучения к итоговой (государственной) аттестации в форме Единого государственного экзамена по предмету химия. |
|
2 |
Распространение педагогического опыта |
Отзыв учителей городского методического объединения химии об эффективности использования электронного пособия. Публикации |
ОЖИДАЕМЫЕ РЕЗУЛЬТАТЫ И СОЦИАЛЬНЫЙ ЭФФЕКТ
Ожидаемые результаты:
- Стабильность усвоения программного материала, положительная динамика результатов мониторинга химических знаний обучающихся;
- Высокий рейтинг учащихся по результатам государственной (итоговой) аттестации в форме Единого государственного экзамена по предмету химия;
- Сформированность активной учебно-познавательной деятельности обучающихся (повышение положительной мотивации учения, познавательного интереса);
- Сформированность профессиональных намерений и способностей учащихся старшей ступени общеобразовательной школы;
- Развитие способностей действовать в различных проблемных ситуациях, принимать оптимальные решения; активное включение обучающихся в разработку проектов, а также их активное участие в городских, муниципальных, окружных мероприятиях;
- Стабильное поступление выпускников в высшие учебные заведения химико-биологической направленности.
РЕЗУЛЬТАТЫ
- Создание электронного пособия для подготовки учащихся 11-ых классов к ЕГЭ по химии.
- Публикации педагогического опыта. Всероссийский уровень.
Разработки уроков по химии: «Химический марафон: обобщающий урок для 8 класса» Тесты для подготовки к ЕГЭ по темам: «Строение атома», «Химическая связь», «Металлы», «Классы неорганических веществ», «Генетическая связь между классами неорганических веществ», «Электролитическая диссоциация», «Свойства классов неорганических веществ», «Типы химических реакций», «Задачи на растворы», «Задачи на выведение молекулярной формулы вещества», «Свойства веществ и их применение», «получение веществ». Сайт «Сеть работников образования (ns.portal.ru)
3. Качество обучения по освоению программы курса химии:
|
Учебный год |
Общая успеваемость по химии |
качественная успеваемость по химии |
|
2012-2013 |
100% |
44% |
|
2013-2014 |
100% |
56% |
|
2014-2015 |
100% |
56% |
|
2015-2016 |
100% |
63% |
|
2016-2017 |
100% |
65% |
- Результаты учащихся на государственной итоговой аттестации по предмету химия:
-результаты ОГЭ: 2017 г. – успеваемость-100%, качество-83%, средний балл-20;
-результаты ЕГЭ стабильные: все учащиеся проходят минимальный порог, средний балл выше городских и окружных значений: 2013г.-73,8 баллов; 2014г.-54,33 балла; 2015г.-51 балл; 2016г.-54 балла.5.
4. Результаты предметной олимпиады:
II этап Всероссийской олимпиады школьников по химии:
-призеры муниципального этапа Всероссийской олимпиады школьников по химии (2013г., 2016г.);
-победитель муниципального этапа Всероссийской олимпиады школьников по химии (2015г.);
-участие во II всероссийской дистанционной олимпиаде по химии (2012г.);
-участие в городском химико-географическом квесте «Звездный десант»(2013г.);
-участие в городском Фестивале наук (2017г.).
ЛИТЕРАТУРА
- Беспалько В.П. Слагаемые педагогической технологии — М., Педагогика, 1989;
- Инновационные образовательные технологии [Электронный ресурс] http://www.refobrspb.ru/way5.html;
- Кларин М.В. Технология учебного процесса /Современная дидактика: Теория –практике / Под ред. Лернера, И.К Журавлева, М., 1994;
- Селевко Г.К. Современные образовательные технологии: Учебное пособие. — М., Народное образование, 1998;
- Современные образовательные технологии [Электронный ресурс] // http://charko.narod.ru/tekst/an4/1.html;
Документы:
- Проект национальной образовательной инициативы «Наша новая школа» (2008 г.)
- Приоритетный национальный проект «Образование»(2009-2012 гг.)
- Концепция развития системы непрерывного образования в РФ до 2012 г.
- Федеральный государственный образовательный стандарт (2009г.)
- Федеральная целевая программа развития образования в РФ (2009-2015гг.)
- Закон РФ «Об образовании» (1992-2010 гг.)

Подготовка к ЕГЭ начинается с
психологического настроя на успех, обязательную сдачу ЕГЭ.
Поэтому не
лишними будут помощь психолога, советы родителей и учителей.
Теория к ЕГЭ. Методика самостоятельной подготовки к ЕГЭ
ТЕОРИЯ ДЛЯ СДАЮЩИХ ЕГЭ
Дopoнькин ЕГЭ. Химия. Большой справочник
Adobe Acrobat Document
7.6 MB
РАСПЕЧАТАТЬ И ИСПОЛЬЗОВАТЬ
Методические рекомендации по подготовке
Adobe Acrobat Document
375.5 KB
ПРОРАБОТАТЬ И ПРИНЯТЬ К СВЕДЕНИЮ
анализ типичных ошибок ЕГЭ-2019 г.pdf
Adobe Acrobat Document
771.7 KB
ПРОГРАММА ПОДГОТОВКИ К ЕГЭ ПО ХИМИИ.doc
Microsoft Word Document
129.5 KB
ВНИМАНИЕ
Тривиальные названия органических вещест
Adobe Acrobat Document
340.1 KB
Теория и тест для самостоятельной проработки.
Основные способы получения металлов.pptx
Microsoft Power Point Presentation
920.7 KB
Все свойства органических веществ.
Реакции к основным темам курса 10 класса
Microsoft Word Document
158.0 KB
Общие формулы. УЧИТЬ!!!
Общие формулы классов органических вещес
Adobe Acrobat Document
188.4 KB
Металлы. Соединения металлов. УЧИТЬ!!!
Свойства металлов и их соединений.docx
Microsoft Word Document
2.5 MB
Цепочки превращений.
Задание С3. Цепочки превращений..docx
Microsoft Word Document
674.8 KB
Теория по основным классам неорганических соединений.
Основные классы и их свойства.doc
Microsoft Word Document
880.0 KB
Нужно разобраться и выучить.
Ряд активности металлов.pdf
Adobe Acrobat Document
315.0 KB

Документация и подготовка к ЕГЭ
таблица ПСХЭ.doc
Microsoft Word Document
396.5 KB
Таблица растворимости некоторых веществ
Microsoft Word Document
578.5 KB

Дополнительная информация, теория к ЕГЭ
Адреса сайтов подготовки.
Материалы для подготовки к ОГЭ и ЕГЭ.doc
Microsoft Word Document
15.2 KB
Таблица. Качественные признаки веществ.d
Microsoft Word Document
44.8 KB
Ряд ЭО. Названия кислот и остатков. Степ
Microsoft Word Document
518.7 KB
Таблица ПСХЭ . С обозначением классов со
Microsoft Word Document
498.4 KB
цвета оксидов.doc
Microsoft Word Document
24.0 KB
Номенклатура неорганических веществ.doc
Microsoft Word Document
135.5 KB
Определение ионов. Качественные реакции.
Microsoft Word Document
51.0 KB
Часть представленных здесь материалов взята с
сайта учителя химии Сикорской О.Э.
Методическое пособие по подготовке к егэ по химии (органическая химия)
Аннотация к методическому пособию
В пособии представлен собственный многолетний опыт педагога по подготовке учащихся профильных химико-биологических классов к ЕГЭ. Учтены последние аналитические оценки заданий ЕГЭ по органической химии и результаты экзаменов. Пособие позволяет гарантировано улучшить качество знаний учащихся. Отличается от подобных пособий лаконичностью, системностью информации, охватывает только трудные для понимания учащихся темы курса органической химии. Пособие может быть использовано любым учителем химии для повышения уровня собственной теоретической подготовки.
Введение
Говоря о перспективах повышения эффективности подготовки к ЕГЭ, следует учитывать, что единый государственный экзамен является итогом всего школьного курса химии, поэтому подготовка к нему должна вестись системно, на протяжении всего процесса обучения химии в школе.
Структура курса химии в старшем звене средней школы авторами разных учебников видится по-разному. Авторы многих УМК для средней школы (Гузей Л.С., Кузнецова Л.М., Иванова Р.Г., Новошинский И.И.) предлагают курс химии 10 класса посвятить углубленному изучению неорганической и общей химии, оставив курс органической химии на 11 класс. В других УМК (Габриелян О.С., Рудзитис Г.Е., Кузнецова Н.Е.) предусмотрено изучение органической химии в 10 м классе, а в 11-м изучается курс общей химии. Нам представляется, что второй подход более целесообразен, в том числе и в плане подготовки к ЕГЭ по химии. В пользу такого выбора можно привести следующие доводы:
Изучение курса «Органической химии» в 10-м классе может базироваться на тех пусть небольших знаниях, которые ученики получили при изучении темы «Органические вещества» в 9-м классе. Если эти знания останутся не востребованы в течение еще одного учебного года, они будут полностью утеряны;
Изучение объемного и во многом специфичного материала «Органической химии» будет проходить эффективней в 10-м классе, чем 11-м, поскольку последний загружен подготовкой школьников к итоговой аттестации по различным предметам, психологически и эмоционально более напряжен;
При изучении «Органической химии» в 11-м классе практически не остается возможности для повторения и обобщения всего школьного курса химии, что важно для успешной итоговой аттестации по предмету.
Таким образом, даже если выбранный УМК предусматривает изучение «Органической химии» в 11-м классе, рекомендуется изменить программу и по учебникам 11 класса работать в 10-м.
Основной учебной целью предлагаемого пособия является формирование прочных знаний курса органической химии. Одновременно продолжается развитие умений самостоятельно работать с литературой, систематически заниматься решением задач, работать с тестами различных типов.
Лекционные, объяснительно-иллюстративные методы проведения занятий по подготовке к ЕГЭ обычно малоэффективны. Знания лучше усваиваются человеком, когда он осознал их необходимость. Поэтому занятия можно начинать с решения кратких тестов в парной или групповой работе в сотрудничестве с учителем. Ошибки, допущенные при выполнении этих тестов, служат основой для кратких разъяснений с опорой на теоретический материал, сделанных учителем или наиболее сильными учениками. Полученные знания закрепляются новой серией упражнений, задач, тестов. Тесты и задания, выполненные в ходе самостоятельной работы, вопросы, возникшие при этом, также обсуждаются на занятиях, в том числе и при работе в парах сменного состава. Учитель при этом выступает консультантам по самым сложным вопросам.
При групповой работе учащиеся получают тест, самостоятельно распределяют вопросы теста между членами группы, каждый ученик самостоятельно готовит ответы на свои вопросы теста. Сильные ученики, справившись со своими вопросами, помогают более слабым товарищам найти нужный ответ и его аргументировать. Затем все вопросы теста обсуждается в группе с тем, чтобы каждый ученик мог аргументировать ответ на любой вопрос.
Для успешной работы на ЕГЭ и на других видах контроля в аналогичном формате, ученики должны знать основные виды заданий, ориентироваться в их структуре, понимать, в какой форме нужно давать ответ. Большую помощь в подготовке к экзамену ученикам и педагогам окажет предлагаемое пособие.
1 тема. Основные понятия органической химии. Номенклатура органических соединений. Классы органических веществ.
Органическая химия – это раздел химической науки, в котором изучаются соединения углeрода, их строение, свойства, способы получения и практического использования. Соединения, в состав которых входит углерод, называются органическими. Кроме углерода, они почти всегда содержат водород, довольно часто – кислород, азот и галогены, реже – фосфор, серу и другие элементы.
Ряд соединений, в котором каждый член отличается от предыдущего на постоянную структурную единицу, называется гомологическим рядом. Члены этого ряда называются гомологами.
Структурными изомерами называются вещества, которые имеют одинаковый количественный и качественный состав, но различное строение.
Первичный углеродный атом связан только с одним другим атомом углерода. Вторичный углеродный атом связан только с двумя другими атомами углерода. Третичный углеродный атом связан только с тремя другими атомами углерода. Четвертичный углеродный атом связан с четырьмя атомами углерода. Рассмотрим это на примере 2,2,4-триметилпентана (изооктана):
Алканы – предельные углеводороды. Их общая формула СnH2n+2. Предельные углеводороды называют насыщенными. В насыщенных соединениях все свободные валентности атома углерода насыщены водородом или другими атомами. Первые четыре члена ряда алканов имеют случайные названия. Начиная с пятого члена ряда, названия алканов происходят от греческого слова, которое обозначает число атомов углерода с добавлением окончания «ан».
Алкены — ациклические углеводороды, содержащие в молекуле помимо одинарных связей, одну двойную связь между атомами углерода и соответствующие общей формуле СnН2n.
1. Выбор главной цепи. Образование названия углеводорода начинается с определения главной цепи — самой длинной цепочки атомов углерода в молекуле. В случае алкенов главная цепь должна содержать двойную связь.
2. Нумерация атомов главной цепи. Нумерация атомов главной цепи начинается с того конца, к которому ближе находится двойная связь.
Например,правильное название соединения:

5-метилгексен-2
Если по положению двойной связи нельзя определить начало нумерации атомов в цепи, то его определяет положение заместителей так же, как для предельных углеводородов.

3. Формирование названия. В конце названия указывают номер атома углерода, у которого начинается двойная связь, и суффикс -ен, обозначающий принадлежность соединения к классу алкенов. Например:

Алкины — ациклические углеводороды, содержащие в молекуле помимо одинарных связей, одну тройную связь между атомами углерода и соответствующие общей формуле СпН2n-2. Наличие тройной связи в молекулах углеводородов этого класса отражается суффиксом — ин, а ее положение в цепи — номером атома углерода. Например:

Циклоалканы – это предельные (насыщенные) углеводороды, которые содержат замкнутый углеродный цикл. Общая формула циклоалканов CnH2n,
По правилам международной номенклатуры:
1. В циклоалканах главной считается цепь углеродных атомов, образующих цикл.
2. Название строится по количеству атомов в замкнутой цепи с добавлением приставки «цикло».
3. При наличии в цикле заместителей нумерацию атомов углерода в кольце проводят так, чтобы ответвления получили, возможно, меньшие номера.

Алкадиены (диены) – непредельные алифатические углеводороды, молекулы которых содержат две двойные связи. Общая формула алкадиенов СnH2n-2. По правилам IUPAC главная цепь молекулы алкадиена должна включать обе двойные связи. Нумерация атомов углерода в цепи проводится так, чтобы двойные связи получили наименьшие номера. Названия алкадиенов производят от названий соответствующих алканов (с тем же числом атомов углерода) с добавлением окончания –диен.
Ароматические углеводороды (Арены) – это органические соединения, в молекулах которых имеется одно или несколько бензольных колец. Бензольное кольцо, или ядро, – циклическая группа атомов углерода с особым характером связей.Общая формула — CnH2n-6. Номенклатура. Широко используются тривиальные названия (толуол, ксилол, кумол и т.п.). Систематические названия строят из названия углеводородного радикала (приставка) и слова бензол (корень):С6Н5СH3 метилбензол(толуол) ,С6Н5С2H5— этилбензол, С6Н5—С3H7— пропилбензол.
Если радикалов два или более, их положение указывается номерами атомов углерода в кольце, с которыми они связаны. Нумерацию кольца проводят так, чтобы номера радикалов были наименьшими.
Для дизамещенных бензолов R-С6Н4—R используется также и другой способ построения названий, при котором положение заместителей указывают перед тривиальным названием соединения приставками:
орто— (о-) заместители у соседних атомов углерода кольца, т.е. 1,2;
мета— (м-) заместители через один атом углерода (1,3);
пара— (п-) заместители на противоположных сторонах кольца (1,4).
Ароматические одновалентные радикалы имеют общее название «арил«.
Из них наиболее распространены в номенклатуре органических соединений два: С6Н5— фенил и С6Н5-СH2— бензил.
Спиртами (или алканолами) называются органические вещества, молекулы которых содержат одну или несколько гидроксильных групп (групп —ОН), соединенных с углеводородным радикалом. Общая формула— СnН2n+1ОН. При образовании названий спиртов к названию углеводорода,соответствующего спирту,добавляют (родовой) суффикс-ол. Цифрами после суффикса указывают положение гидроксильной группы в главной цепи, а префиксами ди-, три-,тетра- и т.д.-их число:
Альдегидами называются производные углеводородов, в молекулах которых карбонильная группа связана с углеводородным радикалом и атомом водорода. Общая формула- CnH2nО. Название альдегида по международной номенклатуре (систематической) образуется от названия соответствующего алкана с таким же числом атомов углерода с добавлением окончания –аль. Нумерацию углеродной цепи начинают от атома углерода альдегидной группы (карбонильный атом углерода).
Кетоны – органические вещества, в молекулах которых карбонильная группа связана с двумя углеводородными радикалами. Общая формула- CnH2nО.Очевидно, общая формула кетонов имеет вид:

Карбонильную группу кетонов называют кетогруппой.
В простейшем кетоне – ацетоне – карбонильная группа связана с двумя метильными радикалами:

Класс карбоновых кислот объединяет соединения с функциональной группой -COOH, называемой карбоксилом. Общая формула- CnH2nО2. Систематические названия кислот образуются, путем прибавления к названию углеводорода с соответствующим числом углеродных атомов окончания –овая и слова кислота.
Сложные эфиры — производные кислот (карбоновых или минеральных, одноосновных или многоосновных), в которых атомы водорода гидроксильных групп -ОН замещены на углеводородные радикалы R. Общая формула- CnH2nО2.
Амины – азотсодержащие органические вещества, производные аммиака (NH3), в молекулах которых один или несколько атомов водорода замещены на углеводородный радикал (- R или – CnH2n+1). В большинстве случаев названия аминов образуют из названий углеводородных радикалов и суффикса амин. Например, CH3-NH2-Метиламин,CH3-CH2-NH2 Этиламин . Различные радикалы перечисляются в алфавитном порядке — CH3-CH2-NH-CH3 Метилэтиламин .
Задание 11. Тема — Номенклатура и классификация органических соединений. :
1)Установите соответствие между названием соединения и общей формулой гомологического ряда, к которому оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ СОЕДИНЕНИЯ |
ОБЩАЯ ФОРМУЛА |
|
|
А) бутин Б) циклогексен В) бутадиен-1,2 |
1) 2) 3) 4) |
2)Установите соответствие между названием соединения и общей формулой гомологического ряда, к которому оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ СОЕДИНЕНИЯ |
ОБЩАЯ ФОРМУЛА |
|
|
А) бутан Б) бутин-1 В) циклогексан |
1) 2) 3) 4) |
3)Установите соответствие между названием соединения и общей формулой гомологического ряда, к которому оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ СОЕДИНЕНИЯ |
КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ |
|
|
А) бутадиен-1,3 Б) 2-метилпропанол-1 В) этилформиат |
1) простые эфиры 2) сложные эфиры 3) спирты 4) углеводороды |
4)Установите соответствие между формулой вещества и классом (группой) органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ФОРМУЛА ВЕЩЕСТВА |
КЛАСС (ГРУППА) СОЕДИНЕНИЙ |
|
|
А) Б) В) |
1) предельный одноатомный спирт 2) алкен 3) предельный альдегид 4) алкадиен |
5)Установите соответствие между формулой вещества и классом (группой) органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ФОРМУЛА ВЕЩЕСТВА |
КЛАСС (ГРУППА) СОЕДИНЕНИЙ |
|
|
А) Б) В) |
1) сложные эфиры 2) спирты 3) простые эфиры 4) углеводы |
6)Установите соответствие между общей формулой гомологического ряда и классом (группой) органических соединений, соответствующим этой формуле: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ОБЩАЯ ФОРМУЛА РЯДА |
КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ |
|
|
А) Б) В) |
1) предельные альдегиды 2) одноатомные фенолы 3) предельные одноатомные спирты 4) предельные двухатомные спирты |
7)Установите соответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА КЛАСС/ГРУППА
А) аланин 1) аминокислоты
Б) анилин 2) спирты
В) дивинил 3) непредельные углеводороды
4) амины

НАЗВАНИЕ ВЕЩЕСТВА КЛАСС/ГРУППА
А) аланин 1) углеводороды
Б) толуол 2) спирты
В) стирол 3) аминокислоты
4) фенолы
9)Установите соответствие между формулой вещества и его названием: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА НАЗВАНИЕ ВЕЩЕСТВА
А) C2H6O2 1) метанол
Б) CH2O2 2) пропанол
В) C4H8O 3) этиленгликоль
4) муравьиная кислота
5) бутаналь
10) Установите соответствие между формулой вещества и его названием: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА НАЗВАНИЕ ВЕЩЕСТВА
А) C4H6 1) бутадиен-1,3
Б) C4H4 2) хлорэтан
В) C2H3Cl 3) хлорэтен
4) винилацетилен
5) циклобутан
11) Установите соответствие между общей формулой гомологического ряда и названием вещества, принадлежащего к нему: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ОБЩАЯ ФОРМУЛА НАЗВАНИЕ ВЕЩЕСТВА
А) CnH2n–6 1) толуол
Б) CnH2n+2 2) гексан
В) CnH2n 3) изопрен
4) метилциклопропан
12)Установите соответствие между названием вещества и классом/группой органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА КЛАСС/ГРУППА ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ
А) целлюлоза 1) моносахариды
Б) сахароза 2) дисахариды
В) фруктоза 3) полисахариды
4) сложные эфиры
13) Установите соответствие между формулой вещества и классом/группой органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА КЛАСС/ГРУППА ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ
А) HCOOCH3 1) простые эфиры
Б) С6Н5СНО 2) кетоны
В) C6H5ОС6Н5 3) cложные эфиры
4) альдегиды
14) Установите соответствие между названием вещества и классом/группой органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА КЛАСС/ГРУППА ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ
А) дезоксирибоза 1) спирты
Б) цис-бутен-2 2) углеводороды
В) крахмал 3) углеводы
4) пептиды
15)Установите соответствие между формулой вещества и классом (группой) органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ
А) С6H12O6 1) сложные эфиры
Б) HCOOCH3 2) простые эфиры
В) СH3OCH3 3) кетоны
4) углеводы
5) амины
6) углеводороды
16) Установите соответствие между формулой вещества и классом (группой) органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ
А) CH3CHO 1) сложные эфиры
Б) C8H10 2) простые эфиры
В) СH3NH2 3) альдегиды
4) углеводы
5) амины
6) углеводороды
17)Установите соответствие между названием вещества и общей формулой класса (группы) органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ОБЩАЯ ФОРМУЛА |
|
|
А) рибоза Б) ацетон В) изопрен |
1) 2) 3) 4) |
18) Установите соответствие между молекулярной формулой вещества и классом (группой) органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
МОЛЕКУЛЯРНАЯ ФОРМУЛА |
КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ |
|
|
A) Б) В) |
1) многоатомные спирты 2) одноатомные спирты 3) одноосновные кислоты 4) алкины |
19)Установите соответствие между названием вещества и классом (группой) органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ |
|
|
A) циклогексан Б) лактоза B) фенилаланин |
1) карбоновые кислоты 2) аминокислоты 3) углеводороды 4) углеводы 5) фенолы |
20)Установите соответствие между названием органического соединения и классом, к которому оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ СОЕДИНЕНИЯ |
КЛАСС ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ |
|
|
А) 2-метилпропанол-2 Б) цис-бутен-2 В) фенилаланилглицин |
1) спирты 2) пептиды 3) углеводороды 4) эфиры |
Задание 12. 2 тема Теория строения органических соединений. Изомерия.
Гибридизация — это мысленная операция превращения обычных (энергетически наиболее выгодных) атомных орбиталей в новые орбитали, геометрия которых соответствует экспериментально определенной геометрии молекул.
Можно предложить два способа определения типа гибридизации различных атомов в молекуле.
Способ 1. Наиболее общий способ, пригодный для любых молекул. Основан на зависимости валентного угла от гибридизации:
а) валентные углы 109,5°, 107° и 105° свидетельствуют об sр3-гибридизации;
б) валентный угол около 120° -sр2-гибридизация;
в) валентный угол 180°-sp-гибридизация.
Способ 2. Пригоден для большинства органических молекул. Поскольку тип связи (простая, двойная, тройная) связан с геометрией, можно по характеру связей данного атома определить тип его гибридизации:
а) все связи простые – sр3-гибридизация;
б) одна двойная связь – sр2 -гибридизация;
в) одна тройная связь — sp-гибридизация.
Одна из характеристик химических связей — тип перекрывания орбиталей атомов в молекуле.
По характеру перекрывания различают σ-(сигма) и π‑(пи) связи. σ-Связь — это связь, в которой перекрывание орбиталей происходит вдоль оси, соединяющей ядра атомов. π-Связь — это связь, в которой перекрывание орбиталей происходит в плоскости, перпендикулярной оси, соединяющей ядра атомов, сверху и снизу от оси связи.
π-Связь является дополнительной к σ-связи, она менее прочная и легче разрывается при химических реакциях.
|
Одинарная связь С–С, С–Н, С–О |
Двойная связь С=С, С=О |
Тройная связь С≡С, С≡N |
|
σ-связь |
σ-связь + π-связь |
σ-связь + две π-связи |
Таким образом, число сигма-связей (σ-связей) в молекуле метана равно четырем:
В молекуле этилена число сигма-связей равно пяти, а также есть одна пи-связь (между атомами углерода):
В молекуле ацетилена всего три сигма-связи и две пи-связи: H–C≡C–H
Изомеры – это вещества, имеющие одинаковый состав (число атомов каждого типа), но разное взаимное расположение атомов – разное строение.
Изомерия – это явление существования веществ с одинаковым составом, но различным строением.
Например, формуле C4H10 соответствуют два изомерных соединения н-бутан с линейным углеродным скелетом и изобутан (2-метилбутан) с разветвленным скелетом:

Виды изомерии
Различают два основных вида изомерии: структурную и пространственную (стереоизомерию).
Структурная изомерия
Структурные изомеры – соединения с одинаковым составом, но различным порядком связывания атомов, т.е. с различным химическим строением. Молекулярная формула у структурных изомеров одинаковая, а структурная различается.
1. Изомерия углеродного скелета: вещества различаются строением углеродной цепи, которая может быть линейная или разветвленная.
Например, молекулярной формуле С5Н12 соответствуют три изомера:

2. Изомерия положения обусловлена различным положением кратной связи, функциональной группы или заместителя при одинаковом углеродном скелете молекул.
2.1. Изомерия положения функциональной группы. Например, существует два изомерных предельных спирта с общей формулой С3Н8О: пропанол-1 (н-пропиловый спирт) пропанол-2 (изопропиловый спирт):

2.2. Изомерия положения кратной связи может быть вызвана различным положением кратной (двойной или тройной) связи в непредельных соединениях. Например, в бутене-1 и бутене-2:

2.3. Межклассовая изомерия – ещё один вид структурной изомерии, когда вещества из разных классов веществ имеют одинаковую общую формулу.
Например, формуле С2Н6О соответствуют: спирт (этанол) и простой эфир (диметиловый эфир):


Пространственная изомерия
Пространственные изомеры – это вещества с одинаковым составом и химическим строением, но с разным пространственным расположением атомов в молекуле. Виды пространственной изомерии – геометрическая (цис—транс) и оптическая изомерия.
Геометрическая изомерия (или цис-транс-изомерия).
Геометрическая изомерия характерна для соединений, в которых различается положение заместителей относительно плоскости двойной связи или цикла. Например, для алкенов и циклоалканов.
Двойная связь не имеет свободного вращения вокруг своей оси.
Поэтому заместители у атомов углерода при двойной связи могут быть расположены либо по одну сторону от плоскости двойной связи (цис-изомер), либо по разные стороны от плоскости двойной связи (транс-изомер). При этом никаким вращением нельзя получить из цис-изомера транс-изомер, и наоборот.
Например, бутен-2 существует в виде цис— и транс-изомеров

1,2-Диметилпропан также образует цис-транс-изомеры:

Для соединений вида СH2=СHR и СR2=СHR’ цис—транс-изомерия не характерна.
12 задание ЕГЭ.Теория строения органических соединений. Изомерия.
Тесты . Выберите из предложенного перечня 2 правильных ответа.:
1) Из предложенного перечня выберите два вещества, которые содержат атомы углерода в состоянии sp-гибридизации.
бутан
бутин-1
бутен-1
бутадиен-1,2
бутадиен-1,3
2) Из предложенного перечня выберите два вещества, которые содержат атомы углерода в первом валентном состоянии.
n-гексан
этилен
ацетилен
бензол
этан
3) Из предложенного перечня выберите два вещества, которые содержат π-связи.
циклобутан
уксусная кислота
тетрахлорметан
дивинил
1,2-дихлорбутан
4) Из предложенного перечня выберите два вещества, в молекулах которых содержатся только σ-связи.
циклогексан
винилацетилен
толуол
изопентан
пропилен
5) Из предложенного перечня выберите два вещества, в молекулах которых встречаются атомы углерода с длиной связи между ними 0,12 нм и углом между связями 180°.
этан
ацетилен
гептен-1
гептен-2
пентин-1
6) Из предложенного перечня выберите два класса веществ, в молекулах которых присутствует функциональная группа
спирты
кетоны
простые эфиры
фенолы
пептиды
7) Из предложенного перечня выберите два типа гибридизации орбиталей атома углерода, которые имеются в молекуле 2-метилбутена-2.
sp3
sp2
sp
sp3 и sp
sp2 и sp

CH3NO2 и CH3NH2
CH3OH и CH3COOH
CH3CH2CH2OH и CH3OH
CH3Cl и CH3Br
CH3CHO и C2H5COH
9) Из предложенного перечня выберите два вещества, в молекулах которых имеется две π-связи.
акриловая кислота
пропен
бутан
бутен
ацетилен
10) Из предложенного перечня выберите два вещества, которые относятся к тем же гомологическим рядам, что и вещества, имеющие молекулярную формулу С5Н10.
метан
этилен
бензол
циклопропан
ацетилен
11) Из предложенного перечня выберите два вещества, которые являются структурными изомерами пентена-1.
циклопентан
пентадиен-1,3
2-метилбутан
2-метилбутен-2
3-метилбутин-1
12) Из предложенного перечня выберите два класса органических веществ, к которым может относиться вещество, формула которого C4H10O.
спирты
альдегиды
простые эфиры
сложные эфиры
кетоны
13) Из предложенного перечня выберите два вещества, между молекулами которых образуются водородные связи.
этанол
этан
этаналь
ацетон
этановая кислота
14) Из предложенного перечня выберите два вещества, которые имеют систему сопряжённых связей.
фенол
бутадиен-1,3
циклогексен
2-метилбутан
бутин-1
15) Из предложенного перечня выберите две пары веществ, каждое из которых содержит функциональную группу –ОН.
фенол и рибоза
диэтиловый эфир и глюкоза
сахароза и формальдегид
фенол и толуол
пропанол и крезол
16) Из предложенного перечня выберите два вещества, которые являются гомологами глицина.
CH3CH2CONH2
CH3CH(NH2)COOH
CH3CH2COOH
CH3CH2CH(NH2)COOH
CH3CH2NH2
17) Из предложенного перечня выберите два вещества, которые являются гомологами бензола.
циклогексан
толуол
ацетилен
винилбензол
фенилэтан
18) Из предложенного перечня выберите два вещества, которые содержат атомы углерода только в состоянии sp3-гибридизации.
1) бутан 2) циклобутан 3) ацетон 4) бутадиен-1,3 5) бензол
19) Из предложенного перечня выберите два вещества, в молекулах которых только один атом углерода находится в состоянии sp2-гибридизации.
1) CH3-CH2-CHO 2) CH2=CH-CH3 3) HCOOH 4) CH2=CH-COOH 5) C6H5-CHO
20) Из предложенного перечня выберите два вещества, для которых не характерна изомерия углеродного скелета. 1) бутин-1 2) 2-метилбутен-2 3) пропандиол-1,2 4) бутаналь 5) изобутан
21) Из предложенного перечня выберите два вещества, которые являются изомерами.
1) бутилформиат 2) 2-метилпропаналь 3) 2-метилпропанол-2 4) диэтиловый эфир 5) пропилформиат
22) Из предложенного перечня выберите два вещества, в молекулах которых имеется одна или несколько гидроксильных групп. 1) толуол 2) стирол 3) этанол 4) бензол 5) глицерин
23) Из предложенного перечня выберите два вещества, которые являются гомологами уксусной кислоты. 1) муравьиная кислота 2) хлоруксусная кислота 3) бензойная кислота 4) стеариновая кислота 5) аминоуксусная кислота
24) Из предложенного перечня соединений выберите два таких, которые являются изомерами диизопропилового эфира. 1) гексанол-1 2) изопропанол 3) бутилэтиловый эфир 4) дибутиловый эфир 5) 3-метилбутанол
25) Из предложенного перечня выберите два вещества, молекулы которых содержат только один атом углерода в состоянии sp2-гибридизации. 1) пропаналь 2) пропеновая кислота 3) муравьиная кислота 4) пропен 5) бензальдегид
26) Из предложенного перечня молекулярных формул выберите две таких, которые могут соответствовать веществам с карбоксильной группой в молекуле.
1) C3H4O4 2) C2H4O 3) C3H8O2 4) C5H10O 5) C4H8O2
27) Из предложенного перечня выберите два вещества, которые являются по отношению друг к другу структурными изомерами.
1) 1,1-диметилциклопропан 2) пентин 3) 2-метилциклобутен 4) цис-бутен-2 5) транс-бутен-2
28) Из предложенного перечня соединений выберите два таких, молекулы которых содержат в своем составе карбоксильную группу.
1) этиловый эфир аминоуксусной кислоты 2) глицилаланин 3) анилин 4) фенол 5) трифторуксусная кислота
29) Из предложенного перечня соединений выберите два таких, которые являются изомерами бутилформиата.
1) этилацетат 2) пропилэтаноат 3) изобутилацетат 4) 2-метилбутановая кислота 5) 2,3-диметилбутановая кислота
30) Из предложенного перечня выберите два вещества, которые являются изомерами изопрена.
1) 2-метилбутадиен-1,3 2) 1-метилциклобутен 3) дивинил 4) циклопентадиен-1,3 5) винилциклопропан
31) Из предложенного перечня выберите два вещества, которые не могут существовать в виде геометрических изомеров. 1) 2-метилбутен-2 2) пентен-2 3) 2-метилгексен-3 4) 1,1-дифенилэтен 5) 1,2-дибромпропен
32) Из предложенного перечня формул выберите две таких, которые не могут соответствовать веществам с кратными связями в молекуле. 1) C3H8O3 2) C5H10O 3) C4H10O 4) C4H9N 5) C2H4O
33) Из предложенного перечня соединений выберите два таких, которые не могут существовать в виде цис- и транс-изомеров. 1) 1,2-дихлорпропен 2) 1,2-дихлорэтан 3) нитроэтилен 4) 1,4-дийодбутен-2 5) 3-метилпентен-2
34) Из предложенного перечня соединений выберите два таких, которые являются структурными изомерами.
1) бутаналь 2) изопропиловый спирт 3) пропионовый альдегид 4) 2-метилпропаналь 5) бутанол-1
35) Из предложенного перечня соединений выберите два таких, которые могут существовать в виде геометрических изомеров.
1) пропеновая кислота 2) бутен-2-аль 3) винилэтиловый эфир 4) стирол 5) 1,2-дихлорэтилен
36) Из предложенного перечня соединений выберите два таких, молекулы которых содержат 3 σ-связи. 1) ацетилен 2) этаналь 3) формальдегид 4) метанол 5) метан
37) Из предложенного перечня соединений выберите два таких, молекулы которых содержат атомы углерода в состоянии sp3 -гибридизации. 1) ацетилен 2) этилен 3) изопрен 4) хлоропрен 5) этан
38) Из предложенного перечня соединений выберите два таких, молекулы которых содержат атомы углерода в состояниях sp3 — и sp2 -гибридизации. 1) пропионовая кислота 2) муравьиная кислота 3) этаналь 4) этанол 5) стирол
Тема. Углеводороды. Способы получения и химические свойства.
Задание 13. Тема. Углеводороды. Способы получения и химические свойства.
Тесты. Выберите 2 правильных ответа
1) Из предложенного перечня выберите два вещества, при взаимодействии которых с раствором перманганата калия в присутствии серной кислоты будет наблюдаться изменение окраски раствора.
гексан
бензол
толуол
пропан
пропилен
2) Из предложенного перечня выберите два вещества, из которых напрямую можно получить полимер.
циклопропан
винилацетилен
бутадиен
бензол
пентан
3) Из предложенного перечня выберите два вещества, которые могут быть использованы для получения бензола.
Ацетилен
Этилен
Этан
Бензоат натрия
Бутадиен-1,3
4) Из предложенного перечня выберите два вещества, которые могут при окислении перманганатом калия в кислой среде образовать карбоновые кислоты.
бутен-2
2-метилпропен-1
бутин-1
этилен
бензол
5) Из предложенного перечня выберите два вещества, которые могут получиться при крекинге алканов.
бутан
бензол
пропин
пропен
толуол
6) Из предложенного перечня выберите две реакции, которые можно использовать для получения пентана.
пентен-2 с водородом
C5H11Cl с Na
C5H11COONa с NaOH
циклопентан с хлороводородом
C5H11Cl с KOH
7) Из предложенного перечня выберите две реакции, в каждой из которых образуется ацетилен.
1)CH4 1500°C
→
2)CH4 1000°C
→
3)CH4 700°C
→
Ni
4_CaC2+H2O→
5)CH2=CH2+H2 t°
→
Ni

винилхлорид
дивинил
изопрен
стирол
2-хлорбутадиен-1,3
9) Из предложенного перечня выберите два ряда веществ, при взаимодействии каждого из которых с раствором перманганата калия будет наблюдаться изменение окраски раствора.
ацетилен, п-ксилол, пропилен
хлорэтан, пропан, бензол
циклопентан, этилен, ацетилен
этан, этилен, ацетилен
пропилбензол, дивинил, пропин
10) Из предложенного перечня выберите два вещества, которые могут реагировать с бромоводородом.
метан
полиэтилен
бензол
изобутилен
циклопропан
11) Из предложенного перечня выберите два вещества, которые можно получить гидратацией алкина.
бензол
изопрен
этаналь
ацетон
каучук
12) Из предложенного перечня выберите две реакции, которые можно использовать для получения пентана.
пентен-2 с водородом
C5H11Cl с Na
C5H11COONa с NaOH
циклопентан с хлороводородом
C5H11Cl с KOH
13) Из предложенного перечня выберите две реакции, в которые, в отличие от бутана, может вступать циклобутан.
гидрирование
горение
этерификация
гидрогалогенирование
дегидрирование
14) Из предложенного перечня выберите два вещества, которые могут преимущественно образовываться при действии спиртового и водного растворов гидроксида калия на 2-бромбутан.
бутен-1
бутен-2
циклобутан
бутиловый спирт
бутанол-2
15) Из предложенного перечня выберите два вещества, с которыми может взаимодействовать натрий.
этилен
этан
хлорэтан
ацетилен
полиэтилен
16) Из предложенного перечня выберите два ряда, каждое вещество которых взаимодействует с пропеном.
H2,KOH,H2O
H2O,H2O2,I2
H2,O2,CH4
HBr,NaMnO4,Cl2
C2H6,H2O,HBr
17) Из предложенного перечня выберите два типа реакций, в каждую из которых вступают как н-гептан, так и метилциклогексан.
дегидрирование
замещение атома водорода на гидроксогруппу
присоединение галогеноводородов
замещение с галогеноводородами
риформинг
18) Из предложенного перечня выберите две реакции, которые можно использовать для получения соответственно циклобутана и циклопропана.
дегидрирование бутана
взаимодействие 1,4-дихлорбутана с цинком
нагревание бутанола-1 с концентрированной H2SO4
нагревание 1,4-дибромбутана и 1,3-дибромпропана со спиртовым раствором NaOH
нагревание 1,3-дибромпропана с цинком
19) Из предложенного перечня выберите два вещества, с каждым из которых реагирует аммиачный раствор оксида серебра.
бутин-2
бутен-2
бутин-1
бутен-1
ацетилен
20) Из предложенного перечня выберите два вещества, которые преимущественно образуются при присоединении бромоводорода к метилпропену и 2-метилбутену-1 соответственно.
2-бром-2-метилпропан
1-бром-2-метилпропан
2-бром-2-метилбутан
1-бром-2-метилбутан
1,2-дибром-2-метилбутан
21) Из предложенного перечня выберите два вещества, которые взаимодействуют с водой в присутствии катализатора. 1) циклогексан 2) бензол 3) бутин-2 4) толуол 5) пропилен
22) Из предложенного перечня выберите две реакции, в результате которых образуется алкан.
1) гидрохлорирование ацетилена 2) гидролиз карбида кальция 3) крекинг пропана 4) деполимеризация полистирола 5) электролиз раствора ацетата натрия
23) Из предложенного перечня выберите два углеводорода, при окислении которых перманганатом калия в кислой среде образуется углекислый газ.
1) этен 2) пропин 3) пентан 4) гексен-3 5) толуол
24) Из предложенного перечня выберите две реакции, в результате которых образуется бензол.
1) окисление метилбензола 2) дегидрирование циклогексана 3) тримеризация этина 4) полимеризация бутадиена-1,3 5) дегидратация пропанола
25) Из предложенного перечня выберите исходные вещества, в результате взаимодействия которых образуется н-бутан.
1) C4H8 и H2 2) C4H9NO2 и H2 3) C3H8 и CH4 4) C2H5Cl и Na 5) CH2Br–CH2–CH2–CH2Br и Zn
26) Из предложенного перечня выберите две реакции, в результате каждой из которых образуется пропен.
1) дегидратация пропанола-1 2) тримеризация этина 3) дегидрирование пропанола-2 4) окисление бутена-1 5) дегалогенирование 1,2-дибромпропана
27) Из предложенного списка веществ выберите те, которые реагируют со стиролом,но не реагируют с кумолом.
1)бром 2)натрий 3)бромоводород 4)кислород 5)вода
28) Из предложенного перечня выберите два вещества, с которыми циклобутан взаимодействует, а бутан нет.
1) Br2 2) H2 3) H2S 4) HCl 5) O2
29) Из предложенного перечня выберите два вещества, каждое из которых обесцвечивает нейтральный раствор перманганата калия.
1) толуол 2) 2-метилбутан 3) циклопентан 4) циклогексен 5) бензол
30) Из предложенного перечня веществ выберите те, которые реагируют и с толуолом, и с циклогексеном.
1) калий 2) перманганат калия 3) водород 4) бромная вода 5) бромоводород
31) Из предложенного перечня выберите два вещества, при взаимодействии каждого из которых с натрием протекает реакция замещения.
1) толуол 2) ацетилен 3) 3-метилбутин-1 4) 2-метилпропан 5) пропилен
32) Из предложенного перечня выберите два вещества, которые не могут вступать в реакцию радикального замещения с хлором.
1) толуол 2) кумол 3) бензойная кислота 4) этан 5) бензол
33) Из предложенного перечня выберите два утверждения, которые справедливы для характеристики реакции метана с хлором.
1) начинается с разрыва связи между атомами углерода 2) протекает по радикальному механизму 3) протекает по ионному механизму 4) является окислительно-восстановительной 5) является каталитической
34)Из предложенного перечня выберите два вещества, которые могут быть синтезированы в одну стадию из бутана.
1) этанол 2) дивинил 3) изопрен 4) ацетилен 5) этановая кислота
35) Из предложенного перечня выберите два вещества, которые можно окислить до бензойной кислоты.
1) 1,3-диметилбензол 2) п-метилстирол 3) толуол 4) бензол 5) этилбензол
36) Из предложенного перечня выберите два вещества, с которыми может вступать в реакцию бутин-2.
1) [Ag(NH3)2]OH 2) Na 3) H2O 4) Cu(OH)2 5) KMnO4
37) Из предложенного перечня выберите два утверждения, справедливые для циклопропана.
1) не имеет изомеров 2) вступает в реакции присоединения 3) относится к непредельным углеводородам 4) при нормальных условиях является газом 5) хорошо растворим в воде
38) Из предложенного перечня выберите два вещества, для которых невозможно 1,4-присоединение.
1) изопрен 2) пентадиен-1,4 3) бутадиен-1,3 4) хлоропрен 5) гексадиен-1,5
16 задание
Химические свойства углеводородов.
1) Установите соответствие между схемой реакции и веществом X, которое принимает в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ ВЕЩЕСТВО Х
А) X + Zn =циклопропан 1) 1-хлорпропан
Б) X + Na =гексан 2) 1,2-дихлорпропан
В) X + Mg =пропен 3) 1,3-дихлорпропан
Г) X + Mg =метилциклопропан 4) 1-хлорбутан
5) 1,3-дихлорбутан
6) 1,4-дихлорбутан
2) Установите соответствие между названием углеводорода и продуктом его полного гидрирования: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ УГЛЕВОДОРОДА ПРОДУКТ ГИДРИРОВАНИЯ
А) циклогексен 1) бутан
Б) бензол 2) бутен-2
В) бутин-2 3) гексан
Г) винилацетилен 4) циклогексан
5) бензиловый спирт
6) бутадиен-1,3
3) Установите соответствие между реагирующими с хлором веществами и преимущественно образующимся продуктом реакции и условиями осуществления этих реакций: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГЕНТ И ПРОДУКТ РЕАКЦИИ |
УСЛОВИЯ ОСУЩЕСТВЛЕНИЯ РЕАКЦИИ |
|
А) циклопропан → 1,3-дихлорпропан |
1) ультрафиолетовое облучение |
4) Установите соответствие между реагирующими веществами и характеристикой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ХАРАКТЕРИСТИКА РЕАКЦИИ |
|
А) CH4+Cl2→ |
1) ионная полимеризация |
5)Установите соответствие между названием исходного вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с хлором: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
А) пропан |
1) |
6) Установите соответствие между химической реакцией и органическим веществом, которое преимущественно образуется в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАКЦИЯ |
ПРОДУКТ РЕАКЦИИ |
|
А) гидратация этина с перманганатом калия (H2SO4 р-р) |
1) |
7) Установите соответствие между формулами исходных веществ и продуктом, который преимущественно образуется при взаимодействии этих веществ с водой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ФОРМУЛА ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
А) CH3–CH=CH2 |
1) этанол |

|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
А) пропен |
1) фенол |
9) Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с избытком хлороводорода: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТЫ РЕАКЦИИ |
|
А) пропен |
1) 2-хлорпропан |
10) Установите соответствие между исходным веществом и продуктом, который преимущественно образуется при взаимодействии этого вещества с хлором при освещении: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ИСХОДНОЕ ВЕЩЕСТВО |
ПРОДУКТ РЕАКЦИИ |
|
А) 2-метилбутан |
1) хлорциклогексан |
11) Установите соответствие между преимущественно образующимся продуктом реакции и веществом, которое взаимодействовало со спиртовым раствором гидроксида калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ПРОДУКТ РЕАКЦИИ |
РЕАГИРУЮЩЕЕ ВЕЩЕСТВО |
|
А) 2-метилпропен |
1) 1-бромпентан |
12) Установите соответствие между исходными веществами и продуктами их дегалогенирования: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
А) 1,4-дибромбутан |
1) циклобутан |
13) Установите соответствие между реагирующими с хлором веществами и преимущественно образующимся продуктом реакции и условиями осуществления этих реакций: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГЕНТ И ПРОДУКТ РЕАКЦИИ |
УСЛОВИЯ ПРОВЕДЕНИЯ РЕАКЦИИ |
|
А) бензол → хлорбензол |
1) ультрафиолетовое облучение |
14) Установите соответствие между формулой одного из реагирующих веществ и названием одного из продуктов, который можно получить. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЯ ВЕЩЕСТВ |
ПРОДУКТ РЕАКЦИИ |
|
А) C2H2 |
этиловый спирт нитроэтан нитробензол пропанол бензол пропионовая кислота |
15) Установите соответствие между названиями класса веществ и названием типа реакции, характерной для этого класса. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЯ ВЕЩЕСТВ |
ТИП РЕАКЦИИ |
|
А) алкан |
нитрование полимеризация с образованием продукта, который является основой для получения каучуков этерификация гидролиз гидратация с образованием спиртов гидратация с образованием альдегида или кетона |
16) Установите соответствие между тривиальными названиями реагирующих веществ и названиями продуктов, которые в этих реакциях образуются. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЯ ВЕЩЕСТВ |
ПРОДУКТЫ РЕАКЦИИ |
|
А) ацетилен + вода |
бутан этанол бутанол-1 этаналь поливинилацетилен бутадиен-1,3 |
17) Установите соответствие между названием углеводорода и продуктом реакции, который образуется преимущественно при взаимодействии его с избытком брома. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЯ ВЕЩЕСТВ |
ПРОДУКТЫ РЕАКЦИИ |
|
А) ацетилен |
1,1 — дибромэтан 1,2-дибромэтан 1,1,2,2 — тетрабромэтан 1,2,3,4-тетрабромбутан 1,1,2,2,3,4-гексабромбутан 1,2 — дибромбутан |
18) Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с бромом: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА
этан
изобутан
циклопропан
циклогексан
19) Установите соответствие между названием вещества и продуктом, который преимущественно образуется при его взаимодействии с избытком хлороводорода. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
20) Установите соответствие между названием вещества и органическим продуктом, который образуется при взаимодействии этого вещества с горячим подкисленным раствором перманганата калия. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
21) Установите соответствие между названием вещества и продуктом, который преимущественно образуется при его взаимодействии с избытком спиртового раствора щёлочи при нагревании. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
22) Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с бромом: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
23) Установите соответствие между реагирующими веществами и углеродсодержащим продуктом их взаимодействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
А) CH3-CH2-CH=CH2 + KMnO4 1 ) CH3-C(O)-CH2-CH3
Б) CH3-CH2-C≡CH + H2O 2) CO2 и CH3-CH2-COOH
В) CH3-CH2-CH=CH2 + H2 3) CH3-CH2-C≡CAg
Г) CH3-CH2-C≡CH + Ag2O 4) CH3-CH2-CH2-COOAg
5) CH3-CH2-CH2-CHO
6) CH3-CH2-CH2-CH3
24) Установите соответствие между химической реакцией и органическим веществом, преимущественно образующимся в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАКЦИЯ ПРОДУКТ РЕАКЦИИ
А) гидратация пентена-1 1) пентанон-2
Б) гидрирование циклопропана 2) пентаналь
В) гидратация пентина-1 3) пентанол-2
Г) дегидрирование пропана 4) пентанол-1
5) пропилен
6)пропан
25) Установите соответствие между реагирующими веществами и углеродсодержащим продуктом их взаимодействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
А) C2H4Cl2 + KOH(спирт. р-р) 1) CH3-CH3
Б) C2H4 + H2O 2) CH4
В) C2H2 + H2O 3) CH3-CH2-OH
Г) C2H4Cl2 + Zn 4) CH2=CH2
5) HC≡CН
6) CH3-CHO
26) Установите соответствие между названием углеводорода и продуктом его окисления сернокислым водным раствором перманганата калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
УГЛЕВОДОРОД ПРОДУКТЫ
А) стирол 1) бензойная кислота и муравьиная кислота
Б) циклогексен 2) циклогексанон
В) изопропилбензол 3) циклогесандиол-1,2
Г) циклопентан 4) бензойная кислота и углекислый газ
5) гександиовая кислота
6) циклопентанон
7) исходный углеводород не окисляется в данных условиях
27) Установите соответствие между реагирующими веществами и органическим продуктом, который преимущественно образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
|||||||
|
А) 2-бромпропан и натрий Б) хлорэтан и В) хлорэтан и Г) бутен-2 и водород 28) Установите соответствие между реагирующими веществами и продуктом, который преимущественно образуются в реакции между ними: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
1) гексан 2) 2,3-диметилбутан 3) этанол 4) бутан 5) этаналь 6) этен |
29) Установите соответствие между формулой углеводорода и формулой органического продукта, который преимущественно образуется при взаимодействии углеводорода с водой (в присутствии необходимого катализатора): к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ФОРМУЛА УГЛЕВОДОРОДА |
ФОРМУЛА ПРОДУКТА ВЗАИМОДЕЙСТВИЯ С ВОДОЙ |
|
|
А) Б) В) Г) |
1) 2) 3) 4) 5) 6) |
30) Установите соответствие между формулой углеводорода и формулой органического продукта его взаимодействия с подкисленным раствором перманганата калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ФОРМУЛА УГЛЕВОДОРОДА |
ФОРМУЛА ПРОДУКТА ВЗАИМОДЕЙСТВИЯ С ПЕРМАНГАНАТОМ КАЛИЯ |
|
|
А) Б) В) Г) |
1) 2) 3) 4) 5) 6) |
31) Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с водой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
|
А) этилен Б) ацетилен В) 2-метилпропен Г) фенилацетилен |
1) 2) 3) 4) 5) 6) |
32) Установите соответствие между названием углеводорода и продуктом, который преимущественно образуется при его взаимодействии с азотной кислотой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТЫ РЕАКЦИИ |
|
|
A) метан Б) 2-метилпропан В) толуол Г) трет-бутилбензол |
1) 2) 3) 4) 5) 6) |
33) Установите соответствие между названием вещества и органическим продуктом, который образуется при взаимодействии этого вещества с водным (слабощелочным) раствором перманганата калия
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТЫ РЕАКЦИИ |
|
|
А) ацетилен Б) бутен-2 В) толуол Г) 1,2-диэтилбензол |
1) 2) 3) 4) 5) 6) |
34) Установите соответствие между названием вещества и органическим продуктом, который преимущественно образуется при взаимодействии этого вещества с водой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ОРГАНИЧЕСКИЙ ПРОДУКТ РЕАКЦИИ |
|
|
А) бутин-2 Б) бутин-1 В) бутен-2 Г) 2-метилпропен |
|
35) Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с бромом в соответствующих условиях.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ОРГАНИЧЕСКИЙ ПРОДУКТ РЕАКЦИИ |
|
|
А) циклогексан Б) бензол В) изопропилбензол Г) толуол |
|
36) Установите соответствие между названием вещества и органическим продуктом, который образуется при взаимодействии этого вещества с горячим подкисленным раствором перманганата калия.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ОРГАНИЧЕСКИЙ ПРОДУКТ РЕАКЦИИ |
|
|
А) пентин-1 Б) гексен-3 В) стирол Г) 1,2-диметилбензол |
|
37) Установите соответствие между названием вещества и органическим продуктом, который образуется при взаимодействии этого вещества с водным (слабощелочным) раствором перманганата калия.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ОРГАНИЧЕСКИЙ ПРОДУКТ РЕАКЦИИ |
|
|
А) бутен-1 Б) этилен В) стирол Г) толуол |
|
38) Установите соответствие между названием вещества и продуктом, который преимущественно образуется при нагревании этого вещества с цинком: к каждой позиции, обозначенной буквой, подберите соответствующую
позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
|
А) 1,2-дихлорпропан Б) 1,3-дихлорпропан В) 2,3-дибромбутан Г) 1,3-дибромбутан |
|
39) Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с бромом в отсутствие катализатора.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
|
А) 2-метилбутан Б) циклопентан В) толуол Г) стирол |
|
40) Установите соответствие между названием вещества и углеводородом, который можно получить из этого вещества в одну стадию.
|
НАЗВАНИЕ ВЕЩЕСТВА |
УГЛЕВОДОРОД |
|
|
А) 1-бромпропан Б) 1,2-дихлорэтан В) хлорметан Г) 1,4-дихлорбутан |
|
41) Установите соответствие между названием вещества и углеводородом, который можно получить из этого вещества в одну стадию.
|
НАЗВАНИЕ ВЕЩЕСТВА |
УГЛЕВОДОРОД |
|
|
А) бензоат калия Б) бутанол-1 В) хлорэтан Г) 1,3-дихлорбутан |
|
42) Установите соответствие между реагентами и продуктами, которые преимущественно образуются при их взаимодействии.
|
РЕАГЕНТЫ |
ПРОДУКТЫ РЕАКЦИИ |
|
|
|
|
43) Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с избытком хлороводорода. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
|
А) этилен Б) ацетилен В) пропен Г) 3-метилбутин-1 |
|
44) Установите соответствие между названием вещества и органическим продуктом, который образуется при взаимодействии этого вещества с горячим подкисленным раствором перманганата калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
|
А) 4–метилпентин–1 Б) циклогексен В) циклогексадиен–1,3 Г) 1,4–диметилбензол |
|
45) Установите соответствие между названием вещества и органическим продуктом, который образуется при взаимодействии этого вещества с горячим подкисленным раствором перманганата калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
|
А) циклопентен Б) 3–метилстирол В) гексадиен–1,5 Г) 4,4–диметилпентен–1 |
|
46) Установите соответствие между схемой реакции и веществом, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
СХЕМА РЕАКЦИИ |
ВЕЩЕСТВО Х |
|||||||
|
А) Б) В) Г) 47) Установите соответствие между названием углеводорода и продуктом, который преимущественно образуется при его взаимодействии с азотной кислотой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
1) пропин 2) бутин–2 3) бутен–1 4) бутен–2 5) пропен 6) бутан |
48) Установите соответствие между исходным веществом, которое реагируют с бромоводородом и продуктом, который преимущественно образуется в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ИСХОДНОЕ ВЕЩЕСТВО ПРОДУКТ
А) 2-фенилпропен 1) 2-бром-2-фенилпропан
Б) метилциклопропан 2) 1-бром-2-фенилпропан
В) стирол 3) 2-бромбутан
Г) пропилен 4) 1,3-дибромбутан
5) 1-бром-1-фенилэтан
6) 1-фенил-2-бромэтан
7) 1-бромпропан

49) Установите соответствие между дигалогеналканом и продуктом его взаимодействия со спиртовым раствором щелочи: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ДИГАЛОГЕНАЛКАН ПРОДУКТ
А) 1,2-дихлорэтан 1) пропилен
Б) 1,2-дихлорпропан 2) бутин-1
В) 2,3-дибромбутан 3) бутин-2
Г) 2,2-дихлорпропан 4) ацетилен
5) пропин
6) 2-метилпропен
7) циклопропан
15 задание. Азотсодержащие органические вещества. Углеводы, жиры.
Из предложенного перечня выберите два вещества, с каждым из которых взаимодействует диметиламин.
1) C2H4;
2) HCl;
3) CH3Cl;
4) NH4Cl;
5) Cu(OH)2;
2) Из предложенного перечня выберите два вещества, которые не взаимодействуют с веществом, формула которого NH2CH2CH(CH3)COOH.
1) азотная кислота;
2) аминоуксусная кислота;
3) толуол;
4) этан;
5) гидроксид калия;
3) Из предложенного перечня выберите два вещества, с каждым из которых реагирует аминоуксусная кислота.
1) хлорид натрия;
2) гидроксид натрия;
3) азотная кислота;
4) метан;
5) бензол;
4) Из предложенного перечня выберите два вещества, с каждым из которых реагирует глицин.
1) H2SO4;
2) CaSO4;
3) NH2-CH(CH3)-COOH;
4) CH3COOCH2CH3;
5) CO2;
5)Из предложенного перечня выберите два вещества, которые реагируют как с метиламином, так и с анилином.
1) Br2 (водн.);
2) HBr;
3) NaOH;
4) H2;
5) O2;
6) Из предложенного перечня выберите два вещества, с которыми не взаимодействует фенилаланин.
1) азотная кислота;
2) диэтиловый эфир;
З) хлорид натрия;
4) метанол;
5) уксусная кислота;
7)Из предложенного перечня выберите два вещества, с которыми не взаимодействует диметиламин.
1) хлороводород;
2) гидроксид кальция;
З) уксусная кислота;
4) хлорметан;
5) оксид меди (II);
8)Из предложенного перечня выберите два вещества, каждое из которых образует соль при взаимодействии с пропиламином.
1) вода;
2) соляная кислота;
З) метанол;
4) гидроксид калия;
5) уксусная кислота;
9)Из предложенного перечня выберите два вещества, с которыми реагирует анилин.
1) бромная вода;
2) гидроксид калия;
З) хлорид натрия;
4) соляная кислота;
5) гидроксид меди (II);
10)Этиламин можно получить при взаимодействии
1) C2H6 и HONO2;
2) C2H4 и NH3;
З) C2H5OH и N2;
4) [C2H5NH3]Cl и NaOH;
5) C2H5NO2 и H2.
11)Из предложенного перечня выберите два вещества, с которыми может взаимодействовать метиламин.
1) иодоводород;
2) бензол;
3) гидроксид калия;
4) хлорэтан;
5) анилин;
12)Из предложенного перечня выберите два вещества, с которыми реагирует глюкоза.
1) этен;
2) этан;
3) азотная кислота;
4) раствор перманганата калия;
5) вода;
13)Из предложенного перечня выберите два вещества, с которыми реагирует сахароза.
1) [Ag(NH3)2]OH (р—р);
2) N2;
3) Cu(OH)2;
4) H2O (H+);
5) Cu;
14)Из предложенного перечня выберите два вещества, с которыми реагирует крахмал.
1)I2;
2)N2;
3)C2H6;
4)H2O;
5)NaСl;
15)Из предложенного перечня выберите два вещества, с которыми реагирует метиламин.
1) CH3COOH;
2)C6H6;
3)C2H6;
4)NaCl;
5)C2H5Сl;
16)Из предложенного перечня выберите два вещества, с которыми реагирует аланин.
1)HNO3;
2) C6H6;
3) C2H6;
4) NaCl;
5)C2H5OH;
17) Из предложенного перечня выберите два вещества, с которыми реагирует метиламин.
1) пропан;
2) хлорметан;
3) водород;
4) гидроксид натрия;
5) соляная кислота;
19)Из предложенного перечня выберите два вещества, при взаимодействии которых с метиламином образуется соль.
1) бромэтан;
2) кислород;
3) бромоводородная кислота;
4) вода;
5) азотистая кислота;
20)Из предложенного перечня выберите два вещества, которые образуются при взаимодействии хлорметана с избытком аммиака.
1) CH3NH2;
2) CH3NH3Cl;
3) HCl;
4) NH4Cl;
5) N2;
21)Из предложенного перечня выберите два вещества, которые взаимодействуют с соляной кислотой.
1) анилин;
2) глицин;
3) фенол;
4) толуол;
5) нитробензол;
22)Из предложенного перечня выберите два вещества, которые подвергаются гидролизу.
1) сахароза;
2) глюкоза;
3) целлюлоза;
4) рибоза;
5) фруктоза;
23)Из предложенного перечня выберите два вещества, которые реагируют как с глюкозой, так и с сахарозой.
1) гидроксид меди(II);
2) кислород;
3) аммиачный раствор оксида серебра(I);
4) вода;
5) этан;
24)Из предложенного перечня выберите два вещества, которые не подвергаются гидролизу.
1) аминоуксусная кислота;
2) дипептид цистеина;
3) метиловый эфир аланина;
4) целлюлоза;
5) аминопропионовая кислота;
25)Из предложенного перечня выберите два вещества, которые могут образоваться при щелочном гидролизе белка.
1) NH2CH2COONa;
2) C6H5NH2;
3) CH3CH2OH;
4) CH3CH(NH2)COONa;
5) C6H5ONa;
26)Из предложенного перечня выберите два вещества, с которыми реагирует аланин.
1) гидроксид калия;
2) метанол;
3) сульфат натрия;
4) бензол;
5) медь;
27)Из предложенного перечня выберите два вещества, которые образуются при гидролизе трипальмитата избытком раствора гидроксида калия.
1) C3H8O3
2) C17H33COOH
3) C15H31COOK
4) C17H31COOK
5) C15H31COOH
28)Из предложенного перечня выберите два вещества, с помощью которых НЕЛЬЗЯ различить водные растворы сахарозы и глюкозы.
1) гидроксид натрия
2) гидроксид меди (II)
3) аммиачный раствор оксида серебра (I)
4) бромная вода
5) хлорид натрия
29)Из предложенного перечня выберите два типа реакции, которые характерны как для глюкозы, так и для сахарозы.
1) этерификация
2) горение
3) омыление
4) гидролиз
5) гидрирование
30)Из предложенного перечня выберите два наиболее вероятных продукта гидролиза этилового эфира α-аминопропионовой кислоты в присутствии бромоводородной кислоты.
1) CH3CH(NH2)COOH
2) CH2(NH2)CH2COOH
3) [CH3CH(NH3)COOH]Br
4) C2H5Br
5) C2H5OH
17 задание . Химические свойства спиртов, карбоновых кислот, альдегидов и кетонов.
1.Установите соответствие между реагирующими веществами и продуктом, который преимущественно образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
|
А) фенол и хлор |
1) п-хлорфенол |
2. Установите соответствие между спиртом и исходным веществом, использованным для его получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
СПИРТ |
ИСХОДНОЕ ВЕЩЕСТВО |
|
А) глицерин |
1) CH2=CH–CH3 |
3. Установите соответствие между исходными веществами и продуктом, который преимущественно образуется при их прокаливании: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ИСХОДНЫЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
А) CH3CH2COOК и КOH |
1) пропан |
4. Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии этого вещества с водой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
А) 1-бромпропан |
1) ацетальдегид |
5. Установите соответствие между схемой реакции и веществом X, которое принимает в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
СХЕМА РЕАКЦИИ |
ВЕЩЕСТВО X |
|
А) X+H2O(H+) → пропанол-2 |
1) ацетон |
6. Установите соответствие между формулой вещества и продуктом, который может образоваться при окислении этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ФОРМУЛА ВЕЩЕСТВА |
ПРОДУКТ ОКИСЛЕНИЯ |
|
А) CH3OH |
1) пропанон |
7. Установите соответствие между названием вещества и продуктом(-ами), который(-ые) преимущественно образуется(-ются) при взаимодействии этого вещества с бромом: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ(-Ы) РЕАКЦИИ |
|
А) бензойная кислота |
1) |
8. Установите соответствие между названием спирта и продуктом, который преимущественно образуется при нагревании этого спирта в присутствии концентрированной серной кислоты: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ СПИРТА И УСЛОВИЯ РЕАКЦИИ |
ПРОДУКТ РЕАКЦИИ |
|
А) бутанол-1 (t < 140 °С) |
1) бутадиен-1,3 |
9. Установите соответствие между названием вещества и продуктом, который преимущественно образуется при взаимодействии с водой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
А) 1-хлорпропан |
1) ацетальдегид |
10. Установите соответствие между схемой реакции и веществом X, принимающим участие в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
СХЕМА РЕАКЦИИ |
ВЕЩЕСТВО Х |
|
А) X + HCl → 3-хлорпропановая кислота |
1) ацетальдегид |
11. Установите соответствие между названием соли и веществами, при взаимодействии которых эта соль образуется: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ СОЛИ |
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
|
А) ацетат натрия |
1) уксусная кислота и формиат натрия |
12. Установите соответствие между исходными веществами и продуктом, который преимущественно образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ИСХОДНЫЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
А) карболовая кислота и бромная вода |
1) п-бромфенол |
13. Установите соответствие между веществом, взаимодействующим с гидроксидом меди(II), и преимущественно образующимся продуктом реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ВЕЩЕСТВО |
ПРОДУКТ РЕАКЦИИ |
|
А) этанол |
1) уксусная кислота |
14. Установите соответствие между веществом, которое вступает во взаимодействие с пропионовой кислотой, и одним из продуктов этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ВЕЩЕСТВО |
ПРОДУКТ РЕАКЦИИ |
|
А) Cu(OH)2 |
1) пропилен |
15. Установите соответствие между реагирующими веществами и преимущественно образующимся(-имися) продуктом(-ами) реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРОДУКТ(-Ы) РЕАКЦИИ |
|
А) фенол и гидроксид натрия |
1) фенилацетат |
16. Установите соответствие между исходными веществами и продуктом, который преимущественно образуется при их прокаливании: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ИСХОДНЫЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
А) CH3CH2COONa и NaOH |
1) пропан |
17. Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который преимущественно образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.РЕАГИРУЮЩИЕ ВЕЩЕСТВА ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
A) уксусная кислота и сульфит натрия 1) ацетат натрия
Б) муравьиная кислота и оксид натрия 2) этилат натрия
B) этаналь и водород 3) этанол
Г) этанол и натрий 4) формиат натрия
5) уксусная кислота
6) углекислый газ
18. Установите соответствие между схемой превращений веществ и названием реакции, которая лежит в основе этой схемы: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА ПРЕВРАЩЕНИЯ НАЗВАНИЕ РЕАКЦИИ
A) этанол → этан ал ь 1) дегидратация
Б) глюкоза → этанол 2) этерификация
B) метанол → диметиловый эфир 3) гидролиз
Г) метилацетат → метанол 4) брожение
5) дегидрирование
6) поликонденсация
19. Установите соответствие между реагирующими веществами и органическим веществом — продуктом этой реакции: к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА ПРОДУКТ РЕАКЦИИ
A) СН3СООН и К 1) метилформиат
Б) СН3СООН и NH3 2) ацетат аммония
B) СН3СООН и СН3OH 3) ацетат калия
Г) СН3СООН и К2СO3 4) метилацетат
5) этилат калия
6) аминоуксусная кислота
20. Установите соответствие между схемой реакции и органическим веществом, которое является продуктом реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ ПРОДУКТ РЕАКЦИИ
А) ацеток –H2, Ni→ 1) пропанол–1
Б) метаналь –H2, Ni→ 2) пропанол–2
В) этанол –Cu, t °→ 3) муравьиная кислота
Г) этаналь –KMnO4, H2SO4, t °→ 4) уксусная кислота
5) этаналь
6) метанол
21. Установите соответствие между схемой химической реакции и органическим продуктом, который в ней образуется: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ ПРОДУКТ РЕАКЦИИ
A) СН3СН2ОН –H2SO4, t ° → 1) СН3С(O)OСН3
Б) СН3СН2ОН –Cu, t ° → 2) СН3СН2С(O)СН2СН3
B) СН3СООН + СН3ОН –H+, t ° → 3) СН3С(O)Н
Г) CH3COONa + C2H5CI → 4) СН3СН(ОН)ОСН2СН3
5) СН3СН2ОСН2СН3
6 ) СН3С(O)OСН2СН3
22. Установите соответствие между веществом и углеродсодержащим продуктом реакции, который преимущественно образуется при взаимодействии этого вещества с оксидом меди(II): к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО ПРОДУКТ РЕАКЦИИ
A) уксусная кислота 1) ацетон
Б) этанол 2) ацетальдегид
B) метанол 3) формальдегид
Г) пропанол–2 4) пропаналь
5) формиат меди(II)
6) ацетат меди(II)
23. Установите соответствие между веществом и углеродсодержащим продуктом реакции, который преимущественно образуется при взаимодействии этого вещества с натрием: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО ПРОДУКТ РЕАКЦИИ
A) уксусная кислота 1) этилат натрия
Б) этанол 2) этен
B) муравьиная кислота 3) бутан
Г) хлорэтан 4) этаналь
5) формиат натрия
6) ацетат натрия
24. Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
|
А) уксусная кислота и сульфид натрия |
1) пропионат натрия |
25. Установите соответствие между веществом и углеродсодержащим продуктом реакции, который преимущественно образуется при взаимодействии этого вещества с гидроксидом натрия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
|
А) муравьиная кислота |
1) этилат натрия |
26. Установите соответствие между реагирующими веществами и углеродсодержащим продуктом реакции, который преимущественно образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
|
А) пропаналь и водород |
1) этилат калия |
27. Установите соответствие между веществом и углеродсодержащим продуктом реакции, который преимущественно образуется при взаимодействии этого вещества с оксидом меди (II): к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
|
А) пропанол-1 |
1) формальдегид |
28. Установите соответствие между химической реакцией и углеродсодержащим продуктом, который преимущественно образуется в результате этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАКЦИЯ |
ПРОДУКТ РЕАКЦИИ |
|
А) межмолекулярная дегидратация этанола |
1) пропанол-1 |
29. Установите соответствие между названием вещества и углеродсодержащим продуктом, который образуется при взаимодействии этого вещества с метанолом: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ПРОДУКТ РЕАКЦИИ |
|
А) метанол |
1) метилформиат |
30. Установите соответствие между химической реакцией и углеродсодержащим продуктом, который образуется в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
РЕАКЦИЯ |
ПРОДУКТ РЕАКЦИИ |
|
А) дегидратация этанола |
1) метанол |
Взаимосвязь органических веществ.
1.Задана следующая схема превращений веществ:
Y
C6H6→X → C6H5NH2
Определите, какие из указанных веществ являются веществами X и Y.
C6H5OH
C6H5CH3
C6H5NO2
ZnO + NaOH (р-р)
Fe + HCl (р-р)
2. Задана следующая схема превращений веществ:
CuO Cu(OH)2
C2H5OH → X → Y
Определите, какие из указанных веществ являются веществами X и Y.
этилен
этиленгликоль
этановая кислота
уксусный альдегид
ацетат меди(II)
3. Задана следующая схема превращений веществ:
Cl2,hν NaOH(водн.р−р),t°
2−метилпропан → X → Y
Определите, какие из указанных веществ являются веществами X и Y.
1-хлор-2-метилпропан
2-хлор-2-метилпропан
2-метилпропаналь
2-метилпропанол-1
2-метилпропанол-2
4. Задана следующая схема превращений веществ:
Cu(OH)2,t°
бромэтан → X → уксусный альдегид → Y
Определите, какие из указанных веществ являются веществами X и Y.
этан
уксусная кислота
этанол
ацетилен
бутан
5. Задана следующая схема превращений веществ:
Cl2 H2SO4(конц.),t<140°C
Этан → X→ C2H5OH → Y
Определите, какие из указанных веществ являются веществами X и Y.
C2H5Cl
CH3CHO
C2H4Cl2
C2H5–O–C2H5
C2H4
6. Задана следующая схема превращений веществ:
H2O t°
Al4C3 → X → Y→ этаналь
Определите, какие из указанных веществ являются веществами X и Y.
ацетилен
этанол
метанол
метан
уксусная кислота
7. Задана следующая схема превращений веществ:
CH3Cl,Na,t° KMnO4,H2SO4,t°
C6H5Cl → X → Y
Определите, какие из указанных веществ являются веществами X и Y.
стирол
толуол
бензальдегид
бензойная кислота
фенол
8. Задана следующая схема превращений веществ:
X Y
CH3CHO → CH3COOH → ClCH2COOH
Определите, какие из указанных веществ являются веществами X и Y.
O2
H2
Cl2
HCl
NaCl
9. Задана следующая схема превращений веществ:
этан → X → Y → дивинил
Определите, какие из указанных веществ являются веществами X и Y.
C2H5OH
C2H4Cl2
C2H5Cl
CH3COH
CH3OH
10. Задана следующая схема превращений веществ:
CaC2 → X → Y → уксусная кислота
Определите, какие из указанных веществ являются веществами X и Y.
ацетон
ацетилен
этанол
этилацетат
этаналь
11. Задана следующая схема превращений веществ:
Cl2,hν H2O(H+)
н−C4H10 → X → Y
Определите, какие из указанных веществ являются веществами X и Y.
1-хлорбутан
2-хлорбутан
1,2-дихлорбутан
бутанол-1
бутанол-2
12. Задана следующая схема превращений веществ:
этан → X → Y → бутадиен-1,3
Определите, какие из указанных веществ являются веществами X и Y.
C2H4O2
C2H5Cl
CH3COH
C2H2
C4H10
13. Задана следующая схема превращений веществ:
X
C2H2 → CH3CHO→Y→C2H4
Определите, какие из указанных веществ являются веществами X и Y.
C2H6
CH3COOH
H2O
CH3CH2Cl
C2H5OH
14. Задана следующая схема превращений веществ:
KMnO4,H2SO4,t° HNO3,H2SO4,t°

Определите, какие из указанных веществ являются веществами X и Y.
бензиловый спирт
бензойная кислота
м-нитробензойная кислота
м-сульфобензойная кислота
о-нитробензойная кислота
15. Дана схема химических превращений:
X Y
CH3COOH → CH3COOCH3 → CH3COOK
Определите, какие из указанных веществ являются веществами X и Y.
KOH
HCOOK
H2O
CH3OH
C2H5OH
16. Дана схема химических превращений:
H2O CH3COOH,H+
Этилен → X → Y
Определите, какие из указанных веществ являются веществами X и Y.
этилацетат
этин
этанол
этан
этаналь
17. Дана схема химических превращений:
HCOH O2
C6H5OH → X → Y
Определите, какие из указанных веществ являются веществами X и Y.
формальдегид
фенолформальдегидная смола
нитрофенол
углекислый газ
бензол
18. Дана схема химических превращений:
HCl,t0 Na,t0
Циклопропан → X → Y
Определите, какие из указанных веществ являются веществами X и Y.
пропен
1-хлорпропан
пропен
циклопропан
гексан
19. Дана схема химических превращений:
Ca(OH)2 t0
X → Y → ацетон
Определите, какие из указанных веществ являются веществами X и Y.
CH3COOCH3
HCOOH
(CH3COO)2Ca
C2H5OH
C3H7COH
20. Задана схема превращений веществ:
X –
HBr→ C2H5Br –Y→ C2H4
Определите, какие из указанных веществ являются веществами X и Y.
1) этан
2) вода
3) этен
4) NaOH(водн.)
5) КОН(спирт.)
21. Задана следующая схема превращений веществ:
X → метанол –Y→ метиламин
Определите, какие из указанных веществ являются веществами X и Y.
1) CH3CH2NH2
2) NH3
3) HNO3
4) СНСl3
5) СО
22. Задана следующая схема превращений веществ:
хлорэтан → X → этаналь –Cu(OH)2, t °→ Y
Определите, какие из указанных веществ являются веществами X и Y.
1) этан
2) этандиол–1,2
3) бромэтан
4) этиловый спирт
5) уксусная кислота
23. Задана следующая схема превращений веществ:
CH2Br–CH2Br → X → этан –HONO2→ Y
Определите, какие из указанных веществ являются веществами X и Y.
1) этандиол
2) оксид углерода(IV)
3) ацетилен
4) этиламин
5) нитроэтан
24. Задана следующая схема превращений веществ:
СН3ОН –X→ CH3ONa –Y→ СН3СOOСН3
Определите, какие из указанных веществ являются веществами X и Y.
1) Na2CO3
2) Na
3) CH3COOH
4) CH3COONa
5) СН3С(O)Cl
25. Задана следующая схема превращений веществ:
этаналь –Y→ уксусная кислота → Х –электролиз→ этан
Определите, какие из указанных веществ являются веществами X и Y.
1) 1,2–дихлорэтан
2) гидроксид меди(II)
3) этанол
4) ацетат калия
5) серная кислота (конц.)
26. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами 

1)
2)
3)
4)
5)
27. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами 

1)
2)
3)
4)
5)
28. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами 

1)
2)
3)
4)
5)
29. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами 

1)
2)
3)
4)
5)
30. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами 

1)
2)
3)
4)
5)
31. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами 

1)
2)
3)
4)
5)
32.Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами 

1)
2)
3)
4)
5)
33. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами 

1)
2)
3)
4)
5)
34. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами 

1)
2)
3)
4)
5)
35. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами 

1)
2) 
3) 
4)
5)
36. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1)
2)
3)
4)
5)
37. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1)
2)
3)
4)
5)
38. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1)
2)
3)
4)
5)
39. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1)
2)
3)
4)
5)
40.
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1)
2)
3)
4)
5)
Цепочки превращений.
1)
2)
3)
4)
5)
6)
7)

9)
10)
11)
12)
Задачи на вывод формул.
1)При полном сгорании образца органического вещества А массой 3,3 г было получено 2,64 г углекислого газа, 2,43 г бромоводорода, 90 мг воды и 112 мл (при н.у.) азота. Известно, вещество А может быть получено при бромировании вещества Б, не содержащего атомы углерода в sp3-гибридизации.
На основании данных условия задания:
1) проведите все необходимые вычисления (указывайте единицы измерения физический величин) и установите молекулярную формулу исходного органического вещества;
2) составьте структурную формулу этого вещества, которая отображает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
2) Вещество А содержит 54,13% углерода, 11,28% водорода, 24,06% кислорода и 10,53% азота по массе. Известно, что вещество А содержит один четвертичный атом углерода. При нагревании вещества А с гидроксидом бария образуется органическая соль и выделяется газ, молекула которого содержит один атом углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции, протекающей при нагревании вещества А с гидроксидом бария (используйте структурные формулы органических веществ)
3) Органическое вещество содержит 54,13% углерода, 11,28% водорода, 24,06% кислорода и 10,53% азота. В составе органического вещества имеется четвертичный атом углерода. При нагревании исходное вещество реагирует с гидроксидом бария с образованием органической соли и газа. В состав молекулы газа входит 1 атом углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте возможную структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции исходного органического вещества с гидроксидом бария (используйте структурные формулы органических веществ).
4) Органическое вещество содержит 62,75% углерода, 7,19% водорода, 20,91% кислорода и 9,15% азота. В составе органического вещества есть только один атом углерода в sp3-гибридизации. При нагревании исходное вещество реагирует с гидроксидом кальция с образованием органической соли и газа, содержащего один атом углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте возможную структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции исходного органического вещества с гидроксидом кальция (используйте структурные формулы органических веществ).
5) При взаимодействии двух солей, одна из которых содержит органический катион, получено вещество А и бромид серебра. При сгорании 3,12 г вещества А образуется 5,28 г углекислого газа, 1,44 г воды и 448 мл азота (н.у.).
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте возможную структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А при взаимодействии исходных солей (используйте структурные формулы органических веществ).
6) Вещество А содержит 45,93% углерода, 2,39% водорода и 51,68% серебра по массе и образуется при взаимодействии углеводорода Б с избытком гидроксида диамминсеребра(I).
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества A;
2) составьте возможную структурную формулу вещества Б, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции гидратации углеводорода Б (используйте структурные формулы органических веществ).
7) При сгорании 9 г органического вещества А получили 15,68 л углекислого газа (н.у.) и 5,4 г воды. Известно, что вещество А не содержит атомов углерода в sp3-гибридизации, а при его окислении сернокислым раствором перманганата калия образуется только одно органическое соединение – бензойная кислота.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте возможную структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение окисления вещества А раствором перманганата калия в присутствии серной кислоты (используйте структурные формулы органических веществ).

На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества A;
2) составьте возможную структурную формулу вещества A, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с избытком гидроксида диамминсеребра(I) (используйте структурные формулы органических веществ).
9) При сгорании 13,24 г органического вещества А получили 10,56 г углекислого газа и 9,72 г бромоводорода. Известно, что вещество А образуется при бромировании гидроксильного соединения Б.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества A;
2) составьте возможную структурную формулу вещества A, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение бромирования гидроксильного соединения Б с образованием вещества А (используйте структурные формулы органических веществ).
10) При сгорании 1 г органического вещества А получили 1,12 л углекислого газа (н.у.) и 0,72 г воды. Известно, что вещество А образуется при гидратации углеводорода Б, который вступает в реакцию с гидроксидом диамминсеребра(I) в молярном соотношении 1:2.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества A;
2) составьте возможную структурную формулу вещества A, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение гидратации углеводорода Б с образованием вещества А (используйте структурные формулы органических веществ).
Ответы на тесты.
Тема — Номенклатура и классификация органических соединений.
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
|
А |
3 |
1 |
4 |
3 |
4 |
2 |
1 |
3 |
3 |
1 |
1 |
3 |
3 |
3 |
4 |
3 |
3 |
1 |
3 |
1 |
|
Б |
3 |
3 |
3 |
1 |
1 |
4 |
4 |
1 |
4 |
4 |
2 |
2 |
4 |
2 |
1 |
6 |
4 |
4 |
4 |
3 |
|
В |
3 |
2 |
2 |
4 |
3 |
1 |
3 |
1 |
5 |
3 |
4 |
1 |
1 |
3 |
2 |
5 |
1 |
3 |
2 |
2 |
Тема- Теория строения органических соединений. Изомерия.
|
1 |
2,4 |
20 |
1,3 |
|
2 |
1,5 |
21 |
3,4 |
|
3 |
2,4 |
22 |
3,5 |
|
4 |
1,4 |
23 |
1,4 |
|
5 |
2,5 |
24 |
1,3 |
|
6 |
2,5 |
25 |
1,3 |
|
7 |
1,2 |
26 |
2,4 |
|
8 |
3,5 |
27 |
4,5 |
|
9 |
1,5 |
28 |
1,5 |
|
10 |
2,4 |
29 |
2,4 |
|
11 |
1,4 |
30 |
2,5 |
|
12 |
1,3 |
31 |
4,5 |
|
13 |
1,5 |
32 |
1,3 |
|
14 |
1,2 |
33 |
2,3 |
|
15 |
1,5 |
34 |
1,4 |
|
16 |
2,4 |
35 |
2,5 |
|
17 |
2,5 |
36 |
1,3 |
|
18 |
1,2 |
37 |
3,5 |
|
19 |
1,3 |
38 |
1,3 |
Тема. Углеводороды. Способы получения и химические свойства.
|
1 |
3,5 |
20 |
1,3 |
|
2 |
2,3 |
21 |
3,5 |
|
3 |
1,4 |
22 |
3,5 |
|
4 |
1,3 |
23 |
1,2 |
|
5 |
1,4 |
24 |
2,3 |
|
6 |
1,3 |
25 |
1,4 |
|
7 |
1,4 |
26 |
1,5 |
|
8 |
2,4 |
27 |
3,5 |
|
9 |
1,5 |
28 |
2,4 |
|
10 |
4,5 |
29 |
1,4 |
|
11 |
3,4 |
30 |
2,3 |
|
12 |
1,3 |
31 |
2,3 |
|
13 |
1,4 |
32 |
3,5 |
|
14 |
2,5 |
33 |
2,4 |
|
15 |
3,4 |
34 |
2,5 |
|
16 |
2,4 |
35 |
3,5 |
|
17 |
1,4 |
36 |
3,5 |
|
18 |
2,5 |
37 |
2,4 |
|
19 |
3,5 |
38 |
2,5 |
Тема: Химические свойства углеводородов.
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
|
|
А |
3 |
4 |
5 |
2 |
5 |
4 |
3 |
5 |
1 |
3 |
3 |
1 |
2 |
5 |
1 |
4 |
3 |
5 |
6 |
2 |
5 |
5 |
2 |
3 |
|
Б |
1 |
4 |
4 |
4 |
2 |
2 |
5 |
4 |
4 |
1 |
2 |
3 |
1 |
1 |
5 |
2 |
2 |
2 |
2 |
1 |
2 |
2 |
1 |
6 |
|
В |
2 |
1 |
1 |
4 |
3 |
5 |
2 |
2 |
2 |
2 |
5 |
2 |
1 |
2 |
6 |
1 |
4 |
3 |
4 |
4 |
4 |
3 |
6 |
1 |
|
Г |
5 |
1 |
2 |
4 |
6 |
1 |
6 |
2 |
5 |
5 |
1 |
6 |
2 |
3 |
2 |
1 |
5 |
6 |
1 |
6 |
6 |
6 |
3 |
5 |
|
25 |
26 |
27 |
28 |
29 |
30 |
31 |
32 |
33 |
34 |
35 |
36 |
37 |
38 |
39 |
40 |
41 |
42 |
43 |
44 |
45 |
46 |
47 |
48 |
49 |
|
|
А |
5 |
4 |
2 |
5 |
3 |
2 |
3 |
6 |
1 |
1 |
3 |
2 |
2 |
2 |
6 |
2 |
5 |
5 |
6 |
3 |
4 |
1 |
3 |
1 |
4 |
|
Б |
3 |
5 |
6 |
3 |
4 |
1 |
2 |
4 |
6 |
1 |
4 |
1 |
3 |
3 |
1 |
4 |
2 |
3 |
4 |
5 |
2 |
5 |
4 |
3 |
5 |
|
В |
6 |
4 |
3 |
4 |
6 |
4 |
1 |
5 |
3 |
4 |
1 |
4 |
5 |
6 |
2 |
6 |
6 |
2 |
3 |
4 |
3 |
3 |
5 |
5 |
3 |
|
Г |
4 |
7 |
4 |
2 |
2 |
4 |
6 |
2 |
4 |
6 |
5 |
6 |
5 |
5 |
4 |
3 |
4 |
4 |
2 |
2 |
5 |
5 |
2 |
8 |
5 |
Тема: Химические свойства азотсодержащих соединений.
|
1 |
2,3 |
16 |
1,5 |
|
2 |
3,4 |
17 |
2,5 |
|
3 |
2,3 |
19 |
1,3 |
|
4 |
1,3 |
20 |
1,4 |
|
5 |
2,5 |
21 |
1,2 |
|
6 |
2,3 |
22 |
1,3 |
|
7 |
2,5 |
23 |
1,2 |
|
8 |
2,5 |
24 |
1,5 |
|
9 |
1,4 |
25 |
1,4 |
|
10 |
4,5 |
26 |
1,2 |
|
11 |
1,4 |
27 |
1,3 |
|
12 |
3,4 |
28 |
1,2 |
|
13 |
3,4 |
29 |
1,2 |
|
14 |
1,4 |
30 |
3,5 |
|
15 |
1,5 |
Тема. Химические свойства спиртов, карбоновых кислот, альдегидов и кетонов.
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
|
|
А |
1 |
1 |
4 |
3 |
3 |
5 |
6 |
4 |
3 |
5 |
6 |
2 |
3 |
2 |
6 |
4 |
1 |
5 |
3 |
2 |
2 |
6 |
6 |
|
Б |
3 |
1 |
3 |
5 |
2 |
1 |
4 |
5 |
5 |
4 |
5 |
3 |
1 |
3 |
4 |
3 |
4 |
4 |
2 |
6 |
3 |
2 |
1 |
|
В |
5 |
3 |
4 |
1 |
1 |
2 |
5 |
3 |
1 |
1 |
4 |
4 |
3 |
5 |
1 |
4 |
3 |
1 |
4 |
5 |
1 |
3 |
5 |
|
Г |
6 |
2 |
5 |
2 |
4 |
3 |
2 |
2 |
2 |
3 |
2 |
4 |
4 |
2 |
5 |
5 |
2 |
3 |
3 |
4 |
6 |
1 |
3 |
|
24 |
25 |
26 |
27 |
28 |
29 |
30 |
|
|
А |
5 |
5 |
5 |
5 |
4 |
5 |
2 |
|
Б |
4 |
1 |
6 |
3 |
6 |
1 |
1 |
|
В |
3 |
2 |
4 |
4 |
3 |
5 |
3 |
|
Г |
2 |
3 |
2 |
1 |
1 |
3 |
5 |
Тест. Взаимосвязь органических веществ.
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
||
|
Х |
3 |
4 |
2 |
3 |
1 |
4 |
2 |
1 |
3 |
2 |
2 |
2 |
3 |
2 |
4 |
3 |
2 |
2 |
1 |
3 |
|
|
Y |
5 |
3 |
5 |
2 |
4 |
1 |
4 |
3 |
1 |
5 |
5 |
5 |
5 |
3 |
1 |
1 |
4 |
5 |
3 |
5 |
|
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
30 |
31 |
32 |
33 |
34 |
35 |
36 |
37 |
38 |
39 |
40 |
||
|
Х |
5 |
4 |
3 |
2 |
2 |
2 |
1 |
1 |
2 |
5 |
5 |
1 |
3 |
1 |
2 |
2 |
5 |
2 |
3 |
4 |
|
|
Y |
2 |
5 |
5 |
5 |
4 |
5 |
3 |
5 |
4 |
2 |
4 |
2 |
1 |
4 |
1 |
3 |
2 |
1 |
1 |
1 |
Цепочки превращений:
1)
2)
3)
4)
5)
6)
7)

9)
10)
11)
12)
Задачи на вывод формулы
1)Молекулярная формула: C6H4NBr3
Структурная формула:
Реакция получения вещества А из вещества Б:
2) Молекулярная формула вещества: C6H15NO2
Структурная формула вещества А:
Реакция вещества А с гидроксидом бария:
3) 1. Молекулярная формула — С6H15O2N
2-3. Структурная формула и уравнение:

4) 1. Молекулярная формула — С8H11O2N
2-3. Структурная формула и уравнение:

5)
1. Молекулярная формула — С6H8O3N2
2-3. Структурная формула и уравнение:

6) 1. Молекулярная формула — С8H5Ag
2-3. Структурная формула и уравнение:

7) Молекулярная формула — С14H12
2-3. Структурная формула и уравнение:


2-3. Структурная формула и уравнение:

9) 1. Молекулярная формула — С6H3OBr3
2-3. Структурная формула и уравнение:

10) 1. Молекулярная формула — С5H8O2
2-3. Структурная формула и уравнение:

Полный курс подготовки к ЕГЭ по химии-2023. Здесь приведена теория по каждому заданию в соответствии с спецификацией и кодификатором ЕГЭ по химии. Учебные материалы и теория, необходимые для подготовки к ЕГЭ по химии.
Вы можете поддержать работу сайта, разработку новых материалов и тестов. Донаты принимаются через форму:
Обратите внимание! Форма выше — это не оплата курса по химии, это форма для сбора донатов на работу сайта)
Кодификатор ЕГЭ по химии-2022
| 1 | ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ | |
| |
1.1. | Современные представления о строении атома |
| 1.1.1. | Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атомов и ионов. Основное и возбужденное состояния атомов
Тренировочные тесты в формате ЕГЭ по теме «Строение атома» (задание 1 ЕГЭ по химии) ( с ответами) |
|
| 1.2 | Периодический закон и Периодическая система химических элементов Д.И. Менделеева |
|
| 1.2.1. | Закономерности изменения свойств элементов и их соединений по периодам и группам
Тренировочные тесты в формате ЕГЭ по теме «Периодический закон» (задание 2 ЕГЭ по химии) ( с ответами) |
|
| 1.2.2. | Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. | |
| 1.2.3. | Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в Периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов | |
| 1.2.4. | Общая характеристика неметаллов IVА–VIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов | |
| 1.3. | Химическая связь и строение вещества |
|
| 1.3.1 | Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь
Тренировочные тесты в формате ЕГЭ по теме «Химические связи» (задание 4 ЕГЭ по химии) ( с ответами) |
|
| 1.3.2. | Электроотрицательность. Степень окисления и валентность химических элементов
Тренировочные тесты в формате ЕГЭ по теме «Степень окисления и валентность» (задание 3 ЕГЭ по химии) ( с ответами) |
|
| 1.3.3. | Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения | |
| 1.4. | Химическая реакция | |
| 1.4.1. | Классификация химических реакций в неорганической и органической химии
Тренировочные тесты в формате ЕГЭ по теме «Классификация реакций» ( с ответами) |
|
| 1.4.2. | Тепловой эффект химической реакции. Термохимические уравнения | |
| 1.4.3. | Скорость реакции, ее зависимость от различных факторов
Тренировочные тесты в формате ЕГЭ по теме «Скорость реакции» ( с ответами) |
|
| 1.4.4. | Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов
Тренировочные тесты в формате ЕГЭ по теме «Химическое равновесие реакции» ( с ответами) |
|
| 1.4.5. |
Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты | |
| 1.4.6. | Реакции ионного обмена | |
| 1.4.7. |
Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная
Тренировочные тесты в формате ЕГЭ по теме «Гидролиз» (с ответами) |
|
| 1.4.8. |
Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее
Тренировочные тесты в формате ЕГЭ по теме «Окислительно-восстановительные реакции» (задание 19 ЕГЭ по химии) ( с ответами) |
|
| 1.4.9. |
Электролиз расплавов и растворов (солей, щелочей, кислот)
Тренировочные тесты в формате ЕГЭ по теме «Электролиз» (задание 20 ЕГЭ по химии) ( с ответами) |
|
| 1.4.10. |
Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии | |
| 2 | НЕОРГАНИЧЕСКАЯ ХИМИЯ | |
| 2.1. | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная)
Тренировочные тесты в формате ЕГЭ по теме «Классификация неорганических веществ» (задание 5 ЕГЭ по химии) ( с ответами) |
|
| 2.2. | Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, магния, алюминия; переходных металлов (меди, цинка, хрома, железа) | |
| 2.3. | Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния | |
| 2.4. | Характерные химические свойства оксидов: основных, амфотерных, кислотных | |
| 2.5. | Характерные химические свойства оснований и амфотерных гидроксидов | |
| 2.6. | Характерные химические свойства кислот | |
| 2.7. | Характерные химические свойства солей: средних, кислых, основных; комплексных (на примере соединений алюминия и цинка) | |
| 2.8. | Взаимосвязь различных классов неорганических веществ | |
| 3. | ОРГАНИЧЕСКАЯ ХИМИЯ | |
| 3.1. | Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах
Тренировочные тесты в формате ЕГЭ по теме «Теория строения орг. соединений» ( с ответами) |
|
| 3.2. | Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа | |
| 3.3. | Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная)
Тренировочные тесты в формате ЕГЭ по теме «Классификация орг. соединений» ( с ответами) |
|
| 3.4. | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола) | |
| 3.5. | Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола. | |
| 3.6. | Характерные химические свойства альдегидов, карбоновых кислот, сложных эфиров | |
| 3.7. | Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Важнейшие способы получения аминов и аминокислот
Тренировочные тесты в формате ЕГЭ по теме «Свойства азотсодержащих соединений» ( с ответами) |
|
| 3.8. | Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды, полисахариды) | |
| 3.9. | Взаимосвязь органических соединений | |
| 4. | МЕТОДЫ ПОЗНАНИЯ В ХИМИИ. ХИМИЯ И ЖИЗНЬ | |
| 4.1. | Экспериментальные основы химии | |
| 4.1.1. | Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии | |
| 4.1.2. | Научные методы исследования химических веществ и превращений. Методы разделения смесей и очистки веществ | |
| 4.1.3. | Определение характера среды водных растворов веществ. Индикаторы | |
| 4.1.4. | Качественные реакции на неорганические вещества и ионы | |
| 4.1.5. | Качественные реакции органических соединений | |
| 4.1.6. | Основные способы получения (в лаборатории) конкретных веществ, относящихся к изученным классам неорганических соединений | |
| 4.1.7. | Основные способы получения углеводородов (в лаборатории): алканов, алкенов, алкинов, циклоалканов, алкадиенов, аренов | |
| 4.1.8. | Основные способы получения органических кислородсодержащие соединений (в лаборатории): спиртов, альдегидов и кетонов, карбоновых кислот | |
| 4.2.1. | Понятие о металлургии: общие способы получения металлов | |
| 4.2.2. | Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия | |
| 4.2.3. | Природные источники углеводородов, их переработка | |
| 4.2.4. | Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки | |
| 4.3. | Расчеты по химическим формулам и уравнениям реакций | |
| 4.3.1. | Расчеты с использованием понятия «массовая доля вещества в растворе» | |
| 4.3.2. | Расчеты объемных отношений газов при химических реакциях | |
| 4.3.3. | Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ | |
| 4.3.4. | Расчеты теплового эффекта реакции | |
| 4.3.5. | Расчеты массы (объема, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси) | |
| 4.3.6. | Расчеты массы (объема, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества | |
| 4.3.7. | Установление молекулярной и структурной формулы вещества | |
| 4.3.8. | Расчеты массовой или объемной доли выхода продукта реакции от теоретически возможного | |
| 4.3.9. | Расчеты массовой доли (массы) химического соединения в смеси |
1.1.1. Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атомов и ионов. Основное и возбужденное состояния атомов
Тренировочные тесты в формате ЕГЭ по теме «Строение атома» (задание 1 ЕГЭ по химии) ( с ответами)
1.2. Периодический закон и Периодическая система химических элементов Д.И. Менделеева
Тренировочные тесты в формате ЕГЭ по теме «Периодический закон» (задание 2 ЕГЭ по химии) ( с ответами)
1.2.1. Закономерности изменения свойств элементов и их соединений по периодам и группам
1.2.2. Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов.
1.2.3. Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в Периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов
1.2.4. Общая характеристика неметаллов IVА–VIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов
1.3. Химическая связь и строение вещества
1.3.1. Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь
Тренировочные тесты в формате ЕГЭ по теме «Химические связи» (задание 4 ЕГЭ по химии) ( с ответами)
1.3.2. Электроотрицательность. Степень окисления и валентность химических элементов
Тренировочные тесты в формате ЕГЭ по теме «Степень окисления и валентность» (задание 3 ЕГЭ по химии) ( с ответами)
1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения
1.4. Химическая реакция
1.4.1. Классификация химических реакций в неорганической и органической химии
1.4.2. Тепловой эффект химической реакции. Термохимические уравнения
1.4.3. Скорость реакции, ее зависимость от различных факторов
Тренировочные тесты в формате ЕГЭ по теме «Скорость реакции» (задание 20 ЕГЭ по химии) ( с ответами)
1.4.4. Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов
Тренировочные тесты в формате ЕГЭ по теме «Химическое равновесие реакции» (задание 24 ЕГЭ по химии) ( с ответами)
1.4.5. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты
1.4.6. Реакции ионного обмена
1.4.7. Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная
Тренировочные тесты в формате ЕГЭ по теме «Гидролиз» (задание 23 ЕГЭ по химии) ( с ответами)
1.4.8. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее
Тренировочные тесты в формате ЕГЭ по теме «Окислительно-восстановительные реакции» (задание 21 ЕГЭ по химии) ( с ответами)
1.4.9. Электролиз расплавов и растворов (солей, щелочей, кислот)
Тренировочные тесты в формате ЕГЭ по теме «Электролиз» (задание 22 ЕГЭ по химии) ( с ответами)
1.4.10. Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии
2. НЕОРГАНИЧЕСКАЯ ХИМИЯ
2.1. Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная)
Тренировочные тесты в формате ЕГЭ по теме «Классификация неорганических веществ» (задание 5 ЕГЭ по химии) ( с ответами)
2.2. Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, магния, алюминия; переходных металлов (меди, цинка, хрома, железа)
2.3. Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния
2.4. Характерные химические свойства оксидов: основных, амфотерных, кислотных
2.5. Характерные химические свойства оснований и амфотерных гидроксидов
2.6. Характерные химические свойства кислот
2.7. Характерные химические свойства солей: средних, кислых, основных; комплексных (на примере соединений алюминия и цинка)
2.8. Взаимосвязь различных классов неорганических веществ
3. ОРГАНИЧЕСКАЯ ХИМИЯ
3.1. Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах
3.2. Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа
3.3. Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная)
3.4. Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола)
3.5. Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола.
3.6. Характерные химические свойства альдегидов, карбоновых кислот, сложных эфиров
3.7. Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Важнейшие способы получения аминов и аминокислот
3.8. Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды, полисахариды)
3.9. Взаимосвязь органических соединений
4. МЕТОДЫ ПОЗНАНИЯ В ХИМИИ. ХИМИЯ И ЖИЗНЬ
4.1. Экспериментальные основы химии
4.1.1. Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии
4.1.2. Научные методы исследования химических веществ и превращений. Методы разделения смесей и очистки веществ
4.1.3. Определение характера среды водных растворов веществ. Индикаторы
4.1.4. Качественные реакции на неорганические вещества и ионы
4.1.5. Качественные реакции органических соединений
4.1.6. Основные способы получения (в лаборатории) конкретных веществ, относящихся к изученным классам неорганических соединений
4.1.7. Основные способы получения углеводородов (в лаборатории): алканов, алкенов, алкинов, циклоалканов, алкадиенов, аренов
4.1.8. Основные способы получения органических кислородсодержащие соединений (в лаборатории): спиртов, альдегидов и кетонов, карбоновых кислот
4.2.1. Понятие о металлургии: общие способы получения металлов
4.2.2. Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия
4.2.3. Природные источники углеводородов, их переработка
4.2.4. Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки
4.3. Расчеты по химическим формулам и уравнениям реакций
4.3.1. Расчеты с использованием понятия «массовая доля вещества в растворе»
4.3.2. Расчеты объемных отношений газов при химических реакциях
4.3.3. Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ
4.3.4. Расчеты теплового эффекта реакции
4.3.5. Расчеты массы (объема, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси)
4.3.6. Расчеты массы (объема, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества
4.3.7. Установление молекулярной и структурной формулы вещества
4.3.8. Расчеты массовой или объемной доли выхода продукта реакции от теоретически возможного
4.3.9. Расчеты массовой доли (массы) химического соединения в смеси
Курс подготовки к ЕГЭ или ОГЭ (ГИА) по химии:
Общая химия
Часть 1. Строение вещества
1. Строение атома. Электронные формулы атомов
2. Периодический закон
3. Строение молекул. Типы химических связей. Основные характеристики ковалентной связи. Межмолекулярные связи
4. Строение вещества (кристаллические решетки). Основные физические свойства различных кристаллов
5. Степень окисления и валентность химических элементов.
Часть 2. Основы неорганической химии
1. Классификация неорганических веществ
2. Номенклатура неорганических веществ
3. Способы получения оксидов
4. Химические свойства основных оксидов
5. Химические свойства кислотных оксидов
6. Химические свойства амфотерных оксидов
7. Химические свойства и способы получения кислот
8. Химические свойства и способы получения солей
9. Химические свойства и способы получения оснований
10. Взаимосвязь основных классов неорганических веществ
11. Бинарные соединения — гидриды.
12. Реакции разложения в неорганической химии
Часть 3. Физико-химия растворов:
1. Понятие о растворах, растворимость
2. Теория электролитической диссоциации
3. Реакции ионного обмена
4. Гидролиз.
Часть 4. Окислительно-восстановительные реакции
1. Окислительно-восстановительные реакции.
2. Электролиз солей. Электролиз солей карбоновых кислот. Коррозия.
Часть 5. Особенности работы в лаборатории
Часть 6. Химические реакции. Закономерности их протекания
1. Классификация химических реакций.
2. Кинетика (скорость) химических реакций и ее зависимость от разных факторов.
3. Термодинамика химических реакций: химическое равновесие и его смещение.
Органическая химия
1. Теория строения органических веществ. Классификация органических веществ. Гомологи и изомеры. Виды изомерии.
2. Алканы: химические и физические свойства, строение, получение, изомерия.
3. Алкены: химические и физические свойства, строение, получение, изомерия.
4. Алкины: химические и физические свойства, строение, получение, изомерия.
5. Алкадиены: химические и физические свойства, строение, получение, изомерия.
6. Арены: химические и физические свойства, строение, получение, изомерия.
7. Циклоалканы: химические и физические свойства, строение, получение, изомерия.
8. Спирты: химические и физические свойства, строение, изомерия и способы получения. Фенолы: химические свойства, способы получения, строение и изомерия.
9. Альдегиды и кетоны: химические и физические свойства, строение и изомерия, получение.
10. Карбоновые кислоты: химические и физические свойства, строение, номенклатура и изомерия, способы получения.
11. Сложные эфиры: химические и физические свойства, строение, получение, изомерия.
12. Жиры: химические и физические свойства, строение, получение.
13. Углеводы: химические и физические свойства, строение, получение.
14. Амины: химические и физические свойства, строение, получение, изомерия.
15. Аминокислоты: химические и физические свойства, строение, получение, изомерия.
16. Белки: химические и физические свойства, строение и получение.
17. Взаимосвязь разных классов органических веществ.
18. Качественные реакции в органической химии.
Характерные реакции в органической химии:
Реакция Дюма Электролиз солей карбоновых кислот Пиролиз метана Реакция Вагнера
Химия элементов
Часть 1. Химия щелочных металлов и их соединений. Пероксиды щелочных металлов. Гидроксиды щелочных металлов.
Часть 2. Химия щелочноземельных металлов. Оксиды щелочноземельных металлов. Гидроксиды щелочноземельных металлов.
Часть 3. Химия алюминия и его соединений. Оксид алюминия. Гидроксид алюминия. Соли алюминия.
Часть 4. Химия углерода. Оксид углерода (II) и оксид углерода (IV). Угольная кислота и ее соли (карбонаты и гидрокарбонаты).
Часть 5. Химия кремния. Оксид кремния (IV). Кремниевая кислота. Силан. Силикаты.
Часть 6. Химия азота и его соединений. Оксиды азота. Аммиак. Нитриды. Азотная кислота и азотистая кислота. Нитраты.
Часть 7. Химия фосфора и его соединений. Фосфин. Фосфиды металлов. Оксиды фосфора III и V. Фосфорные кислоты и их соли (фосфаты, гидрофосфаты и дигидрофосфаты, пирофосфаты и метафосфаты). Фосфористая кислота.
Часть 8. Химия кислорода и его соединений.
Часть 9. Химия серы и ее соединений. Сероводород и сульфиды. Оксиды серы – сернистый газ и серный ангидрид. Серная кислота и ее свойства. Сернистая кислота. Особенности химии сульфатов и сульфитов.
Часть 10. Химия галогенов и их соединений.
Часть 11. Химия d-элементов: железа, хрома, цинка, меди.
Часть 12. Химия водорода и его соединений.
Задачи: базовый блок
1. Атомно -молекулярное учение
2. Способы выражения концентрации в растворах: массовая доля, растворимость, молярная концентрация.
3. Расчеты по уравнению реакции
4. Задачи на избыток-недостаток
5. Задачи на примеси
6. Задачи на выход
Задачи повышенной сложности
1. Задачи на электролиз
2. Задачи на кристаллогидраты
3. Задачи на пластинки
4. Задачи на порции
5. Неполное разложение
6. Задачи на альтернативные реакции (кислые/средние соли, амфотерность)
7. Задачи на атомистику
8. Задачи на смеси и сплавы
9. Задачи на растворимость
Диагностические и тренировочные работы
Все реальные варианты КИМ ЕГЭ по химии
Тренировочная работа по химии в формате ЕГЭ 26 октября 2017 года
Тренировочная работа по химии для 11 классов 30 ноября 2017 года
Досрочный ЕГЭ по химии 25.03.2019
Видеоопыты
Видеоопыты по общей и неорганической химии
Видеоопыты по органической химии
Спецификация ЕГЭ по химии-2022
Подготовка к ЕГЭ по химии
Как проходит ЕГЭ по химии в 2023 году
На ЕГЭ по химии, как и в случае с большинством других предметов, ученик 11 класса должен будет справиться с 2 частями экзамена:
-
1-я часть: 28 заданий с кратким ответом;
-
2-я часть: 6 заданий с развернутым ответом.
Чтобы решить все 34 задания единого государственного экзамена, у ученика будет 210 минут. За это время нужно будет успеть ответить на вопросы обеих частей, подготовить полное решение для задач 2-й части и перенести ответы в бланк.
Кстати, в отличие от ОГЭ, на ЕГЭ по химии не будет задания-эксперимента. Только обычные химические задания разной сложности. В таблице ниже можно посмотреть, сколько будет легких, средних и сложных вопросов.
| Уровень сложности заданий на ЕГЭ по химии | |
|---|---|
| Базовая | 17 |
| Повышенная | 11 |
| Высокая | 6 |
Если вы хотите больше узнать об особенностях экзамена и подготовки к нему, советуем заглянуть в раздел «Демоверсии, спецификации, кодификаторы» сайта ФИПИ. Там вы найдете всю актуальную информацию о ЕГЭ по химии и методические рекомендации. Все это поможет распланировать подготовку к экзамену так, чтобы сдать его на 100 баллов.
Изменения в ЕГЭ по химии
По сравнению с 2022 годом экзамен по химии немного изменится. Вот список нововведений:
-
Немного поменялось условие задания 23, в котором нужно рассчитать концентрацию веществ. Теперь данные в нем будут записаны текстом, а не в таблице.
-
Задания 33 и 34 поменялись местами.
-
Задания 9, 12 и 16 теперь станут повышенной сложности.
Получай лайфхаки, статьи, видео и чек-листы по обучению на почту
Демоурок по подготовке к экзаменам
Составим ваш личный путь к высоким баллам — учтем сроки, уровень знаний и цель.
Как хорошо сдать ЕГЭ по химии: разбор сложных задач
Как мы узнали из таблицы в предыдущем разделе, экзамен по химии — один из самых сложных. На 34 задания в нем приходится целых 11 повышенной сложности и 6 — высокой. Но если вы хотите поступить в вуз мечты, советуем научиться их решать так, чтобы не упустить ни одного балла. А потому предлагаем начать подготовку прямо сейчас и вместе разобрать несколько таких задач.
Задание 7
Это задание проверяет буквально все ваши знания в области неорганической химии. Здесь нужно знать как химические свойства простых соединений, так и химические свойства сложных соединений. Давайте разберем одно из таких заданий, чтобы понять, как их решать, чтобы сдать ЕГЭ по химии.
Установите соответствие между веществом и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| Вещество | Реагенты |
|---|---|
| А) S | 1) AgNO3, K3PO4, Cl2 |
| Б) SO3 | 2) BaO, NaOH, H2O |
| В) Zn(OH)2 | 3) H2, Cl2, O2 |
| Г) ZnBr2 | 4) HBr, LiOH, CH3COOH (p-p) |
| 5) H3PO4 (p-p), BaCl2, CuO |
Решение:
-
Вариант под буквой А — простое вещество, сера. Как правило, простые вещества взаимодействуют с другими простыми веществами, значительно реже со сложными веществами. Под это описание подходит вариант № 3.
-
Вещество под буквой Б — кислотный оксид. Кислотные оксиды не реагируют с кислотами, поэтому смело вычеркиваем варианты, где присутствует хоть одна кислота. Остаются варианты № 1–3. Реагенты под цифрой 3 тоже можем вычеркнуть, так как кислотный оксид уже в своей максимальной степени окисления и дальше взаимодействовать с кислородом не может. Остаются варианты № 1 и № 2. Оксид серы (VI) может реагировать с основным оксидом с образованием соли, со щелочью с образованием соли и воды, и с водой, при этом образуя кислоту. Выбираем № 2.
-
Амфотерный нерастворимый в воде гидроксид цинка может взаимодействовать только с теми, что способны его растворить. Единственно верный вариант под № 4, где указаны кислоты и щелочь.
-
При взаимодействии соли с другими сложными веществами надо помнить про три признака протекания химической реакции: выпадения осадка, выделение газа и образование малодиссоциирующего вещества — воды. Под это описание подходит вариант под № 1. Но как же хлор? Дело в том, что вышестоящие в группе галогены способны вытеснить нижестоящие из их солей.
Ответ: 3241.
Задание 15
Это задание Единого государственного экзамена проверит ваши знания химических свойств органических соединений. Чтобы справиться с ним, нужно по записанным словами реагирующим веществам составить уравнение реакции и выбрать из перечня один из получившихся продуктов. Давайте рассмотрим на примере, как решать такую задачу.
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| Реагирующие вещества | Продукт взаимодействия |
|---|---|
| А) уксусная кислота и сульфид калия | пропионат калия |
| Б) муравьиная кислота и гидроксид калия | этилат калия |
| В) муравьиный альдегид и гидроксид меди (II) при нагревании | формиат меди (II) |
| Г) этанол и калий | формиат калия |
| ацетат калия | |
| углекислый газ |
Решение:
-
Органические кислоты могут реагировать с солями, если те имеют летучий анион. В результате взаимодействия образуется соль уксусной кислоты и сероводород (летучее соединение). Соль, которая образована в таких условиях, — ацетат калия. Это вещество № 5.
-
Муравьиная кислота проявляет свойства неорганической кислоты и может взаимодействовать с щелочами с образованием соли и воды. Соль муравьиной кислоты — формиат. Правильный ответ № 4.
-
Под буквой В описана качественная реакция на альдегиды с образованием соответствующей кислоты, оксида меди (I) и воды. Исключение — муравьиный альдегид. Он окисляется до углекислого газа, а остальные продукты реакции те же. Соответственно, правильный ответ № 6.
-
Калий как активный металл может замещать протон водорода в гидроксогруппе у спиртов с образованием алкоголята. Правильный ответ: № 2.
Ответ: 5462.
Задание 16
Это задание всё так же проверяет ваши знания по химическим свойствам и, как следствие, умение записывать превращения в рамках органической химии. Однако оно усложняется тем, что теперь вам самим нужно подобрать такой реактив, чтобы произошло уже известное превращение. Давайте попробуем решить один из вариантов такой задачи вместе — это повысит ваши шансы сдать ЕГЭ на 100 баллов.
Задана схема превращений веществ:
Определите, какие из указанных веществ являются веществами х и у:
-
2-бромбутан;
-
этаналь;
-
этен;
-
метилпропан;
-
хлорэтан.
Решение:
Посмотрим, что случилось с известными нам веществами.
-
У спирта исчезла ОН-группа, затем что-то произошло, и углеродная цепочка увеличилась вдвое. Мы помним, что когда цепочка увеличивается вдвое, то, скорее всего, это реакция Вюрца. А в неё вступают только галогеналканы. Ищем нужный нам вариант. Он находится под номером 5. Первое вещество найдено.
-
Бутан подвергают нагреванию с использованием катализатора. Нужно помнить, что в таких условиях проводится изомеризация алканов. Из бутана получается метилпропан. Ответ: № 4.
Ответ: 54.
Задание 26
Теперь разберем задачи, которые заканчивают тестовую часть ЕГЭ по химии. Рассмотрим условие одной из них на нахождение массы соли, которую необходимо добавить для получения раствора с новой заданной массовой долей.
Вычислите массу нитрата калия (в граммах), которую следует растворить в 160 г раствора с массовой долей этой соли 10% для получения раствора с массовой долей 12%. Ответ округлите до десятых.
Чтобы решить эту задачу, вспомним основную формулу нахождения массовой доли:
-
Найдем массу изначально растворенного нитрата калия в растворе, выразив из формулы выше:
подставим значения:
-
Чтобы увеличить массовую долю соли в растворе, необходимо ее добавить еще. Но мы не знаем сколько, поэтому примем массу добавляемой соли за Х и подставим в исходную формулу нахождения массовой доли с учетом новых значений:
-
Далее в дело вступает чистая математика. Разделим обе части уравнения на 100%:
-
По пропорции перемножим крест-накрест:
0,12 * (160 + X) = 16 + X.
-
Раскроем скобки:
19,2 + 0,12Х = 16 + Х.
-
Приведем подобные: с Х в одну сторону, без Х — в другую:
3,2 = 0,88Х.
-
Найдем Х:
Масса нитрата калия, которую необходимо добавить для увеличения массовой доли раствора до 12%, равна 3,6 граммам.
Ответ: 3,6.
Задание 28
Эта задача может встретиться на экзамене в нескольких вариантах. Давайте разберем один из них — задание на нахождение доли выхода продукта реакции.
В результате реакции тримеризации ацетилена объемом 26,88 л (н.у) получили 24,96 г бензола. Вычислите массовую долю выхода продукта реакции от теоретически возможного.
Решение:
-
Для начала напишем формулу, по которой считается доля выхода продукта:
Как определить, какая масса практическая, а какая — теоретическая? Значения, которые даются после слова «получили», — это практическая масса. Та, которая получилась в результате проведения химической реакции в реальных условиях. Масса теоретическая — та, которую рассчитывают из уравнения реакции, зная массу исходных реагентов.
-
Напишем уравнение химической реакции тримеризации ацетилена:
-
Найдем количество вещества ацетилена:
подставим значения:
-
Перейдем на количество вещества бензола, получаемого из ацетилена:
-
Зная количество вещества бензола, найдем его массу:
подставим значения:
m = 0,4 * 78 = 31,2 грамма.
-
Масса, рассчитываемая по уравнению реакции, является теоретической. Масса практическая дана нам по условию. Подставим полученные данные по массам в формулу для нахождения доли выхода продукта реакции:
Доля выхода бензола из данного объема ацетилена составляет 80%.
Ответ: 80.
Как оценивают готовые работы на ЕГЭ по химии
1-я часть
В 1-й части Единого государственного экзамена по химии задания 1–5, 9–13, 16–21, 25–28 оценивают 1 баллом, если вы запишете верный ответ по эталону. При этом в заданиях 1, 3, 4, 11, 12, 13, 17 и 18 ответ — это ряд цифр. То, в каком порядке вы их запишете, не влияет на оценку. Например, если в задании верны варианты под номерами 1 и 4, их можно записать как 14 или как 41. И в обоих случаях ответ засчитают как верный.
За правильные ответы в заданиях 6, 7, 8, 14, 15, 22, 23 и 24 можно получить по 2 балла. Если ваш ответ отличается от эталона на один символ, его оценят в 1 балл. Во всех остальных случаях задание считают выполненным неверно и ставят 0 баллов.
2-я часть
В этой части нужно записать не только ответ, но и решение. А значит, и оценивать такие задания будут сразу по нескольким критериям. Зато за верный ответ в некоторых вопросах можно получить больше баллов, чем за любое задание 1-й части. Максимум — 5 баллов. А теперь давайте разберемся, как именно их будут оценивать.
| Задание № 29 | Баллы |
|---|---|
| Ответ верный и полный: ученик выбрал вещества и записал уравнение химической реакции, составил электронный баланс, указал окислитель и восстановитель | 2 |
| Есть только один верный элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 2 |
| Задание № 30 | Баллы |
|---|---|
| Ответ верный и полный: ученик выбрал вещества, записал все нужные уравнения реакции | 2 |
| Есть только один верный элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 2 |
| Задание № 31 | Баллы |
|---|---|
| Правильно записаны 4 уравнения реакции | 4 |
| Правильно записаны 3 уравнения реакции | 3 |
| Правильно записаны 2 уравнения реакции | 2 |
| Правильно записано 1 уравнение реакции | 1 |
| Все уравнения реакции записаны неверно | 0 |
| Максимальный балл | 4 |
| Задание № 32 | Баллы |
|---|---|
| Правильно записаны 5 уравнений реакции | 5 |
| Правильно записаны 4 уравнения реакции | 4 |
| Правильно записаны 3 уравнения реакции | 3 |
| Правильно записаны 2 уравнения реакции | 2 |
| Правильно записано 1 уравнение реакции | 1 |
| Все уравнения реакции записаны неверно | 0 |
| Максимальный балл | 5 |
| Задание № 33 | Баллы |
|---|---|
| Ответ верный и полный, записаны все 3 элемента | 3 |
| Правильно записаны только 2 элемента ответа | 2 |
| Правильно записан только 1 элемент ответа | 1 |
| Все элемента ответа записаны неверно | 0 |
| Максимальный балл | 3 |
| Задание № 34 | Баллы |
|---|---|
| Ответ верный и полный, записаны все 4 элемента | 4 |
| Правильно записаны только 3 элемента ответа | 3 |
| Правильно записаны только 2 элемента ответа | 2 |
| Правильно записан только 1 элемент ответа | 1 |
| Все элемента ответа записаны неверно | 0 |
| Максимальный балл | 4 |
Как сдать ЕГЭ по химии на 3, 4 и 5
Мы уже познакомились с критериями, по которым будут оценивать работы на ЕГЭ. А теперь давайте разберемся, сколько баллов нужно получить для оценок 3, 4 или 5. Официально ЕГЭ не оценивают по пятибалльной системе с 2008 года. Если вам так проще оценить свои знания, их можно перевести. Но это будет лишь примерный перевод.
Будьте внимательны: баллы из таблиц выше — первичные, а требования к абитуриентам на поступление выражены в тестовых. Чтобы понять, сколько заданий точно нужно решить, чтобы поступить, надо перевести баллы из одной системы в другую. Это можно сделать по таблице ниже.
| Первичные баллы | Тестовые баллы | Оценка |
|---|---|---|
| <11 | <36 | 2 |
| 11–25 | 36–55 | 3 |
| 26–38 | 56–72 | 4 |
| 39–56 | 73–100 | 5 |
6 рекомендаций, как подготовиться к ЕГЭ по химии
Единый государственный экзамен — это ответственная задача, от результатов подготовки к которой иногда многое зависит. Чтобы немного облегчить для вас этот путь, мы собрали 6 простых, но рабочих советов от наших преподавателей. Следуйте им и тогда сможете подготовиться к экзамену по химии как можно лучше.
-
Узнайте все о структуре ЕГЭ и научитесь работать с КИМами.
-
Начинайте готовиться заранее. Но если получилось так, что осталось мало времени, составьте новый экспресс-план с помощью вашего преподавателя.
-
Ведите календарь подготовки к экзамену. Отмечайте на нем запланированные темы, разные методики, занятия у репетитора, пробные ЕГЭ и самоподготовку.
-
Распределяйте время на темы, исходя из ваших знаний. Больше учите то, что «западает», остальное — повторяйте.
-
Советуйтесь с учителем. Это может быть ваш преподаватель по химии или репетитор. Круто, если он сможет поделиться с вами опытом подготовки к ЕГЭ.
-
Заботьтесь о своем здоровье, не забывайте отдыхать, не лишайте себя живого общения. Все это может сказаться на вашем самочувствии, а значит, и баллах тоже.
Если вы хотите сдать ЕГЭ по химии на 100 баллов, советуем тщательно продумать, как вы будете готовиться к нему. Лучший из них — совмещать самостоятельную работу и дополнительные занятия.
На курсах подготовки к ЕГЭ по химии в Skysmart школьники отрабатывают все типы задач и разбирают критерии оценок. Для каждого из них мы составляем индивидуальный план, который приведет к нужным баллам. Он учитывает уровень знаний ученика и время до экзамена, что позволяет «выжать» максимум из подготовки. А еще мы рассказываем о ЕГЭ без «страшилок» и прикрас, чтобы школьник точно знал, что его ждет на экзамене. Ждем на первом бесплатном занятии!
Эффективные приемы подготовки к ЕГЭ по химии
Автор: Пащенко Вячеслав Сергеевич
Организация: МБОУ СОШ №2
Населенный пункт: Ростовская область, г. Батайск
Как показывает опыт, готовиться к итоговой аттестации ученик начинает за год до проведения экзамена, в лучшем случае за два. Поэтому преподаватель должен грамотно организовать учебно-познавательную деятельность учащегося. Необходимо подобрать важные, ключевые моменты, на которых основываются составители контрольных материалов. С чего лучше начать подготовку выпускника к ЕГЭ по химии? Прежде всего, на первом занятии проводится проверка усвоенных (остаточных) знаний. По результатам проверки на каждого учащегося составляется индивидуальный план. У каждого ученика имеются свои слабые места, поэтому и акценты будут расставлены по-разному. В каждом разделе химии выделяются блоки, группируются темы. В зависимости от сложности тем, при подготовке следует выделять разное количество часов. Например, в блоке «Теоретические основы химии» темы «Современные представления о строении атома», «Периодический закон и Периодическая система химических элементов Д.И.Менделеева», «Химическая связь и строение вещества» повторяем на одном занятии, на такие темы как «Свойства простых веществ и образованных ими соединений» необходимо выделить больше часов, так как это очень объемный материал, требующий от учащихся глубоких знаний о свойствах веществ и их соединений. На первом же занятии нацеливаем детей на то, что химию зубрить не надо, её нужно понимать, видеть закономерности и тогда знания выстраиваются в систему. Если ученик знает законы и правила, он может предсказать и описать свойства незнакомого вещества. Подготовка к экзамену осуществляется по индивидуальным образовательным траекториям учащихся. Весь материал разбивается по блокам: 1. Теоретические основы химии 2. Неорганическая химия 3. Органическая химия 4. Методы познания в химии. Химия и жизнь. Исходя из строгой структуры содержания образовательных траекторий, становится возможной подготовка по пяти основным направлениям: − подготовка по блокам содержания (для учащихся с высоким уровнем подготовки (от 60% на пробном тестировании) и планирующим занятия за 1-2 года до экзамена); − подготовка по вопросам ЕГЭ двух частей (для учащихся со средним уровнем подготовки (30-60%) и планирующим занятия менее чем за год до экзамена); − подготовка к первой части (для учащихся с низким уровнем подготовки и большими пробелами в знаниях); − подготовка ко второй части (для тех, кто отлично справился с подготовкой к первой части); − комбинированная подготовка к ЕГЭ (как правило, её реально осуществить только с учащимися, планирующими занятия за 2 года до экзамена). Сюда включена подготовка по блокам содержания и подготовка по вопросам всего контрольного материала Подготовку к экзамену по химии со школьниками с низким и средним уровнями подготовки считаем целесообразным начинать с тем «Основные понятия химии. Номенклатура неорганических и органических веществ». С сильными школьниками, при этом, лучше идти дедуктивным путём, т.е. начинать повторение с тем «Строение атома. Химическая связь». Особое внимание обращаться на следующие темы: основные классы неорганических веществ; окислительно-восстановительные реакции, электролиз; реакции в растворах электролитов, гидролиз; химическая кинетика и химическое равновесие. Из опыта работы могу выделить основные проблемы у выпускников при подготовке к ЕГЭ:
1. По программе базового уровня недостаточно количество часов для успешной сдачи экзамена;
2. Трудности при проведении практической части (реактивы, оборудование не все имеются в достаточном количестве);
3. Нерациональное распределение времени при выполнении заданий;
4. Учащиеся, которые выбрали предмет «Химия» в формате ЕГЭ, имеют разный уровень подготовки; 62
5. Слабые знания по физике и математике. Очень многие родители и сами учащиеся почему-то считают, что подготовка к ЕГЭ – это натаскивание на тесты. Считаем, что это самая большая ошибка. Безусловно, необходимо отрабатывать имения решать тестовые задания, но, не имея прочных теоретических знаний выполнение тестовой части невозможно. Натаскивание на тесты – это просто тренировка интуиции. Те дети, у которых хорошие знания предмета, обязательно хорошо сдадут ЕГЭ. На самом деле, нет ничего необычного в том, как готовить школьников к ЕГЭ. Не надо этого бояться. Если учитель хорошо знает, объясняет и любит свой предмет, умеет его преподнести, то обязательно сможет подготовить и к ЕГЭ по своему предмету. С чего следует начать? Первое занятие следует посвятить знакомству со структурой КИМа, ценой каждого задания, с правилами распределения времени при выполнении экзаменационных заданий. Проводится входная диагностическая работа, при проверке которой вырисовывается уровень знаний обучающегося. Такая же работа проводится регулярно после изучения тем или блоков. Проводится диагностика качества знаний. Это дает возможность выпускнику получить информацию, необходимую для принятия продуктивных решений. Диагностика как аналитико-оценочная деятельность включает механизмы саморазвития, предоставляет возможность стратегического прогнозирования конечного результата. Ученик сам видит, как изменяется уровень его подготовки. На первом занятии даётся ряд советов:
Совет 1. Освойте химический язык: Карбонат, нитрат, хлорат. Что у них общего? Чем сульфит отличается от сульфида? А хромат – от дихромата? Правила составления формул и названий в химии – универсальны. Каждый суффикс или префикс соответствует определенной формуле. Зная этот язык, вы по названию определите класс вещества и сможете описать его свойства.
Совет 2. Три главные таблицы – ваши официальные шпаргалки на экзамене. На экзамене по химии выдаётся три справочных таблицы: таблица Менделеева, таблица растворимости и ряд активности металлов. 70% всей химической информации можно получить из этих таблиц, если уметь ими пользоваться. Моя задача – научить находить ответы в этих таблицах. Анализировать их.
Совет 3. Подтяните математику. Если у вас не получаются задачи по химии – возможно, проблема с математикой? Задачи первой части на проценты, сплавы, растворы необходимо отработать до автоматизма.
Совет 4. Ничего не принимайте на веру. Задавай вопросы. Если учащийся не понимает, – нет смысла зубрить или просто конспектировать материал. Толку никакого не будет. Нужно постоянно 63 задавать вопросы себе и другим. Только таким способом можно добиться успеха. Необходимо уметь искать ответы в книгах, у учителя, на химических сайтах в интернете. Если ученик вежливо слушает и не задаёт вопросов – значит, занятие проходит впустую.
Совет 5. Уделяйте повторению теоретического материала каждый день 20-30 минут. Помните! Не зубрить, а именно читать, осмысленно анализировать. Чередуйте чтение с выполнением тестовых, демонстрационных вариантов. Выбирайте для этого время, когда вам ничто не мешает сосредоточиться. Хочется остановиться ещё на одном вопросе при подготовке к итоговой аттестации по химии – умение решать качественные экспериментальные задачи. При решении таких задач происходит самообразование учащихся, актуализация необходимых знаний, построение плана работы, анализ эксперимента, подведение итогов. Ведь не секрет, что открытие, которое ученик делает сам, гораздо лучше запомнятся, а это приведет к повышению положительного эмоционального настроя и уверенности в своих силах. Эффективные методы и формы подготовки, учащихся к успешной сдаче экзамена по химии: Бесплатные On-line тесты ГИА 11 класс Различные пособия для подготовки к ОГЭ и ЕГЭ Интерактивные тесты на http://nsportal.ru/ Видеоуроки для подготовки к ГИА. Большой материал по подготовке к ЕГЭ размещен на Интернет ресурсах http://www.fipi.ru/, http://reshuege.ru/, http://egeigia.ru/ сайт СтатГрад Крайне эффективной становится работа накануне экзамена. Она выстраивается следующим образом: в преддверии экзамена проводить ежедневные консультации в течение 5 дней по 1 часу. На них выпускники смогут получить последние наставления, советы, прояснить те вопросы, которые представляют наибольшую трудность.
В заключении хотелось бы отметить, что наиболее эффективными формами, методами и приемами по подготовке к ЕГЭ по химии являются следующие: − работа заданиями в форме тестов; − дифференцированный подход в обучении и подготовке; − индивидуальные занятия, консультации, обзорные уроки; − формирование у учащихся на уроках химии умений, навыков, развитие компетенций, необходимых для успешной сдачи ЕГЭ; выполнение диагностических работ после изучения каждой темы с помощью тестирования, тренажеров по ЕГЭ; − решение максимально возможного количества тестов – вариантов ЕГЭ с последующим анализом допущенных ошибок. Если говорить о технологиях обучения, то это технология обучения в сотрудничестве, личностно ориентированное обучение. И все-таки, приоритетным становится направление на самостоятельную активную познавательную деятельность каждого ученика с учетом его особенностей и возможностей, деятельность, не всегда укладывающуюся в систему урока. Конечно, как бы ни работал учитель, главным в достижении положительного результата является желание самого выпускника сдать хорошо экзамен и соответственно понимание необходимости регулярных занятий по химии.
Приложения:
- file1.docx.. 17,2 КБ