Задания
Версия для печати и копирования в MS Word
Задания Д9 № 10236
Какие объекты не имеют клеточного строения?
1) дизентерийная амёба
2) возбудитель СПИДа
3) вирус табачной мозаики
4) кишечная палочка
5) вибрион холеры
6) бактериофаг
Спрятать пояснение
Пояснение.
Вирусы не имеют клеточного строения. Бактерии состоят из клеток. Вирусы: возбудитель СПИДа; вирус табачной мозаики; бактериофаг.
Ответ: 236.
Раздел кодификатора ФИПИ: 4.1 Многообразие организмов. Основные систематические категории. Вирусы
Спрятать пояснение
·
·
Сообщить об ошибке · Помощь
Открытие вирусов
В 1892 году русский ученый Д. И. Ивановский, изучая заболевание табака, проявляющееся появлением на листах растения своеобразной мозаики, обратил внимание на необычные свойства его возбудителя.
В попытке определить вид организма, вызывающего болезнь, ученый использовал световой микроскоп, однако никаких признаков присутствия в препарате бактерий, грибов или простейших он не обнаружил. Тогда биолог сделал вывод о том, что возбудитель настолько мал, что его невозможно увидеть. Поскольку инфекционная природа заболевания была очевидна (контакт с больным растением вызывал заболевание у здорового), ученый поставил перед собой задачу доказать, что существует какой-то агент, который способствует заражению все новых и новых растений.
Чтобы подтвердить свою теорию, он провел эксперимент. Выделив сок больного растений, он пропустил его через фильтр. Фильтр при этом имел достаточно мелкую структуру и достоверно не мог пропустить через себя даже самые мелкие бактерии. После этого биолог обработал полученным соком здоровое растение и наблюдал развитие заболевание. Эксперимент подтвердил, что существует особенный, «фильтрующийся» вид возбудителей, который способен вызывать болезни. Сам Ивановский еще не использовал термин «вирус», однако своими исследованиями заложил базу для развития науки вирусологии в дальнейшем.
С развитием техники появилась возможность визуализации даже таких небольших структур как вирусы. Было выявлено, что они представляют собой необычные организмы, состоящие из молекулы нуклеиновой кислоты и окружающей ее белковой капсулы.
Еще Ивановский заметил, что вирусы не способны размножаться и развиваться вне организма (на искусственно созданных питательных средах), и этим они отличались от всех других живых существ.
Позднее были выявлены и другие организмы, имеющие подобное строение и схожие особенности жизнедеятельности.
Например, в 1917 году французский микробиолог Д’Эррель открыл бактериофаг – вирус, поражающий исключительно бактерии. Этот термин обязательно нужно знать, он часто встречается на экзамене.
Строение вирусов
В зависимости от строения вирусы делят на простые и сложные.
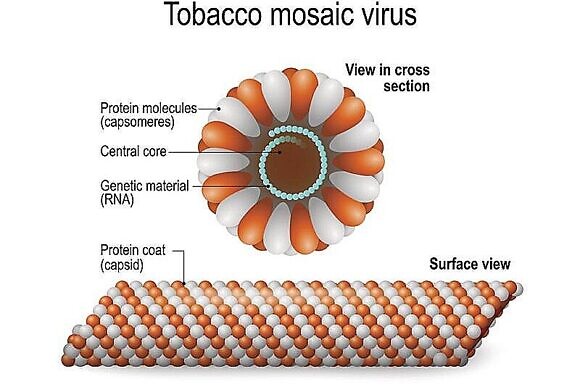
Простые вирусы состоят только из нуклеиновой кислоты (ДНК или РНК) и белковой оболочки (капсида). Расположение молекул белка относительно нуклеиновой кислоты может быть различным:
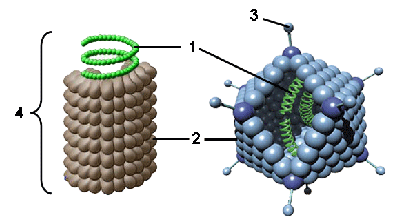
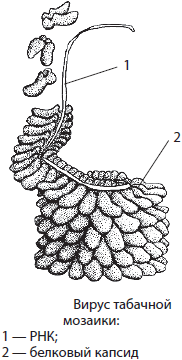
Рисунок 1. Строение вируса
На первом рисунке изображен вирус табачной мозаики (4), у которого нуклеиновая кислота (1) с помощью белков (2) закручена по спирали. На втором рисунке цифрой 3 отмечены антигены вируса, выступающие над поверхностью его оболочки.
Сложные вирусы также имеют НК и капсид, но в дополнение к последнему они получают дополнительную оболочку. Эта оболочка не относится собственно к вирусу, она образуется в процессе выхода из клетки хозяина, это часть ее клеточной мембраны. Такое строению характерно, например, для вируса гриппа.
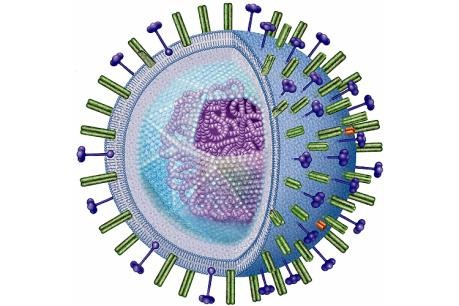
Рисунок 2. Вирус гриппа
Обратите внимание: у вирусов нет ни ядра, ни цитоплазмы, ни цитоплазматической мембраны, поэтому мы не можем сказать, что вирусы имеют клеточное строение. Их относят к доклеточным формам жизни.
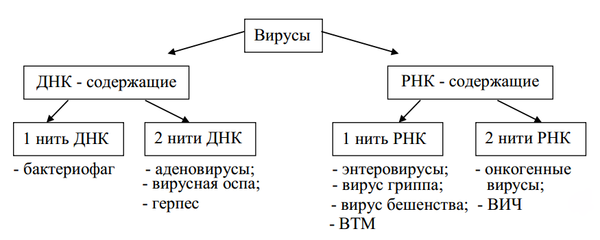
Помимо разделения вирусов на простые и сложные, есть и масса других классификаций. В составе сердцевины вируса могут быть самые различные нуклеиновые кислоты, в зависимости от этого их делят на следующие группы:
Жизнедеятельность вирусов
В тоже время вирусы считают неживыми системами, так как у них не проявляются все признаки живого, например, отсутствует собственный обмен веществ.
Однако стоит отметить, что некоторые свойства живого у вирусов все-таки выражены: они имеют сходное химическое строение с клетками живого, обладают наследственностью изменчивостью и способностью к самовоспроизведению (только в организме хозяина). Типичным примером изменчивости может служить вирус гриппа А, который ежегодно мутирует и рождает новые штаммы вируса, ежегодно поражающие население земного шара.
Вирусы являются облигатными паразитами, использующими живых существ в качестве среды обитания. Поражать они могут и животных, и растения, и бактерии, и грибы.
У человека вирусы вызывают развитие многих инфекционных заболеваний: оспы, герпеса, гепатита, гриппа, бешенства, СПИДа (и т. д). Знать эти заболевания и уметь отличать их от бактериальных инфекций нужно обязательно.
Вирусные заболевания
|
Название болезни |
Поражаемые области тела |
|
Грипп |
Дыхательные пути |
|
Гепатит |
Печень |
|
Герпес |
Кожа на губах, слизистая оболочка глотки, нервные ганглии |
|
Оспа |
Дыхательные пути, затем кожа |
|
Свинка (паротит) |
Дыхательные пути, затем генерализованная инфекция |
|
Корь |
Дыхательные пути, затем переходит на кожу и кишечник |
|
Коревая краснуха (краснуха) |
Дыхательные пути, шейные лимфатические узлы, глаза и кожа |
|
Полиомиелит (детский паралич) |
Глотка и кишечник, затем кровь; нервная система: двигательные нейроны спинного мозга, тогда может наступить паралич |
|
Желтая лихорадка |
Кровеносные сосуды и печень |
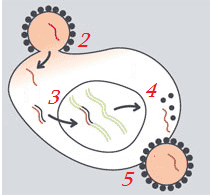
Цикл развития вируса
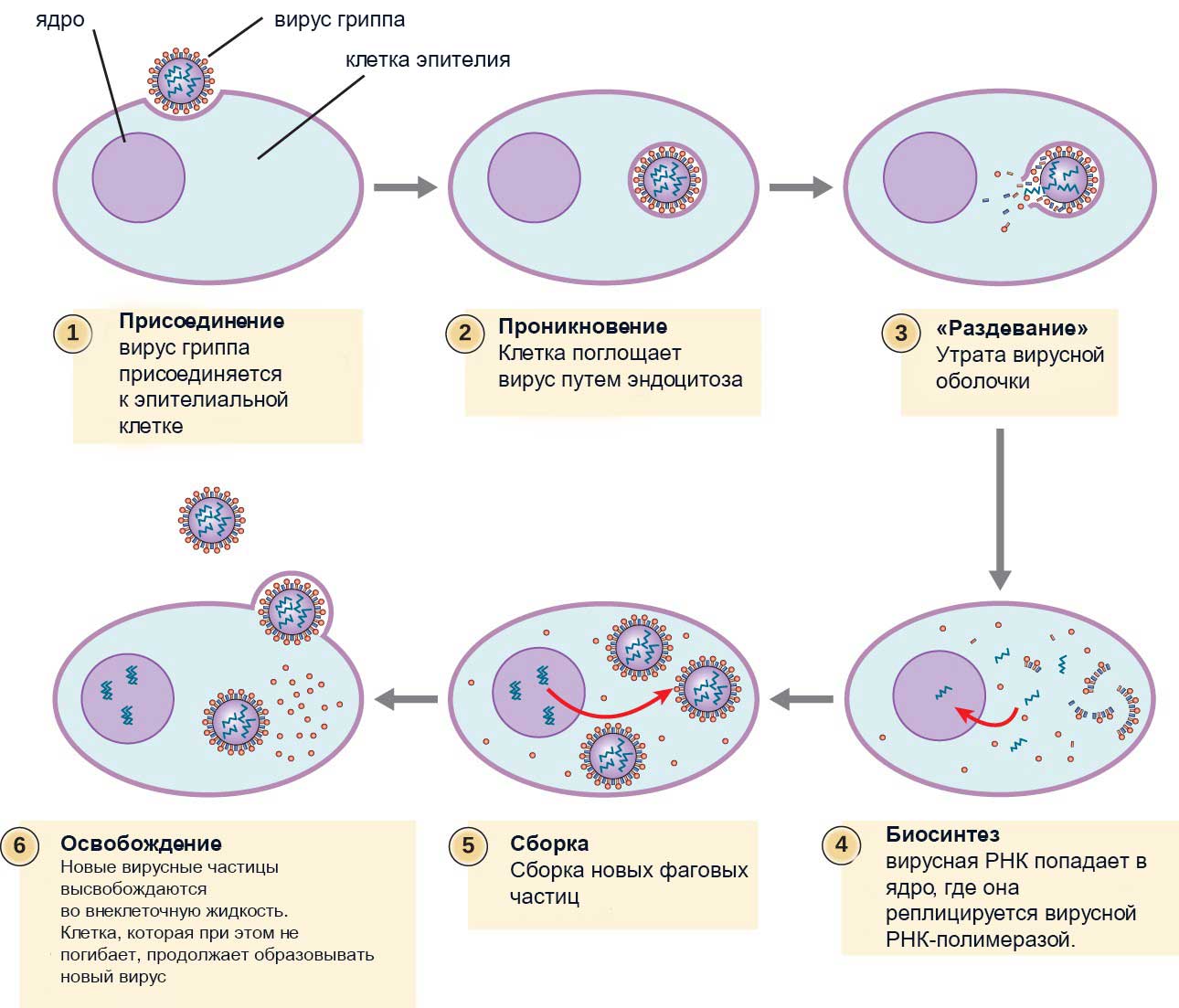
1. Попадая в организм, вирусы ищут клетку-мишень (вирусы часто имеют тропность к определенному виду клеток, например ВИЧ связывается с клетками иммунной системы – лимфоцитами). Прикрепление вируса к клетке опосредовано рецептором. В случае его отсутствия возбудитель не может связаться с ней и в итоге выводится из организма, не вызвав заболевание. У некоторых людей отсутствуют рецепторы, позволяющие вирусу иммунодефицита прикрепиться к клеткам крови, поэтому они не болеют СПИДом, однако, стоит отметить, что таких людей крайне мало. Этап взаимодействия вируса с рецепторами клеток хозяина называется адсорбцией.
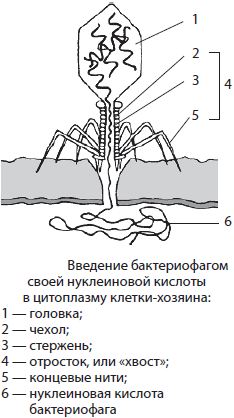
2. После установления контакта вирус проникает внутрь клетки, при этом капсид и наружная оболочка остаются снаружи или растворяются ферментами внутри клетки хозяина, а РНК или ДНК вводятся в цитоплазму. У бактериофага есть специальная ножка, которая помогает ему «впрыскивать» нуклеиновую кислоту в клетку. Этот процесс называется инъекцией вируса в клетку.
3. Далее нуклеиновая кислота встраивается в генетический аппарат клетки хозяина, и начинает воспроизводиться параллельно с ним. При этом клетка хозяина не погибает от этого воздействия, она лишь тратит на вирус часть своих ресурсов. Происходит репликация молекул вирусной нуклеиновой кислоты.
4. В ходе этого процесса в клетке синтезируются новые вирусные НК и молекулы белка, которые организуются в белковые оболочки для новых вирусов. Этот этап можно назвать синтезом вирусных компонентов.
5. Далее происходит сборка вирусных частиц в цитоплазме клетки хозяина.
6. Выход вируса из клетки может осуществляться двумя путями: либо происходит «взрыв» клетки, и все вирусные частиц оказываются вне ее, в таком случае клетка погибает, либо вирусные частички «отпочковываются» от нее, при этом сохраняя ее жизнеспособность.
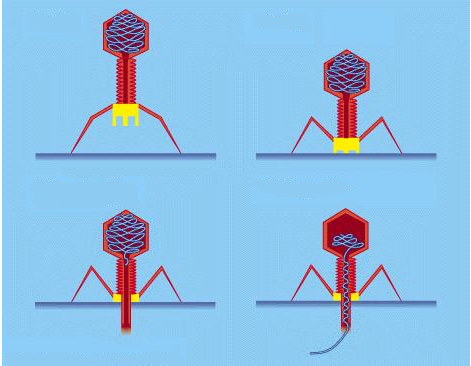
Схематично цикл развития вируса представлен на рисунке ниже:
Термин «вирус», virus, происходит от латинского слова «яд». Вирусы — инфекционные агенты, не существующие самостоятельно. Они встраиваются в клетку и воспроизводят в ней свои гены, переключая ее на производство вирусных белков. Поэтому мы говорим, что вирусы — это неклеточная форма жизни, облигатные паразиты, которые функционируют только внутри организма, а в открытой среде рано или поздно погибают.
В 1892 году отец вирусологии Д. И. Ивановский опубликовал труд, посвященный вирусам. Но и сегодня открытия в этой области продолжаются. Вирусы чрезвычайно малы, их размеры колеблются в интервале от 20 до 300 нм. Они не выращиваются, как бактерии, на искусственных средах, что затрудняет исследования.
Вирусные инфекции делятся на три типа в зависимости от того, как долго вирус находится в клетке, и какие с ней при этом происходят изменения.
1. Литическая
(от греч. лизис — разрушение) инфекция — пораженная клетка гибнет, вирусы покидают ее и «нападают» на другие клетки.
2. Персистентная
(стойкая) инфекция — вирусы оставляют клетку постепенно, клетка живет, но ее функционирование изменено.
3. Латентная (скрытая) инфекция — гены вируса встраиваются в хромосомы хозяйской клетки и передаются дочерним клеткам. Вирусы никуда не мигрируют, могут не активизироваться годами. Однако латентная инфекция может перейти в персистентную или литическую при активизации, размножении и выходе вируса из клетки. В связи с этим вирусы переносят гены от одного организма к другому, копируя части генов разных организмов.
Строение вирусов
1. Вирусы — генетические элементы, одетые в белковую оболочку и переходящие из одной клетки в другую.
2. У вирусов два основных вида симметрии, спиральная и кубическая.
3. Вирион
— отдельная вирусная частица с генетическим материалом в виде ДНК или РНК. Имеет симметричное строение.
4. Капсид — главная белковая оболочка, защищающая вирус от ультрафиолета и действия ферментов нуклеаз, которые разрушают нуклеиновые кислоты. Капсиды имеют многие цепи одного или нескольких типов белков. В состав капсида могут входить не только белки, но и гликопротеины — белки, связанные с углеводами.
5. У некоторых вирусов имеется внешняя оболочка — из липидов, заимствованных из плазмалеммы хозяина. Вирус гриппа имеет наружную оболочку кубического типа симметрии, но при этом спиральный вирион.
На чем основана современная классификация вирусов?
1. Вид и форма нуклеиновой кислоты (РНК — ДНК, линейная — кольцевая, одноцепочечная — двуцепочечная).
2. Тип симметрии — кубическая или спиральная.
3. Присутствие или отсутствие наружной оболочки.
Варианты вирусов по наличию ДНК или РНК
|
Вирусы с ДНК |
Вирусы с РНК |
|||
|
Вирусы с двухцепочечной ДНК. |
Вирусы с одноцепочечной ДНК. |
Вирусы с одноцепочечной РНК. |
Вирусы с двухцепочечной РНК. |
Вирусы с двумя идентичными одноцепочечными РНК. |
|
ДНК могут быть кольцевой или линейной формы (двухцепочечные более разнообразные). |
Такие вирусы могут иметь только кольцевую ДНК. |
Вирус табачной мозаики. Вирус гриппа. |
Вирус гепатита В. |
Некоторые онкогенные (опухолеродные) вирусы (капсид у них кубический). |
|
Бактериофаг Т4, вирус оспы имеют двухцепочечную линейную молекулу ДНК. Кстати, вирус оспы самый крупный и содержит 240 генов! Обезьяний вирус SV40 содержит двухцепочечную кольцевую ДНК. |
Пример — фаг М13, паразитирующий в клетках E. coli. |
Онкогенные ретровирусы имеют внешнюю оболочку. Вирус ВИЧ имеет такое же строение. |
Вирусы
Вирусы (от лат. вирус — яд) – представляют собой мельчайшие неклеточные формы жизни. Вирусы имеют размеры 2-5*10-7см, что значительно меньше, чем бактериальная клетка (от 0,2 до 10 мкм). Рассмотреть вирусы возможно только с помощью электронного микроскопа, увеличивающий в 100 тысяч и более раз. Вирусы относятся к отдельному царству.
Вирусология – наука изучающая вирусы. Становление вирусологии как науки начинается с 30-х годов 20 века.
История открытия вирусов
Впервые вирус табачной мозаики (рис.1) был открыт русским ученым Д.И.Ивановским (1892г.) (рис.2).
Рис.1 Листья табака (слева) пораженные вирусом табачной мозаики (справа)
Студент Петербургского университета Дмитрий Ивановский выезжал на Украину и в Бессарабию для определения причин болезни табака. В листьях табака будущий ученый не обнаружил клеток бактерий, однако было замечено, что сок зараженного растения поражал здоровые листья. Используя свечу Шамберлана Ивановский профильтровал сок больного растения, тем самым исключив прохождение через фильтр мелких бактерий. Полученный фильтрат все равно вызывал заражение листьев табака. Это еще раз доказывало «невиновность» бактерий. Д.И.Ивановский попробовал культивировать возбудителя на питательной среде, однако это не дало результата. После проведенных опытов Дмитрий Иосифович пришел к выводу, что возбудитель является необычной природы и имеет размеры в разы меньше чем клетка бактерии. В последствие возбудитель был назван «фильтрующиеся бактерии».
Рис.2 Д.И.Ивановский — первооткрыватель вирусов
Свои выводы ученый изложил в труде «О двух болезнях табака» в 1892 году. Именно этот год считается годом открытия вирусов.
Наряду с Д.И.Ивановским изучением вирусов занимался голландский микробиолог Мартин Бейеринк, который в 1898 году повторив опыты русского ученого, назвал вирусный раствор – «заразной живой жидкостью» или «жидкий живой контагий».
Первый вирус животных (вирус ящура) был описан в 1897 году Лёффером и Фрошем. В 1901 году вирус желтой лихорадки был открыт англичанами У. Ридом и Д. Кэрроллом.
В 1917 году Ф.д’Эррелем был открыт бактериофаг – вирус, поражающий бактерии.
Удивительно то, что первая вакцина от оспы была предложена за 100 лет до открытия вирусов, в 1796 году английским врачом Э.Дженнером. Второй по открытию стала – антирабическая вакцина, представленная французским ученым микробиологом Л.Пастером в 1885 году.
Названия «ультравирус» и «фильтрующий вирус» использовались в науке до укоренившегося ныне краткого термина — «вирус», который впервые применил Л.Пастер.
Строение и формы вирусов
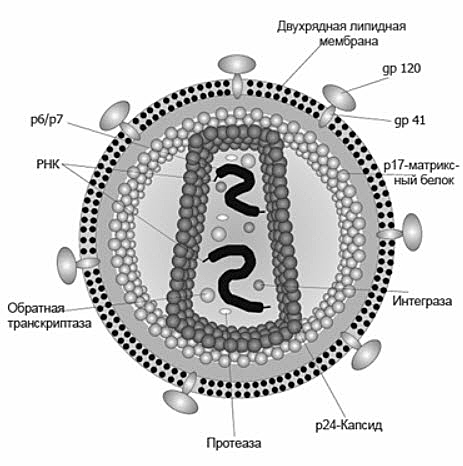
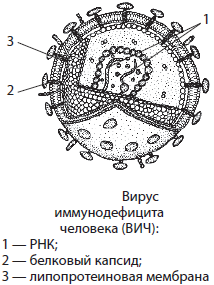
Вирусы — неклеточные частицы, состоящие из белковой оболочки (капсид) и собственного генетического материала в виде нуклеиновой кислоты (ДНК или РНК) (рис.3).
Рис.3 Строение вируса иммунодефицита человека (ВИЧ)
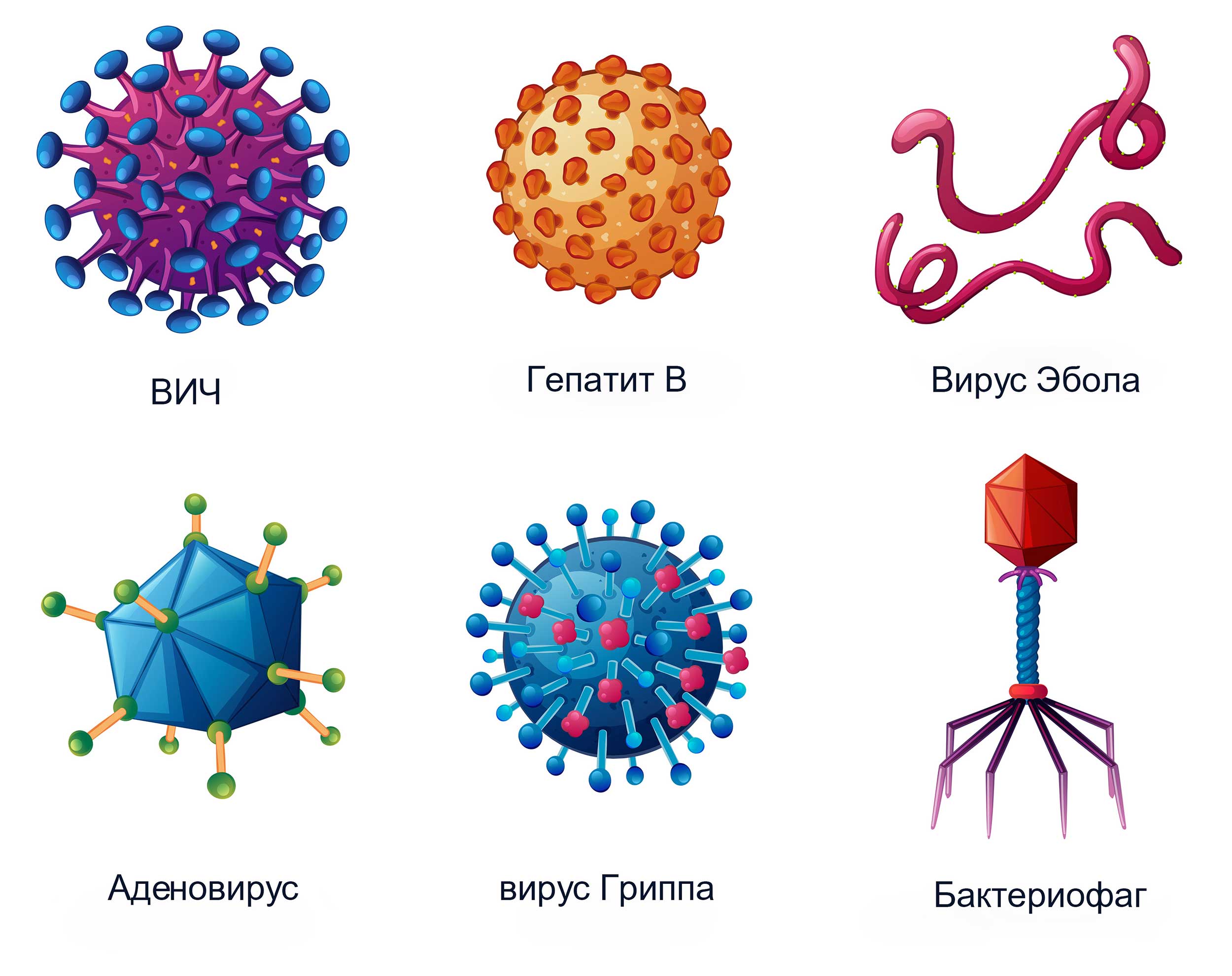
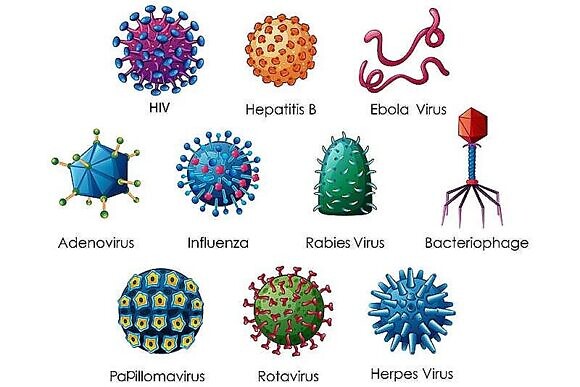
Вирусы могут обладать разнообразными формами: шаровидные, овальные, палочковидные, нитевидные, цилиндры, тетраэдры, октаэдры и др.(рис.4).
Рис.4 Разнообразные формы и виды вирусов
Более сложные вирусы имеют в своем составе дополнительные белковые или липопротеидные оболочки. Вирусы гриппа и герпеса кроме белковой оболочки могут содержать и углеводы.
| ДНК-содержащие вирусы | РНК-содержащие вирусы |
|---|---|
| оспы | бешенства |
| герпеса | кори |
| бактериофаги Т-группы | СПИДа и лейкоза |
| гепатита В | гепатита А |
| паповавирусы | гриппа |
| аденовирусы | полимиелита |
| цитомегаловирус | ОРЗ |
| Эпштейн-Бара | желтой лихорадки |
| и др. | краснухи и др. |
Геном вирусов может быть представлен однонитчатыми и двунитчатыми молекулами ДНК (вирус оспы человека, овец, свиней, аденовирус человека) и РНК (матрица для вирусов насекомых и других животных). Вирусы с однонитчатой молекулой РНК (энцефалит, краснуха, корь, бешенство, грипп и др.).
Вне живой клетки вирус не питается, не передвигается, не растет, не размножается и не проявляет других свойств живого.
Размножение вирусов
Вирусы способны размножаться только внутри живой клетки. Вирус проникает внутрь клетки путем связывания его с особым протеином – рецептором, расположенным на поверхности клетки. На поверхности чувствительной клетки происходит связывание с рецептором, после чего присоединившейся участок погружается в цитоплазму и превращается в вакуоль. Стенки вакуоли, состоящей из цитоплазматической мембраны способны сливаться с другими вакуолями или даже ядром. В результате вирус достигает любой участок клетки.
Основные этапы заражения вирусом:
1.Присоединение вируса к мембране клетки-хозяина.
2.Впрыскивание своей нуклеиновой кислоты (НК) в цитоплазму клетки-хозяина. Капсид остается снаружи.
3. ДНК вируса у эукариотической клетки проникает в ядро клетки и встраивается в ДНК хозяина. В бактериальной клетке ДНК вируса встраивается в ДНК бактерии. РНК содержащие вирусы вначале делают из нее копию в виде ДНК, а затем полученную ДНК встраивают в хромосому или нуклеотид клетки-хозяина.
4. Генетический материал клетки хозяина перестает функционировать. В ядре осуществляется синтез копий вирусной НК, а в цитоплазме на рибосомах – синтез копий вирусного капсида.
5. Образуются функциональные вирусы. НК «одевается» в капсид, происходит сборка вирусных частиц.
6. Образовавшиеся вирусы выходят из клетки-хозяина, так как первая исчерпала свои ресурсы. Вирусы продолжают проникать в новые клетки, расположенные поблизости.
Описанные этапы характерны для литических (от греч. «лизис» — растворение, разрушение, распад) вирусов, вызывающие разрушение или гибель клетки. Существует так же второй вид, так называемых «умеренных» вирусов. Они встраиваю свою нуклеиновую кислоту в ДНК клетки.
Паразитируя на генетическом уровне живой клетки, они встраиваются в ее геном. Внедрив свой генетический код в молекулу ДНК, вирус становится частью живой клетки. В такой форме он может не проявлять себя неопределенно долгое время. В какой-то момент вирусные частицы ДНК «включаются» одновременно во всех зараженных клетках, вызывая их гибель.
Данный процесс до конца не изучен, и возможно именно он мог бы решить вопрос возникновения онкологических заболеваний.
Быстрая способность адаптироваться и видоизменяться, подстраиваясь к геному клетки, делает некоторые вирусные заболевания практически неизлечимыми. Таким образом, вирусы представляют паразитизм на генетическом уровне (рис.5).
Рис.5 Размножение вируса гриппа
Бактериофаги
Совсем по-другому проникает в клетку вирус бактерий – бактериофаг (от греч. фагос – «пожирающий»)(рис.6).
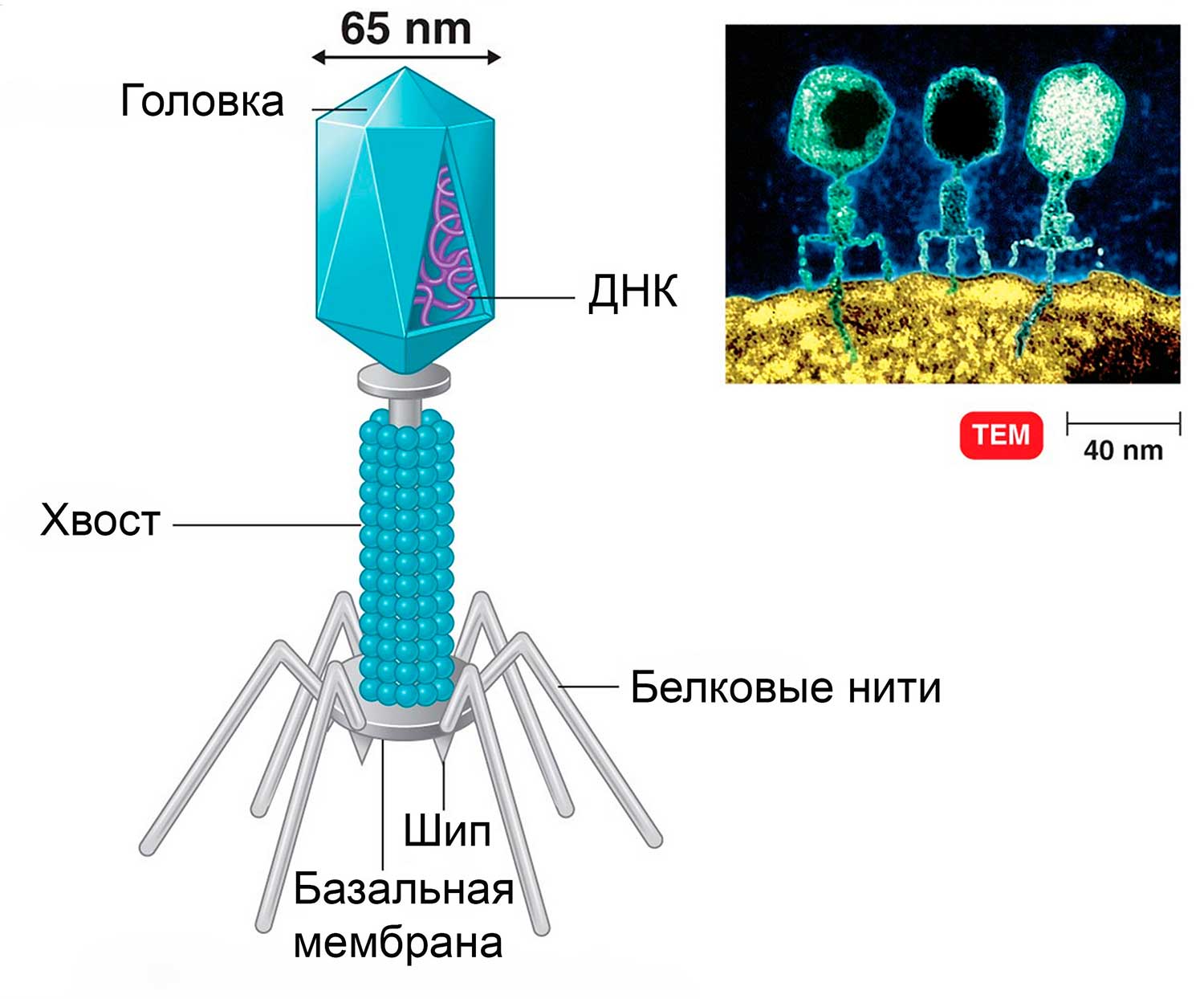
Рис.6 Строение бактериофага
Бактериофаг состоит из головки, хвостика и нескольких хвостовых отростков (белковых нитей). Наружная часть головки покрыта белковой оболочкой. Во внутренней части головки расположена ДНК, а внутри хвоста проходит центральный канал. Из-за толстых клеточных стенок бактерий белок-рецептор бактериофага не может погрузиться в цитоплазму.
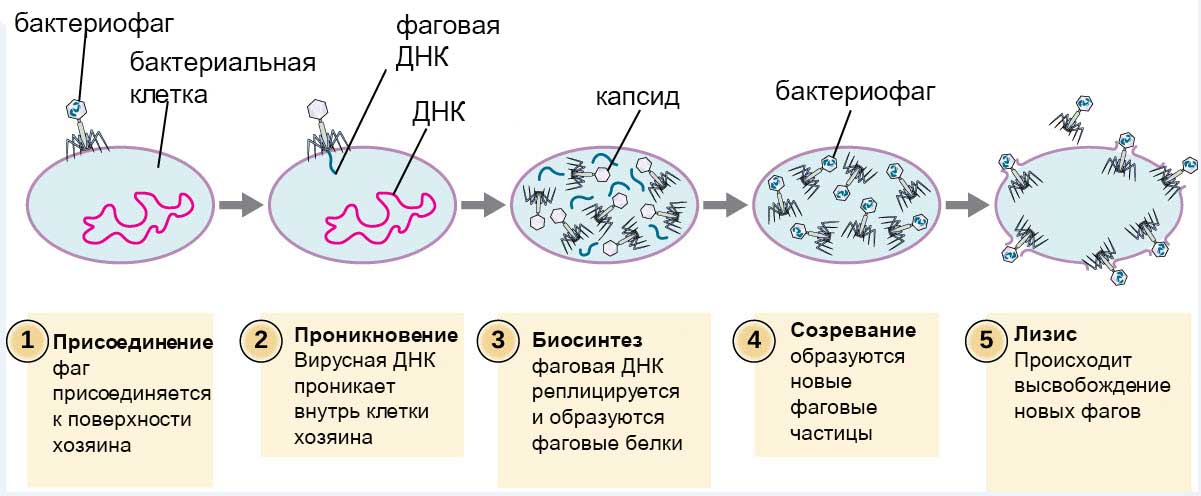
Удерживаясь на поверхности клетки за счет шипов, расположенных под базальной мембраной, бактериофаг пронзает стенку бактерии и вводит внутрь полый стержень. По этому стержню в цитоплазму поступает ДНК (или РНК). Геном бактериофага проникает внутрь клетки, а оболочка остается снаружи. Спустя время, сформировавшиеся зрелые фаговые частицы разрушают бактерию изнутри и выходят наружу (рис.7).
Рис.7 Размножение бактериофага
Обладая способностью полного уничтожения бактериальной клетки, бактериофаги могут быть использованы для лечения разнообразных бактериальных заболеваний (холеры, дизентерии, брюшного тифа и др.).
Отмечено, что отделение от вирусной частицы нуклеиновой кислоты приводит к потере инфекционной способности к репродукции. Это говорит о том, что нуклеиновая кислота играет важную роль в размножении вируса.
При благоприятных условиях вирус очень быстро размножается. Так, за 30 минут в одной клетке появляются сотни новых вирусов.
Вирусы могут продолжительно сохраняться в почве, воде и другим средах. Некоторые представители устойчивы к высоким температурам (свыше +100С) и высушиванию.
Виды вирусных заболеваний
В настоящее время известно около 400 видов вирусов растений и около 500 видов вирусов животных.Вирусы растений вызывают поражение листьев и других органов, вызывая появление разноцветных или бесцветных пятен и полосок. Вирусы вызывают замедление роста растений, изменяет их форму и снижает урожайность.
Наиболее опасными для человека являются вирусы гепатита – А, В, С. Вирус способен сильно повреждать ткани печени, вызвав необратимые последствия.
ВИЧ.СПИД
Более опасную для человечества форму представляет вирус иммунодефицита человека или сокращенно ВИЧ (HIV). Попав в кровь, ВИЧ, поражает иммунную систему человека, приводя к развитию болезни под названием СПИД (синдром приобретенного иммунодефицита человека). РНК-содержащий ВИЧ атакует белые кровяные клетки – лимфоциты, отвечающие за иммунитет, делая человека уязвимым для других болезней.
Внедренный в лимфоциты РНК вирус начинает синтезировать фермент – ревертазу. Этот фермент служит матрицей для последующего синтеза молекулы ДНК. Синтезированная вирусная ДНК встраивается в хромосому лимфоцита. После чего вирус долгое время может не проявлять себя. Это может длиться от 1 до 2 лет, а иногда и более. Спустя время вирусная ДНК начинает проявлять себя, синтезируя сотни тысяч вирусов, что в итоге приводит к разрушению лимфоцита.
Вероятность заражения ВИЧ увеличивается при прямом контакте с кровью больного человека. Распространенные пути передачи вируса; незащищенный половой контакт с инфицированным человеком, инъекции шприцом, переливание крови. ВИЧ не передается воздушно-капельным путем, через укусы насекомых, посуду, при рукопожатиях и пользовании общественными местами (туалеты, бассейны, бани и т.п.).
В настоящее время вакцины против СПИДа нет, но существуют медицинские препараты на основе азотимидина и ингибиторов протеаз, способные подавить синтез вирусной ДНК. Это облегчает течение болезни и значительно удлиняет жизнь человека.
Хочется отметить, что ВИЧ инфицированный человек, вовремя обратившийся в центр СПИДа, может контролировать развитие этой тяжелой болезни и в принципе жить полноценной жизнью с соблюдением определенных мер. При отсутствии строгого контроля и лечения, стадия инфицирования переходит в стадию СПИДа, которая неминуемо ведет к гибели. Человек на стадии СПИДа, из-за «иммунной беспомощности», может погибнуть от ряда инфекционных болезней.
Симптомами СПИДа является температура, постоянный озноб, легкая простужаемость, резкое похудение.
Чтобы предупредить СПИД необходимо соблюдать следующие правила;
— избегать прямого контакта с кровью неизвестного человека (зараженными так же могут быть лимфа, сперма, влагалищные выделения, грудное молоко и др.);
— избегать случайные половые связи;
— использовать презервативы;
— пользоваться одноразовыми шприцами;
— пользоваться личными бритвенными приборами, при этом не разрешать пользоваться своими.
Природным очагом СПИДа по мнению ученых считается Центральная Африка, а носителем вируса являются зеленые мартышки.
Грипп
Всем известный вирус гриппа не менее опасный, наряду с корью, гепатитом и полиомиелитом.
Грипп – болезнь, угрожающая человеческой жизни. В 1918-1919 годах весь земной шар трижды был охвачен волнами гриппа, во время которых погибли 20 млн человек. В США в зиму 1968-1969 годов 50 млн человек перенесли грипп, 70 тыс. из них скончались.
Наиболее распространенные вирусные инфекции, пути заражения и меры профилактики
Инфекция |
Пути заражения |
Меры профилактики |
Гепатит (А) |
«Болезнь грязных рук». | Мыть руки перед едой, овощи и фрукты — перед употреблением. При хранении продуктов соблюдать гигиенические требования |
СПИД |
Половой путь и через кровь | Исключение половых контактов с инфицированными |
Энцефалит |
Переносчики — кровососущие клещи | Исключить укусы клещей, особенно в природных очагах (хвойные леса) и в период активизации (март-май) |
КГЛ — конго-крымская геморрагическая лихорадка |
||
Бешенство |
При укусе больных животных | Исключать контакты с животными, не привитыми от бешенства. При контакте с подозрительным животным немедленно обращаться к врачу |
Грипп (ОРВИ) |
Воздушно-капельный | Марлевые повязки, влажная уборка, дезинфекция и проветривание помещений |
Корь, краснуха |
Воздушно, но не капельный | Соблюдать правила личной гигиены. Не вступать в контакт с инфицированными, применять ватно-марлевые повязки |
Ветряная оспа |
||
Ящур |
Болеют парнокопытные животные (коровы, козы, овцы) | Исключение контакта и срочное обращение к ветеринарному врачу при появлении характерных пятен на слизистых и коже животных |
Полиомиелит |
Чаще через грязные руки, воду, пищевые продукты. Возможно и воздушно-капельное заражение. | Предупредительные прививки |
|
Комплексные инфекции, либо инфекции, вызываемые как бактериями так и вирусами |
||
Пневмония |
Воздушно-капельный | Марлевые повязки, влажная уборка с дезинфицирующими средствами и проветривание помещений. |
Эпидемия — прогрессируемое во времени и пространстве инфекционное заболевание.
Пандемия — инфекционное заболевание захватывающее большие территории (мирового значения). В настоящее время к ряду таких заболеваний относится коронавирусная инфекция (COVID-19) вызванная коронавирусом (SARS-CoV-2).
Профилактика и методы борьбы с вирусами
Основные методы борьбы с вирусными инфекциями — профилактические прививки (вакцины), Ослабленные возбудители болезни, введенные в организм, позволяют выработать иммунитет. Благодаря вакцинам исчезло такое опасное вирусное заболевание, как оспа. Следует помнить, что без оболочки (капсида) вирусная НК сама попасть в клетку не может. Поэтому дезинфекция, вызывающая разрушение белков оболочки вируса (кипячение, хлорирование, обработка карболовой кислотой и др.), — эффективное профилактическое мероприятие. Наш организм тоже обладает защитными механизмами. Так, иммунный белок интерферон способен защищать организм человека от проникновения вирусов гриппа. В целях профилактики воздушно-капельных вирусных инфекций эффективно обрабатывать защитными средствами носовую полость.
Кроме того, сейчас создано несколько видов антивирусных препаратов как на основе неорганических веществ (ремантадин), так и на основе синтетических антител (виферон, биферон и т. д.). Несмотря на то что фармакология и вирусология ведут постоянные успешные исследования, не надо забывать, что соблюдение мер личной гигиены является надежным методом профилактики вирусных инфекций.
Происхождение вирусов
Ученые полагают, что вирусы и бактериофаги представляют собой обособившиеся генетические элементы клеток, подвергшиеся эволюции вместе с клеточными формами жизни.
Биологический русско-английский глоссарий
Вирус — virus |ˈvʌɪrəs|
Бактериофаг — bacteriophage |bakˈtɪərɪə(ʊ)feɪdʒ|
Капсид — capsid |ˈkapsɪd|
ДНК — DNA |ˌdi:ˌenˈeɪ|
РНК — RNA |ɑːrɛnˈeɪ|
Тест: Вирусы — неклеточные формы жизни
Инструкция: «Вам предлагаются задания с одним и несколькими правильными ответами из пяти и более предложенных».
Источники:
Изображения: freepik.com
Терминология на английском языке: wooordhunt.ru
Видеоматериалы: InternetUrok.ru
Вирусы — неклеточные формы жизни
Характеристика вирусов
Наряду с клеточной формой жизни существуют также и неклеточные ее формы — вирусы, вироиды и прионы. Вирусами (от лат. вира — яд) называют мельчайшие живые объекты, неспособные к проявлению каких-либо признаков жизни вне клеток. Факт их существования был доказан еще в 1892 году русским ученым Д. И. Ивановским, установившим, что болезнь растений табака — так называемая табачная мозаика — вызывается необычным возбудителем, который проходит через бактериальные фильтры, однако только в 1917 году Ф. Д’Эррель выделил первый вирус — бактериофаг. Вирусы изучает наука вирусология (от лат. вира — яд и греч. логос — слово, наука).
Вирусы существуют в двух формах: покоящейся, или внеклеточной, и воспроизводящейся, или внутриклеточной. Свободноживущих вирусов не существует, все они внутриклеточные паразиты на генетическом уровне.
В наше время известно уже около 1 000 вирусов, которые классифицируют по объектам поражения, форме и другим признакам, однако наиболее распространенной является классификация по особенностям химического состава и строения вирусов.
Особенности объектов поражения предопределяют подразделение вирусов на две большие группы: собственно вирусы и бактериофаги. Первые являются паразитами эукариотических клеток (животных, растений и грибов), а вторые — только клеток бактерий.
В отличие от клеточных организмов, вирусы состоят только из органических веществ — в основном нуклеиновых кислот и белка, однако часть вирусов содержит также липиды и углеводы.
Все вирусы условно делят на простые и сложные. Простые вирусы состоят из нуклеиновой кислоты и белковой оболочки — капсида. Капсид не монолитен, он собран из субъединиц белка — капсомеров. У сложных вирусов капсид покрыт липопротеиновой мембраной — суперкапсидом, в состав которого входят также гликопротеины и неструктурные белки-ферменты.
Несмотря на принадлежность к простым вирусам, наиболее сложное строение имеют вирусы бактерий — бактериофаги (от греч. бактерион — палочка и фагос — пожиратель), у которых выделяют головку и отросток, или «хвост». Головка бактериофага образована белковым капсидом и заключенной в нее нуклеиновой кислотой. В хвосте различают белковый чехол и спрятанный внутри него полый стержень. В нижней части стержня имеется специальная пластинка с шипами и нитями, ответственными за взаимодействие бактериофага с поверхностью клетки.
В отличие от клеточных форм жизни, у которых имеется и ДНК, и РНК, в вирусах присутствует только один вид нуклеиновой кислоты (либо ДНК, либо РНК), поэтому их делят на ДНК- (вирусы оспы, простого герпеса, аденовирусы, некоторые вирусы гепатита и бактериофаги) и РНК-содержащие вирусы (вирусы табачной мозаики, ВИЧ, энцефалита, кори, краснухи, бешенства, гриппа, остальные вирусы гепатита, бактериофаги и др.). У вирусов ДНК может быть представлена одноцепочечной молекулой, а РНК — двухцепочечной.
Так как вирусы лишены органоидов движения, заражение происходит при непосредственном контакте вируса с клеткой. В основном это происходит воздушно-капельным путем (грипп), через пищеварительную систему (гепатиты), кровь (ВИЧ) или переносчика (вирус энцефалита).
Непосредственно в клетку вирусы могут попадать случайно, с жидкостью, поглощаемой путем пиноцитоза, однако чаще их проникновению предшествует контакт с мембраной клетки-хозяина, в результате которого нуклеиновая кислота вируса или вся вирусная частица оказывается в цитоплазме. Большинство вирусов проникает не в любую клетку организма-хозяина, а в строго определенную, например, вирусы гепатита поражают клетки печени, а вирусы гриппа — клетки слизистой оболочки верхних дыхательных путей, так как они способны взаимодействовать со специфическими белками-рецепторами на поверхности мембраны клетки-хозяина, которые отсутствуют в других клетках.
В связи с тем, что у растений, бактерий и грибов клетки имеют прочные клеточные стенки, у вирусов, поражающих эти организмы, сформировались соответствующие приспособления к проникновению. Так, бактериофаги после взаимодействия с поверхностью клетки-хозяина «прокалывают» ее своим стержнем и вводят в цитоплазму клетки-хозяина нуклеиновую кислоту. У грибов заражение происходит в основном при повреждении клеточных стенок, у растений возможен как вышеупомянутый путь, так и проникновение вируса по плазмодесмам.
После проникновения в клетку происходит «раздевание» вируса, то есть утрата капсида. Дальнейшие события зависят от характера нуклеиновой кислоты вируса: ДНК-содержащие вирусы встраивают свою ДНК в геном клетки-хозяина (бактериофаги), а на РНК либо сначала синтезируется ДНК, которая затем встраивается в геном клетки-хозяина (ВИЧ), либо на ней может непосредственно происходить синтез белка (вирус гриппа). Воспроизведение нуклеиновой кислоты вируса и синтез белков капсида с использованием белоксинтезирующего аппарата клетки являются обязательными компонентами вирусной инфекции, после чего происходят самосборка вирусных частиц и их выход из клетки. Вирусные частицы в одних случаях покидают клетку, постепенно отпочковываясь от нее, а в других случаях происходит микровзрыв, сопровождающийся гибелью клетки.
Вирусы не только угнетают синтез собственных макромолекул в клетке, но и способны вызывать повреждение клеточных структур, особенно во время массового выхода из клетки. Это приводит, например, к массовой гибели промышленных культур молочнокислых бактерий в случае поражения некоторыми бактериофагами, нарушения иммунитета вследствие уничтожения ВИЧ Т4-лимфоцитов, представляющих собой одно из центральных звеньев защитных сил организма, к многочисленным кровоизлияниям и гибели человека в результате заражения вирусом Эбола, к перерождению клетки и образованию раковой опухоли и т. д.
Несмотря на то, что проникшие в клетку вирусы часто быстро подавляют ее системы репарации и вызывают гибель, вероятен также и иной сценарий развития событий — активация защитных сил организма, которая связана с синтезом противовирусных белков, например интерферона и иммуноглобулинов. При этом размножение вируса прерывается, новые вирусные частицы не образуются, а остатки вируса выводятся из клетки.
Происхождение вирусов не совсем ясно, однако полагают, что вирусы и бактериофаги — это обособившиеся генетические элементы клеток (например, плазмиды бактерий), которые эволюционировали вместе с клеточными формами жизни. Существуют также гипотезы упрощения прокариотических организмов вследствие паразитирования, доклеточного происхождения вирусов и занесения их из космоса.
Вирусы вызывают многочисленные заболевания человека, животных и растений. У растений это мозаичность табака и тюльпанов, у человека — грипп, краснуха, корь, СПИД и др. В истории человечества вирусы черной оспы, «испанки», а теперь и ВИЧ унесли жизни сотен миллионов человек. Однако инфицирование способно и повышать устойчивость организма к разнообразным возбудителям заболеваний (иммунитет), и таким образом способствовать их эволюционному прогрессу. Кроме того, вирусы способны «прихватывать» части генетической информации клетки-хозяина и переносить их следующей жертве, обеспечивая тем самым так называемый горизонтальный перенос генов, образование мутаций и, в конце концов, поставку материала для процесса эволюции.
В наше время вирусы широко используют в изучении строения и функций генетического аппарата, а также принципов и механизмов реализации наследственной информации, они применяются как инструмент генетической инженерии и биологической борьбы с возбудителями некоторых заболеваний растений, грибов, животных и человека.
Заболевание СПИД и ВИЧ-инфекция
ВИЧ (вирус иммунодефицита человека) был обнаружен только в начале 80-х годов ХХ века, однако скорость распространения вызываемого им заболевания и невозможность излечения на данном этапе развития медицины заставляют уделять ему повышенное внимание. В 2008 году Ф. Барре-Синусси и Л. Монтанье за исследование ВИЧ была присуждена Нобелевская премия в области физиологии и медицины.
ВИЧ — сложный РНК-содержащий вирус, который поражает главным образом Т4-лимфоциты, координирующие работу всей иммунной системы. На РНК вируса при помощи фермента РНК-зависимой ДНК-полимеразы (обратной транскриптазы) синтезируется ДНК, которая встраивается в геном клетки-хозяина, превращается в провирус и «затаивается» на неопределенное время. Впоследствии с этого участка ДНК начинается считывание информации о вирусной РНК и белках, которые собираются в вирусные частицы и практически одновременно покидают ее, обрекая на гибель. Вирусные частицы поражают все новые клетки и приводят к снижению иммунитета.
ВИЧ-инфекция имеет несколько стадий, при этом длительный период человек может быть носителем заболевания и заражать других людей, однако сколько бы ни длился этот период, все равно наступает последняя стадия, которая называется синдромом приобретенного иммунодефицита, или СПИДом.
Заболевание характеризуется снижением, а затем и полной потерей иммунитета организма ко всем возбудителям заболеваний. Признаками СПИДа являются хроническое поражение слизистых оболочек полости рта и кожи возбудителями вирусных и грибковых заболеваний (герпесом, дрожжевыми грибами и т. д.), тяжелая пневмония и другие СПИДассоциированные заболевания.
ВИЧ передается половым путем, через кровь и другие жидкости организма, но не передается через рукопожатия и бытовые предметы. В первое время в нашей стране инфицирование ВИЧ чаще было сопряжено с неразборчивыми половыми контактами, особенно гомосексуальными, инъекционной наркоманией, переливанием зараженной крови, в настоящее же время эпидемия вышла за пределы групп риска и быстро распространяется на другие категории населения.
Основными средствами профилактики распространения ВИЧ-инфекции являются использование презервативов, разборчивость в половых связях и отказ от употребления наркотиков.
Меры профилактики распространения вирусных заболеваний
Основным средством профилактики вирусных заболеваний у человека является ношение марлевых повязок при контакте с больными заболеваниями дыхательных путей, мытье рук, овощей и фруктов, протравливание мест обитания переносчиков вирусных заболеваний, вакцинация от клещевого энцефалита, стерилизация медицинских инструментов в лечебных учреждениях и др. Во избежание заражения ВИЧ следует также отказаться от употребления алкоголя, наркотиков, иметь единственного полового партнера, использовать индивидуальные средства защиты при половых контактах и т. д.
Вироиды
Вироиды (от лат. вирус — яд и греч. эйдос — форма, вид) — это мельчайшие возбудители болезней растений, в состав которых входит только низкомолекулярная РНК.
Их нуклеиновая кислота, вероятно, не кодирует собственные белки, а только воспроизводится в клетках растения-хозяина, используя ее ферментные системы. Нередко она может также разрезать ДНК клетки-хозяина на несколько частей, обрекая тем самым клетку и растение в целом на гибель. Так, несколько лет назад вироиды вызвали гибель миллионов кокосовых пальм на Филиппинах.
Прионы
Прионы (сокр. англ. proteinaceous infectious и —on) — это небольшие инфекционные агенты белковой природы, имеющие форму нити или кристалла.
Такие же по составу белки имеются и в нормальной клетке, однако прионы обладают особой третичной структурой. Попадая в организм с пищей, они помогают соответствующим «нормальным » белкам приобретать свойственную самим прионам структуру, что приводит к накоплению «ненормальных» белков и дефициту нормальных. Естественно, что это вызывает нарушения функций тканей и органов, в особенности центральной нервной системы, и развитие неизлечимых в настоящий момент заболеваний: «коровьего бешенства», болезни Крейтцфельдта – Якоба, куру и др.
Царство бактерий, строение, жизнедеятельность, размножение, роль в природе.
Бактерии — возбудители заболеваний растений, животных, человека. Профилактика
заболеваний, вызываемых бактериями
Царство бактерий
Бактерии — типичные прокариоты, представленные в основном одноклеточными и колониальными, реже многоклеточными формами. Среди них есть как автотрофы, так и гетеротрофы. Бактерии появились на Земле около 3,5 млрд лет назад и сыграли ключевую роль в преобразовании атмосферы и литосферы планеты. Обитают они во всех средах, от ледниковой минусовой температуры до кипящих источников, их находят даже на метеоритах, упавших на Землю, в атмосфере над ее поверхностью и в океанских глубинах. В настоящее время известно более 100 000 видов бактерий, однако только около 3000 из них изучены в той или иной степени. Изучением бактерий занимается наука бактериология, являющаяся разделом микробиологии. Впервые бактерии были описаны в XVII веке выдающимся микроскопистом А. ван Левенгуком.
Строение бактерий
Средние размеры клетки бактерий составляют 0,5–10 мкм. Бактериальная клетка имеет типичное для прокариот строение: кольцевая молекула ДНК, или хромосома бактерий, не отделена от цитоплазмы мембраной, а располагается в особом ее участке — нуклеоиде. Хромосома может быть не единственной молекулой ДНК в клетке — дополнительные маленькие кольцевые молекулы ДНК, способные встраиваться в хромосому, называются плазмидами. Плазмиды могут нести гены болезнетворности или устойчивости к антибиотикам.
Органоиды бактерий представлены в основном рибосомами, на которых происходит синтез белков. Все ферменты этих организмов находятся либо в цитоплазме, либо на немногочисленных мембранах, например, впячивании плазмалеммы — мезосоме.
Запасные вещества бактерий чаще всего откладываются в виде зерен крахмала или гликогена, капель жира и гранул волютина. У ряда бактерий, особенно у синезеленых водорослей, клетки содержат также вакуоли с белковыми оболочками, выполняющие функцию связывания атмосферного азота.
Так как многие бактерии подвижны, они имеют органоиды движения — жгутики. Кроме того, у них могут быть другие образования — ворсинки, служащие для прикрепления к субстрату или обмена наследственной информацией.
Как и эукариотические клетки, клетка бактерий окружена плазмалеммой, поверх которой чаще всего расположены клеточная стенка и капсула или облако слизи. Основу клеточной стенки большинства бактерий составляет сложное органическое вещество — муреин, цианобактерии имеют целлюлозные клеточные стенки. Муреин расщепляется компонентом слюны человека — лизоцимом, на чем и основывается его бактерицидное действие.
Капсула бактерий представляет собой уплотненный слой слизи, тогда как облако не имеет четко очерченных границ. Бактериальная слизь в основном имеет углеводную природу.
Компоненты поверхностного аппарата выполняют целый ряд функций: защищают бактериальную клетку от воздействия факторов окружающей среды, в том числе от проникновения бактериофагов, придают ей форму, помогают удерживать воду и принимают участие в транспорте веществ, служат резервуаром питательных веществ, объединяют клетки в колонии и цепочки, а также обеспечивают их прикрепление к субстрату.
Некоторые бактерии не образуют ни клеточной стенки, ни капсулы, тогда как другие утратили их в результате воздействия антибиотиков и факторов окружающей среды.
В зависимости от формы клетки бактерии делят на кокки, бациллы, вибрионы, спириллы и спирохеты. Кокки — это бактерии сферической формы, бациллы — палочковидной, спириллы — спиральной, вибрионы имеют вид запятой, тогда как спирохетами называют тонкие, длинные и извитые бактерии, способные к движению. Отдельные сферические бактерии называются микрококками, их группы по две — диплококками, гроздевидные скопления — стафилококками, а вытянутые цепочки — стрептококками. Эти морфологические особенности учитываются в классификации бактерий.
Большинство бактерий, вызывающих заболевания человека, имеют палочковидную форму, например дизентерийная, ботулиническая, дифтерийная, чумная, сибиреязвенная и столбнячная палочки, палочка Коха (туберкулез) и сальмонеллы (сальмонеллез и брюшной тиф). Реже это могут быть вибрионы, как хеликобактерии (язва желудка и двенадцатиперстной кишки) и холерный вибрион, а также спирохеты (сифилис) или диплококки (гонорея).
Если настоящие бактерии представлены одиночными клетками или колониальными формами, то среди цианобактерий (синезеленых водорослей) встречаются также многоклеточные формы, у которых клетки могут различаться по строению и выполняемым функциям. Так, у водоросли анабены среди вегетативных клеток встречаются и большие по размерам клетки — гетероцисты, имеющие общий чехол со всеми остальными клетками. Гетероцисты выполняют функции связывания атмосферного азота и вегетативного размножения, так как именно по этим клеткам происходит разрыв нити водоросли. Цианобактерии содержат хлорофилл и другие пигменты фотосинтеза (каротиноиды и фикобилины), что обусловливает их окраску. К ним принадлежат носток, анабена, осциллятория и др. Особенности строения и процессов жизнедеятельности синезеленых водорослей способствовали их выделению в отдельное подцарство цианобактерий (синезеленых водорослей), тогда как остальные представители царства относятся к подцарству бактерий.
Современная классификация бактерий учитывает не только морфологические их особенности, но и строение их клеточной стенки и процессы жизнедеятельности. По этим критериям бактерии предлагают разделить на два царства: археи и бактерии. Археи составляют сравнительно малоизученную группу прокариотических организмов, одни из которых обитают в экстремальных условиях среды, например в горячих гейзерах и сильно засоленных водоемах, а другие способны выделять метан в процессе жизнедеятельности. Археи присутствуют и в кишечнике человека, где синтезируют витамин В12. По организации наследственной информации и ряду других признаков археи ближе к эукариотическим организмам, чем бактерии.
Жизнедеятельность бактерий
Бактериям присущи все признаки живого, в том числе обмен веществ и превращения энергии, способность к самовоспроизведению и др. По способу питания бактерии относят к гетеротрофам и автотрофам. Среди гетеротрофных бактерий есть сапротрофы, паразиты, мутуалисты и даже хищники. Большинство бактерий поглощают пищу в растворенном виде из-за наличия клеточной стенки, а не заглатывают ее.
Сапротрофы обеспечивают расщепление органических веществ до минеральных, способствуя круговороту веществ в природе. Паразитические бактерии вызывают многочисленные заболевания, например чуму, холеру, туберкулез, пневмонию и другие. Мутуалистами являются бактерии кожи и слизистых оболочек человека, а также кишечника. Они не только защищают человека от других болезнетворных бактерий, но и могут синтезировать витамины, которые не образуются в организме человека. Следует отметить, что попадание мутуалистических бактерий в несвойственные им места приводит к развитию воспалительных процессов, например, стафилококк эпидермальный, в норме обитающий на нашей коже, может вызвать цистит, а стафилококк золотистый со слизистых оболочек — образование нарывов на месте ранок.
Не менее важен симбиоз клубеньковых бактерий с корнями растений. Эти бактерии связывают атмосферный азот в доступной для растений форме, а взамен получают от растений воду и органические вещества.
Автотрофные бактерии получают энергию за счет фотосинтеза или хемосинтеза. Значительная часть фотосинтезирующих бактерий относится к цианобактериям, или синезеленым водорослям, которые представлены свободноживущими формами, компонентами лишайников и мутуалистами, как синезеленая водоросль анабена, образующая симбиоз с водным папоротником азоллой.
Среди автотрофных бактерий, не относящихся к цианобактериям, можно найти как фототрофов, так и хемотрофов. Последние относятся к серо-, железо-, нитрифицирующим и водородным бактериям.
По потребности в кислороде бактерии делят на анаэробов (не нуждающихся в кислороде) и аэробов (требующих кислорода для своей жизнедеятельности). Соотношение этих форм бактерий зависит от особенностей среды обитания.
При неблагоприятных условиях бактерии образуют споры и цисты, имеющие плотные капсулы. Споры способны находиться в неактивном состоянии в течение многих лет (например, споры сибирской язвы — свыше 30 лет), однако при благоприятных условиях «спящая» бактерия возобновляет свою жизнедеятельность.
Размножение бактерий
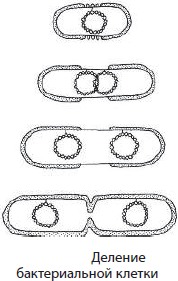
Бактерии размножаются в основном делением клетки надвое, которому предшествует удвоение ДНК. При благоприятных условиях среды бактерии способны делиться каждые 20–30 мин. Нетрудно подсчитать, какое количество бактерий дает одна-единственная материнская клетка в течение суток.
Вегетативное размножение характерно только для многоклеточных цианобактерий, у которых образуются и отделяются специальные нити для размножения, однако нити могут разрываться и по гетероцистам.
У бактерий наблюдаются также процессы одностороннего переноса наследственной информации. В одних случаях происходит передача плазмиды от одной бактерии к другой с помощью специальной ворсинки — это конъюгация. В других случаях определенный участок ДНК от одной зараженной клетки к другой переносит бактериофаг — это трансдукция. Однако одним из наиболее интересных способов передачи наследственной информации является трансформация, при которой клетка не только поглощает ДНК другой бактерии из окружающей среды, но и встраивает ее в собственную хромосому, приобретая закодированные признаки. Открытие явления трансформации бактерий-пневмококков Ф. Гриффитом в 1928 году позволило вскоре установить функции нуклеиновых кислот как основного носителя наследственной информации, а в наше время широко используется в генетике бактерий и генной инженерии.
Роль бактерий в природе
В 1 г сельскохозяйственных почв содержится до 2,5 млрд бактерий, несколько меньше их в воде и в воздухе, до 2 кг этих организмов могут находиться на коже, слизистых оболочках и в кишечнике человека, тогда как не связанные напрямую с окружающей средой органы практически лишены бактериальной микрофлоры.
Бактерии играют исключительную роль в круговороте углерода, кислорода, водорода, азота, фосфора, серы, кальция и других элементов. Они возвращают в почву неорганические вещества (совместно с грибами), разлагая органические, в результате их деятельности образовались кислород земной атмосферы, залежи железной руды, карбонатов и других полезных ископаемых, они связывают азот в почве, образуя симбиоз с корнями бобовых и других растений (клубеньковые бактерии), переводя его в доступную для растений форму. Бактерии принимают активное участие и в биологической очистке водоемов. В отсутствие этих организмов существенно замедляются процессы почвообразования.
Бактерии нашли широкое применение в хозяйственной деятельности человека. Так, молочнокислые бактерии используются не только в производстве молочнокислых продуктов, но и в процессе квашения овощей и силосования кормов. Кишечная палочка с помощью методов генной инженерии «освоила» производство инсулина, она также является индикатором загрязнения воды. Другие бактерии благодаря способности концентрировать металлы используются для их добычи из бедных руд и отвалов.
Вред, наносимый бактериями, не менее значителен. Так, массовое размножение цианобактерий приводит к «цветению» воды, при этом в воду выделяется значительное количество токсических веществ, которые способны вызвать гибель самих синезеленых водорослей и других организмов. При нарушении санитарных норм бактерии портят продукты питания и загрязняют лекарственные препараты, что может приводить к негативным последствиям для здоровья человека, не говоря уже о том, что сами по себе многие бактерии являются болезнетворными организмами.
Бактерии — возбудители заболеваний растений, животных, человека
Паразитические бактерии вызывают заболевания человека, животных и растений, называемые бактериозами. У растений широко распространены такие бактериальные заболевания, как кольцевая гниль и парша картофеля, бактериальный ожог, рак и увядание томатов и др., которые наносят значительный вред сельскому хозяйству.
Животные не менее растений подвержены бактериальным заболеваниям, например чуме, туляремии, сальмонеллезу, сибирской язве, бруцеллезу и др. Больные животные представляют опасность и для человека, так как при контакте с ними или через переносчика (блох, клещей, комаров и др.) может происходить инфицирование. Чаще всего источниками инфекции являются грызуны, домашний скот и птица. В связи с этим необходимо строго придерживаться гигиенических норм и правил при контакте с животными.
Заражение человека возбудителями бактериальных инфекций происходит через пищеварительную систему, органы дыхания, при укусах переносчиков, а также через слизистые оболочки и повреждения кожи. В связи с этим бактериозы делят на кишечные (язва желудка, холера, дизентерия, сальмонеллез, брюшной тиф, ботулизм), респираторные (дифтерия, коклюш, туберкулез), кровяные инфекции (чума, сыпной тиф) и инфекции наружных покровов (сибирская язва, столбняк, сифилис и гонорея).
Механизм болезнетворного влияния бактерий в корне отличается от такового у вирусов, поскольку бактерии выделяют токсические вещества, оказывающие комплексное неблагоприятное воздействие на организм. При этом они могут даже не размножаться в тканях, как при столбняке и ботулизме. Последний вызывается ботулиническим токсином, который вырабатывается бактерией рода клостридиум в неправильно приготовленных и длительное время хранившихся консервах.
К категории особо опасных инфекций бактериальной природы относятся чума, бруцеллез, сибирская язва, сап и холера, так как их возбудители способны заразить почти каждого человека, протекают в тяжелой форме и вызывают как эпидемии, так и пандемии.
Несмотря на четкую организацию санитарно-эпидемиологической службы в Российской Федерации и других странах мира, постоянно сохраняется опасность возникновения эпидемий чумы и холеры, в последнее время вызывают также тревогу и темпы распространения туберкулеза.
Профилактика заболеваний, вызываемых бактериями
Основным средством профилактики бактериальных заболеваний у человека является повышение санитарной культуры населения, своевременное выявление и лечение больных, ношение марлевых повязок при контакте с больными, мытье рук, овощей и фруктов, протравливание мест обитания переносчиков соответствующих заболеваний, вакцинация и др. Например, если профилактика дифтерии заключается в периодической вакцинации, то от туберкулеза вакцины не существует, поэтому требуется своевременное выявление заболевших. Для этого в детском и подростковом возрасте делают пробу Манту, а взрослые обязаны ежегодно проходить флюорографическое исследование. При подозрении на туберкулез берутся дополнительные анализы, по результатам которых ставится окончательный диагноз. Поскольку туберкулезная палочка может поражать не только легкие, но и другие внутренние органы, а в последнее время наблюдается рост заболеваемости туберкулезом и выявлены чрезвычайно опасные его формы, требуется изоляция больных, соблюдение гигиенического режима и длительное лечение в специальных лечебницах и санаториях.
Для лечения бактериальных заболеваний чаще всего применяются антибиотики — сложные химические вещества, выделяемые микроорганизмами и способные подавлять развитие других микроорганизмов и раковых клеток или даже убивать их. Первый пригодный для клинического применения антибиотик — пенициллин — был получен в 1929 году А. Флемингом. Во время Великой Отечественной войны благодаря применению пенициллина были спасены жизни многих солдат. В настоящее время антибиотики применяют для лечения большого количества заболеваний человека, животных и растений, однако длительное применение приводит к появлению устойчивых к ним форм микроорганизмов. Поэтому во всем мире поднимается вопрос об отказе от антибиотиков как от лекарственного средства. Антибиотики применяются также в животноводстве для повышения продуктивности и для исследования тонких механизмов жизнедеятельности, поскольку они способны прерывать некоторые процессы, например образование клеточной стенки или синтез белка.
Бактериофаги, или фаги, — самые распространенные и вместе с тем самые загадочные обитатели нашей планеты. Их открыли в начале прошлого века, и в их лице многие ученые увидели спасительное средство от бактериальных инфекций, которого все так долго ждали. Но вскоре началась эра антибиотиков, и о фагах на время забыли. Очередная волна интереса к бактериофагам поднялась на пике развития молекулярной биологии — они стали модельными организмами, которые помогли заглянуть в самую суть жизни. Новое рождение биология фагов переживает прямо на наших глазах. С одной стороны, возросший интерес к ним обусловлен остро вставшей проблемой антибиотикорезистентности. В то же время, стало понятно, что вирусы бактерий — не просто паразиты, но и симбионты, регуляторы, которые образуют глобальную сеть передачи генетической информации в масштабах биосферы. Бактериофаги играют важную роль в биологии вездесущих прокариот, а те, в свою очередь, формируют условия, в которых обитают все эукариотические организмы, включая человека. Этой статьей «Биомолекула» начинает cпецпроект об увлекательном мире бактериофагов.
Бактериофаги
Партнер спецпроекта — НПЦ «Микромир» — производитель препаратов с бактериофагами для применения в медицине и ветеринарии.
Бактериофаги — это вирусы, заражающие бактериальные клетки. Они составляют наиболее многочисленную и эволюционно древнюю группу вирусов в биосфере Земли. Бактериофаги играют важную роль в контроле численности микробных популяций и в горизонтальном переносе бактериальных генов, выступая в качестве векторных систем.
В спецпроекте мы дадим общую информацию о бактериофагах, истории их изучения, использовании в лаборатории, попытках применения в медицине и ветеринарии и возможных будущих применениях.
Первые знакомства и начало науки о фагах
С миром микроорганизмов заочно были знакомы еще самые первые люди. Наши далекие предки наблюдали результаты жизнедеятельности этих невидимых для невооруженного глаза «соседей» повсюду: бактерии участвуют в формировании почвы и тем самым помогают выращивать урожай; делают несвежими продукты или, наоборот, помогают некоторые из них производить; вызывают болезни. Конечно же, поначалу никто не знал, что за это ответственны микроскопические существа. Коллективные усилия бактерий представали перед первобытными людьми то как благодать богов, то как проделки демонов.
Первым человечество познакомил с миром микроорганизмов нидерландский оптик-самоучка и исследователь-микроскопист Антони ван Левенгук в конце XVII века. Крохотные клетки, которые он увидел под микроскопом, произвели настоящий фурор [1]. На них интересно было смотреть, но пока еще никто не понимал, насколько важную роль они играют для человека и всей окружающей среды (рис. 1).
Рисунок 1. На пути к открытию бактериофагов: основные вехи. Конец XVII века. Антони ван Левенгук впервые увидел живые клетки под микроскопом [1]. 1892 г. Димитрий Иосифович Ивановский открыл первый вирус — вирус табачной мозаики. 1898 г. Британский химик и микробиолог Эрнст Ханбери Ганкин сообщил о литическом действии воды из рек Ганг и Джум, пропущенной через бактериальные фильтры, на возбудителей холеры. Считал, что это связано с летучим бактерицидным веществом. 1898 г. Российский и советский врач, микробиолог и эпидемиолог Николай Федорович Гамалея сообщил о «литическом ферменте», выделенном из лизата культур Baclillus anthracis. Вероятно, на самом деле это были бактериофаги. 1915 г. Фредерик Уильям Туорт впервые наблюдал лизис бактерий фагами. 1917 г. Повторное открытие вирусов бактерий и введение термина «бактериофаг» Феликсом д’Эреллем. 1940-е гг. Получены первые изображения бактериофагов под электронным микроскопом. Ученые убедились — фаги существуют!
Прошло еще почти два столетия, и стала зарождаться настоящая микробиология. Толчок дали работы двух великих ученых — Луи Пастера и Роберта Коха. К началу XX века многие микроорганизмы уже были изучены, открыты возбудители инфекций, против некоторых из них разработаны вакцины, лечебные токсиннейтрализующие сыворотки. Появилась полноценная бактериологическая диагностика.
В конце XIX века открыли и вирусы эукариот. Первым стал вирус табачной мозаики — его в 1892 году обнаружил русский физиолог и микробиолог Димитрий Иосифович Ивановский [2–4].
Казалось бы, мир паразитов изучен до самой последней границы, до самых простейших существ. Но ученых еще ожидал сюрприз, впоследствии положивший начало новому большому разделу биологии. Этим сюрпризом стали суперпаразиты — фаги, вирусы, способные поражать бактерий. Это оказалось настолько неожиданным, что в существование таких «молекулярных роботов» до того, как их удалось разглядеть в электронный микроскоп, отказывались верить некоторые маститые ученые и даже один Нобелевский лауреат.
Кстати, о паразитах на нашем сайте есть целая серия материалов. Читайте статьи «Его величество паразит» [5], «Манипулирование. I. Паразитное манипулирование» [6] и «Паразит паразиту враг» [7].
Как и многие научные открытия, первое знакомство ученых с бактериофагами произошло благодаря случайности. Британский исследователь Фредерик Уильям Туорт (рис. 1, 2а) загорелся идеей вырастить на бесклеточной питательной среде вирус осповакцины (в то время не знали, что с вирусами так не получится). В 1913 году он решил культивировать вирус на бесклеточных средах, для чего использовал осповакцину, по случайности контаминированную стафилококками. Вирусы осповакцины в чашках Петри так и не появились, но Туорт заметил другой загадочный эффект: некоторые колонии стафилококков получились полупрозрачными. В них не было бактерий, но присутствовали какие-то мелкие частицы — видимо, остатки клеток. Когда Туорт переносил стекловидные колонии на свежие, те также превращались в «призраков». Британский ученый так и не понял, что же случилось, он лишь выдвинул три гипотезы. Возможно, стафилококков разрушил некий вирус; либо фермент, выделившийся из погибших клеток; либо какой-то другой «живой» фермент, способный воспроизводить сам себя. Как мы теперь знаем, одна из этих догадок попала точно в цель. Туорт первым предположил, что это вирусы, но, как и его современники, не понимал, что они собой представляют и как «работают» [8].
Второе открытие фагов совершил канадско-французский ученый Феликс д’Эрелль (рис. 2). В 1916 году в Париже он изучал вспышку дизентерии в драгунском эскадроне, стоявшем в Мезон Лавите. И снова, как у Туорта, первым шагом стало ошибочное предположение. Д’Эрелль считал, что диарею вызывает бактерия в сочетании с вирусом, и что они усиливают друг друга. Чтобы проверить эту догадку, ученый получил фильтраты фекалий больных и добавлял их в растущие культуры возбудителя. В результате фильтраты фекалий выздоравливающих пациентов разрушали (лизировали) культуры. А когда этот лизат высевали на агар вместе с новыми культурами, на бактериальных газонах появлялись прозрачные кружки, которые д’Эрелль назвал taches vierges — «чистые пятна» (сейчас их называют бляшками). В отличие от своего предшественника, д’Эрелль сразу понял, в чем дело, и объявил, что открыл вирусы бактерий. Он и назвал их бактериофагами (выбрать «имя» д’Эреллю помогла супруга) [2], [8], [9].
Рисунок 2а. Первооткрыватель бактериофагов Фредерик Уильям Туорт. Он первым увидел те самые бляшки на чашках Петри, но не смог однозначно объяснить, кто виновен в их возникновении.
Рисунок 2б. Феликс д’Эрелль — ученый, во второй раз открывший фагов, давший им название и заложивший основы фаготерапии.
Позже д’Эрелль пошел дальше и объявил фаги естественной защитной системой организма от бактериальных инфекций (в чем, к слову, отчасти оказался прав). В своих работах он критиковал ведущих иммунологов, чем очень уязвил бельгийского ученого Жюля Борде, получившего в 1919 году Нобелевскую премию за открытие системы комплемента. В ответ оскорбленный Борде заявил, что феномен, открытый самонадеянным французом, — всего лишь проявление аутолиза (когда бактериальные клетки разрушают сами себя своими же ферментами), и принялся доказывать свои идеи в экспериментах. Соперничество пошло только на пользу: оно помогло открыть некоторые важные свойства фагов. Все точки над i были расставлены в 1940 году, когда бактериофаги предстали перед учеными воочию, благодаря электронному микроскопу (рис. 1) [10].
Но это не конец истории, а только ее начало — благодаря фагам было сделано множество открытий в биологии и получена не одна Нобелевская премия. Подробнее об этом можно почитать в наших статьях «Пожиратели бактерий: убийцы в роли спасителей» [11] и «Модельные организмы: фаг лямбда» [12].
Знакомьтесь: фаги
Функционал бактериофага, как и любого вируса, незамысловат: найти подходящую клетку, проникнуть в нее, наплодить новые вирусные частицы, освободить их и отправить на поиски новой жертвы. В остальное время нужно лишь обеспечить надежную защиту для генетического материала. В этом плане все бактериофаги практически не различаются, поэтому и их структура организована по одному принципу, включая одни и те же основные компоненты:
- Генетический материал в виде нуклеиновой кислоты — ДНК или РНК.
- Капсула из белков, которая защищает нуклеиновую кислоту, как обшивка космического корабля обеспечивает защиту для экипажа. У бактериофагов это капсид, иногда — мембрана.
- Аппарат, обеспечивающий проникновение генетического материала в бактериальную клетку. Именно в этом компоненте встречаются наиболее заметные различия между разными видами фагов [9].
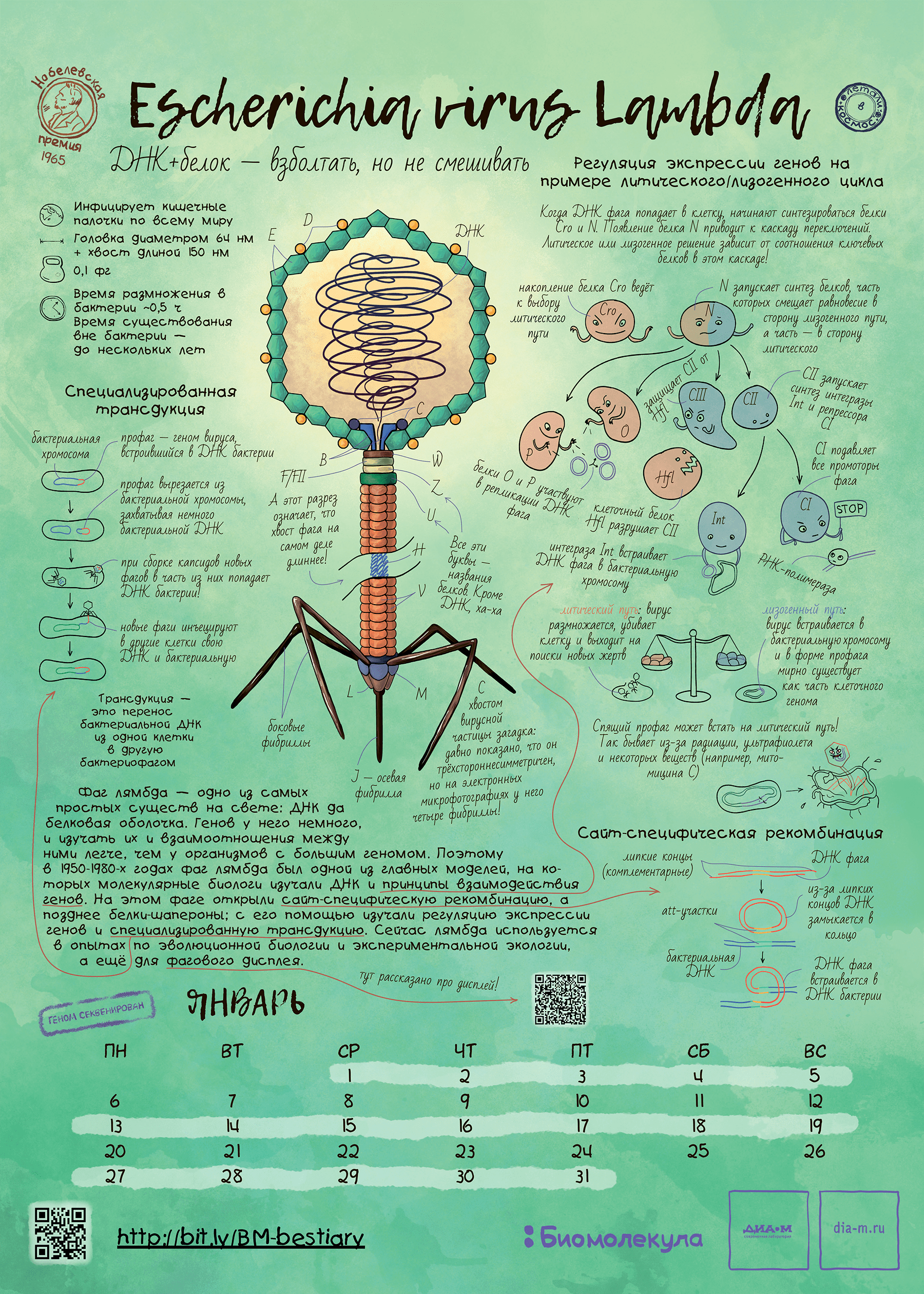
«Визитная карточка» большинства фагов — хвост. Такие фаги относятся к типу Uroviricota [3]. Это самые узнаваемые вирусы бактерий, внешне напоминающие инопланетный космический корабль. Например, так устроен фаг лямбда — модельный организм, который используют ученые по всему миру (рис. 3). В зависимости от типа хвоста, различают три морфологических варианта, (до недавнего времени они соответствовали таксономическим семействам) :
- Сифовирусы — с длинным несократимым хвостом. Это самая многочисленная группа, на нее приходится около 60% всех бактериофагов.
- Миовирусы — с длинным хвостом, который умеет сокращаться. На них приходится 25%.
- Подовирусы — с коротким несократимым хвостом, они составляют 15% [9], [13], [14].
На самом деле таксономия фагов намного сложнее и продолжает пересматриваться — последние значительные изменения (на момент написания этой статьи) произошли в 2020 году. Классификация в зависимости от внешнего вида имеет исторический смысл и в настоящее время применяется для удобства. А полную актуальную классификацию всех вирусов, включая фагов, можно найти на сайте Международного комитета по таксономии вирусов (ICTV).
Рисунок 3. Тут изображен не НЛО, а пример структуры хвостатого фага. А именно — фага лямбда, модельного организма, о котором мы рассказывали в статье «Модельные организмы: фаг лямбда» [12].
Вообще, классификация фагов довольно сложна, и в ней учитываются разные характеристики, такие как морфология, физико-химические свойства вириона, структура нуклеиновых кислот, геномные данные.
Откуда взялись фаги?
Свято место, как известно, пусто не бывает. Бактерии, хотя и являются простейшими организмами, устроены всё же достаточно сложно, чтобы в них можно было паразитировать кому-то еще более мелкому и примитивному. Фаги заняли эту нишу очень давно, вероятно, сразу после возникновения первых прокариот. Точную дату никто не назовет, ведь вирусы — не динозавры и костей не оставляют. До сих пор нет ответа и на другой вопрос, волнующий ученых: откуда взялись бактериофаги? На этот счет существует несколько гипотез [15]:
- Гипотеза коэволюции говорит о том, что предки нынешних вирусов возникли еще до прокариот, в составе так называемого РНК-мира. Ведь существуют же до сих пор вироиды (или вирусоподобные инфекционные агенты): они состоят из РНК и лишены белковой оболочки. Тем не менее такая РНК может и сама действовать как фермент: расщеплять и лигировать другие молекулы РНК, образовывать пептидные связи и даже собственные копии. Возможно, первой формой жизни на нашей планете была именно РНК, а с появлением прокариот она приспособилась к паразитическому образу жизни [16]. Мы рассказывали об этой гипотезе в статье «РНК у истоков жизни?» [17], а еще на нашем сайте есть научный комикс «РНК: начало (мир РНК)» [18].
- Гипотеза клеточного происхождения (прогрессивная гипотеза) гласит, что нуклеиновые кислоты вирусов и бактериофагов — это генетический материал, который «убежал» из клетки и начал жить своей «пиратской» жизнью. Структуры, чем-то напоминающие вирусы, есть и у эукариот — эгоистические генетические элементы (плазмиды, транспозоны и некоторые другие) [19], [20].
- Регрессивная гипотеза утверждает, что вирусы — это клетки, которым было лень самостоятельно обеспечивать свою жизнедеятельность и размножение. Они избавились от всего «лишнего» и стали паразитировать на своих собратьях. Такое упрощение структуры и функционала — распространенное явление в мире паразитов, в том числе в микромире. Например, известны такие «лайтовые бактерии», как риккетсии и хламидии, которые могут размножаться только внутри других клеток. О бактериях-карликах, способных проходить через фильтры, ранее считавшиеся непроницаемыми для клеток, можно почитать в нашей статье «Маленький, да удаленький: самые маленькие клетки» [21]. Может быть, это и есть то самое переходное звено между бактериями и фагами?
- Гипотеза о вирусах-прародителях. Все гипотезы, перечисленные выше, утверждают, что начало жизни на Земле дали клетки, и именно они были первыми. Вирусы либо появились позже, либо существовали изначально, но никак не связаны с первыми прокариотами, а лишь превратились в паразитов. Но некоторые ученые считают, что нашими первыми предками могли быть именно вирусы. Постепенно они усложнились, приобрели механизмы для синтеза мембран, клеточных стенок. Эта гипотеза считается наиболее сомнительной, ведь на данный момент не известно вирусов, которые могли бы размножаться без хозяев, и нет подтверждений, что такие вообще могли существовать. Тем не менее в 2012 году было продемонстрировано, что вирусы могут формировать структуры, напоминающие ядра, в клетках хозяев [22]. В 2020 году российские ученые провели эксперименты с заражением бактерий фагом phiKZ. Внутри клеток этот бактериофаг формирует псевдоядро, напоминающее настоящее , [23]. Подобные структуры не родственны ядрам эукариот, поэтому такие эксперименты вовсе не доказывают, что вирусы могли дать начало клеточным формам жизни. Тем не менее эта способность вирусов весьма интересна и дает почву для дальнейших исследований. Большой интерес для ученых представляют гигантские мимивирусы — есть мнение, что они могут оказаться переходным звеном между доклеточными и клеточными формами жизни [3], [15].
О том, как джамбо-фаги могут образовывать псевдоядра в клетках бактерий, можно почитать в нашей статье «Я в домике!”: бактериофаги, у которых есть ядра» [24].
Если вам интересно узнать больше о мимивирусах и об их врагах в вирусном мире — читайте наши статьи «Гиганты вирусного мира» [25] и «Паразит паразиту враг» [7].
Филогенез бактериофагов до сих пор таит множество загадок. Между разными представителями обнаруживаются определенные сходства и различия, которые помогают выстраивать эволюционные линии. Однако неизвестно, составляют ли все вирусы, или хотя бы все фаги, единую монофилетическую группу. Иными словами, есть ли у них у всех один предок, или же отдельные разновидности возникли параллельно независимо друг от друга [26].
Из нашей статьи «Вирусные геномы в системе эволюции» можно подробнее узнать о происхождении вирусов и их месте в общей модели эволюции [27].
Поиски родственных связей затрудняет одна особенность фагов: мозаицизм их генома. Он напоминает лоскутное одеяло: сшит из многочисленных модулей, каждый из которых обладает собственной эволюционной историей. Эти модули могут включать [28], [29]:
- набор генов, полностью ответственный за сборку определенной «части тела» фага, например, головки или хвоста;
- набор генов, кодирующих белки, необходимые для определенного процесса, например, удвоения ДНК;
- модули субгенного уровня, которые кодируют белковые домены или группу доменов, необходимые для выполнения определенной функции;
- мороны — независимые транскрипционные единицы, обычно состоящие из одного гена, кодирующего белок с «опциональной», дополнительной функцией в фаговом геноме [3].
Геном фагов «пестрый», потому что эволюционируют они не совсем так, как многоклеточные организмы. С одной стороны, у них, как и описано в учебниках школьной биологии, периодически возникают мутации: полезные закрепляются, вредные отбраковываются. Это так называемый вертикальный путь. Но у фагов есть еще и путь горизонтальный, и он очень активно работает. Это так называемый модульный механизм, связанный с латеральным переносом генов за счет различных видов рекомбинации. У бактерий этот механизм тоже работает, но не в такой степени [29–31].
Исследователи фагов традиционно делились на два лагеря. Одни утверждали, что эволюция бактериофагов в первую очередь происходит за счет модульного механизма. Противники были уверены, что, хотя модульный механизм и вносит существенный вклад, главным двигателем нужно признать мутации. Сегодня для всех очевидно, что оба механизма работают, вопрос только в том, насколько существенный вклад вносит каждый из них. Из-за этого и возникают сложности с изучением филогенеза фагов: ведь он пронизан густо переплетенными нитями.
Впрочем, со временем картина становится более четкой. Известно, что у бактериофагов-родственников (условно представителей одного рода и семейства) есть одинаковые гены, объединенные в консервативные кластеры. Тут изменения происходят в основном за счет точечных мутаций, а перестановки модулей наблюдаются редко. Эти участки называются кор-геномом. Они содержат консервативные гены, которые кодируют структурные белки вириона, ферменты, гены транскрипции и репликации. Существенные изменения тут чреваты: чтобы фаг остался жизнеспособным, их нужно компенсировать точечными мутациями. Время на возникновение этих мутаций есть только у умеренных фагов, пока профаг находится в безопасности внутри бактериальной клетки. Зато горизонтальный перенос часто происходит в периферическом геноме, где находятся вариабельные гены, преимущественно мороны [3], [32].
Изучение эволюции фагов важно не только само по себе. Ведь в большинстве случаев она протекает не изолированно, а в форме коэволюции с бактериями-хозяевами. Знание этих процессов важно для более эффективного применения фагов в медицине и других сферах, в изучении их влияния на экосистемы.
Бактерии и фаги: миллиарды лет вместе
Когда у ученых не было эффективных инструментов, чтобы подсчитывать число фагов в окружающей среде, считалось, что эти «инопланетяне» если и влияют на экосистемы, то весьма незначительно. Всё изменилось в 1980–1990-е годы, когда стали широко использовать методы прямого подсчета вирусных частиц в природных образцах, такие как электронная и эпифлуоресцентная микроскопии. Оказалось, что фаги буквально повсюду, и их примерно в 10 раз больше, чем бактерий. Фактически, это самые многочисленные обитатели нашей планеты.
Говоря о бактериофагах как о санитарах микромира, по аналогии с волками — санитарами леса, нужно отметить одно существенное отличие. Если вспомнить пищевые цепочки из школьного курса биологии, то в воображении сразу предстанет пирамида, где внизу травоядные, а у верхушки хищники. Последних меньше, и за счет этого они контролируют размеры популяции более многочисленных жертв, при этом и сами не оставаясь голодными. У фагов же с бактериями всё наоборот: «хищников» больше на порядок. Тем не менее система поддерживается в равновесии: прокариоты не подверглись тотальному геноциду, но и не стали поголовно устойчивыми к фагам.
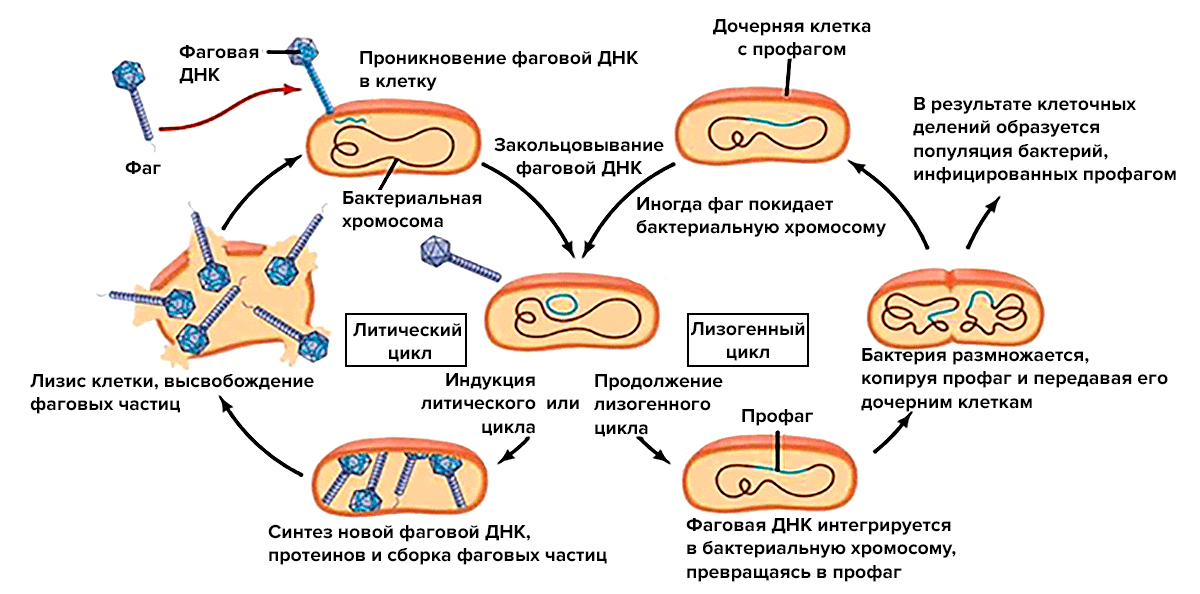
Чтобы понять, как фаги и чувствительные к ним бактерии стабильно сосуществуют, в первую очередь нужно поговорить о двух основных (но не единственных) жизненных циклах фагов (рис. 4):
- Литический цикл напоминает классические отношения «хищник—жертва». Фаг прикрепляется к бактериальной клетке с помощью специальных рецепторов и вводит внутрь свой генетический материал. Такая «зомбированная» бактерия превращается в фабрику по производству новых вирусных частиц. В конечном счете клетка разрушается, и новые фаги выходят во внешнюю среду, чтобы встретить новую жертву. Такие бактериофаги называются вирулентными.
- Лизогенный цикл больше похож на хроническую инфекцию (но этот термин тут не подойдет, для фагов он обозначает другое). Вирусная ДНК или РНК не спешит создавать свои копии и новые вирусные частицы. Такие фаги (они называются умеренными) могут длительно существовать в виде профага. Их ДНК встраивается в бактериальную хромосому или существует в виде плазмиды [14]. Бактерия «остается в живых», и профаг даже может наделять ее новыми полезными свойствами. Это может продолжаться очень долго, но однажды условия меняются, и запускается литический цикл [33–35].
Рисунок 4. Схематическое изображение литического и лизогенного циклов. В то время как одни клетки, инфицированные фагами, погибают, другие остаются живыми и даже получают некоторые новые полезные свойства. Но позже все-таки могут также погибнуть.
Если проанализировать виро́м (совокупность всех вирусов) разных сред, то окажется, что большая часть его населения представлена вирулентными фагами (по крайней мере, они обычно преобладают в воде). Теоретически эта орда должна массово атаковать бактерии и уничтожить их на корню. Но этого не происходит. Бактерии никогда не погибают полностью даже при большой концентрации фаговых частиц и процветают повсеместно. Дело в том, что они защищены с помощью целого ряда механизмов.
В течение миллиардов лет сосуществования бактерий и фагов происходило что-то вроде гонки вооружений. Прокариоты выработали целый арсенал методов защиты — своего рода иммунитет. Причем у бактерий в этой гонке есть преимущество: у них мутации, позволяющие защищаться от фагов, происходят чаще и проще. Бактериофаги в некоторой мере компенсируют это своей численностью [14].
На приобретение защитных мутаций бактериям требуется время, а для начала нужно как-то остаться в живых. Тут дела обстоят как с пандемией COVID-19: иммунитет человека может справиться с вирусом, но пока он «разгонится», вирус может справиться с организмом самого человека. Поэтому врачи рекомендуют меры профилактики: носить маски, избегать общественных мест, часто мыть руки, не подходить к больным людям и, конечно же, вакцинироваться. Бактерии успешно используют некоторые «убежища» (refuges), чтобы «прятаться» от фагов:
- Численное укрытие. В отличие от хищников животного мира, бактериофаги не умеют гоняться за жертвами. Они полностью во власти стихии: им остается только ждать, когда законы физики помогут им коснуться подходящей бактериальной клетки. Понятно, что, в целом, вероятность не очень высока, особенно в таких средах, как почва, или если концентрации бактерий и соответствующих им фагов в целом малы. Под лежачий камень вода, как известно, не течет.
- Пространственное укрытие. Некоторые исследователи называют его одним из самых важных механизмов защиты бактерий от встречи с фагами. Он предполагает изоляцию по крайней мере части чувствительных микроорганизмов. Например, бактерии часто строят «крепости» — биопленки. В качестве кирпичиков микроорганизмы используют собственные тела, а «цементом» служит слизь.
- Физико-химическое укрытие. Некоторые бактерии селятся в таких местах, где есть химические соединения или физические факторы, сильно снижающие способность фагов инфицировать клетки (а то и вовсе сводят ее на нет). Один из примеров такой среды — рубец жвачных животных.
- Физиологическое укрытие. Сами бактерии могут находиться в таком состоянии, которое совсем не способствует размножению и распространению фагов. Например, если микроорганизмам не хватает питательных веществ, и у них нет ресурсов, чтобы превратиться в «вирусную фабрику», фаги всё еще могут проникать в бактериальные клетки, но находятся в них в неактивном состоянии [34].
- «Укрытие за трупами». Единственные «органы чувств» фагов — белки, способные связываться с рецепторами на поверхности бактериальных клеток. Но вместо живой клетки им может попасться бактериальный дебрис (остатки разрушенных бактерий). Фаг необратимо с ним связывается и инактивируется [3], [36].
Санитары микромира
Если смешать вирулентные фаги с чувствительными к ним бактериями, последних тут же станет меньше. В самом деле, фаги — основные убийцы бактерий: на них приходится до 70% бактериальных смертей (в среднем — 15–30%). Кроме того, при хронической инфекции скорость размножения бактерий уменьшается, и это тоже влияет на их численность. Лучше всего все эти процессы изучены в морской воде.
Быстрее всего фаги размножаются в наиболее многочисленных и быстрорастущих популяциях бактерий. Это проявление принципа «убивай побеждающего» — kill the winner. Бактериофаги непрерывно работают как неутомимая и неподкупная антимонопольная служба. Как только популяция какого-нибудь микроорганизма начинает преобладать в экосистеме — среди ее членов немедленно разгорается эпидемия, приводящая к коллапсу. За счет этого никто не может окончательно победить в конкуренции, и поддерживается широкое биоразнообразие [37–39].
Уничтожая бактерий, фаги парадоксальным образом способствуют их размножению. Тут задействованы сложные механизмы, связанные с пищевыми цепочками. Например, в море, если фагов нет, и микроорганизмы идут на пищу зоопланктона, вся биомасса полностью переходит на следующий уровень пищевой цепочки. Бактериофаги же возвращают 99% клеточного содержимого в окружающую среду в растворенном виде. В итоге энергия и вещество остаются в распоряжении микроорганизмов. По некоторым данным, в результате лизиса клеток вирусами в мировой океан ежегодно поступает около трех гигатонн углерода. Вирусы сильно влияют на поток углерода, азота и других питательных веществ в окружающей среде [14], [40]. Также фаги влияют на фиксацию углекислого газа в морской воде и осадочных породах, способствуют высвобождению из микроорганизмов диметилсульфида — газа, который участвует в формировании облаков и влияет на интенсивность поглощения солнечной радиации в атмосфере , [14].
Влияние микроорганизмов на климат — далеко не новость для ученых. Мы рассказывали об этом в статье «О, этот благодатный дождь из бактерий!» [41].
Экологическое значение фагов пока изучено недостаточно, и имеющиеся сейчас данные в основном касаются морских экосистем. Ученым еще предстоит многое узнать о роли этих удивительных существ в жизни бактерий и всех остальных обитателей Земли.
Бактерии защищаются
Бактериальные клетки вовсе не беззащитны перед фагами. В ходе эволюции они сформировали многочисленные механизмы устойчивости и сопротивляются на каждом этапе развития инфекции.
Предотвращение адсорбции фагов
Чтобы запустить свой генетический материал внутрь клетки, для начала фаг должен прикрепиться к ней с помощью особых рецептор-связывающих белков, которые иногда также называют фаговыми адгезинами. В качестве рецепторов приходится использовать различные структуры на поверхности бактериальной клетки. Чтобы сопротивляться адсорбции, бактерии выработали по крайней мере три механизма: блокирование фаговых рецепторов, образование внеклеточного матрикса и продукция конкурентных ингибиторов.
Чтобы блокировать фаговые рецепторы, микроорганизмы могут изменить их химическую структуру или трехмерную конфигурацию. Например, интересный механизм наблюдается у золотистого стафилококка. Эти бактерии производят IgG-связывающий белок — фактор вирулентности А, заякоренный в клеточной стенке. Когда этого белка много, адсорбция фагов ухудшается. Это говорит о том, что белок А вместе со связанными им иммуноглобулинами маскирует фаговый рецептор.
Образование межклеточного матрикса — полимеров, в которые бактерии погружены, как в желе, — защищает микроорганизмы от негативных воздействий внешней среды, а также создает физический барьер между бактериофагами и их рецепторами. Пример с биопленками мы рассматривали выше. Но некоторые фаги научились распознавать полимеры межклеточного матрикса, и даже разрушать их.
Конкурентные ингибиторы — вещества, способные связываться с фаговыми рецепторами и конкурирующие за них с бактериофагами. Например, FhuA — соединение на поверхности кишечных палочек — одновременно отвечает за транспорт железа и служит рецептором для адсорбции фагов. Этот рецептор может быть заблокирован антимикробным пептидом микроцином J25. Бактерии начинают его производить в условиях нехватки ресурсов, чтобы подавить рост представителей родственных видов. Одновременно оно обеспечивает противофаговую защиту.
Предотвращение проникновения ДНК фага в клетку
Этот механизм обеспечивается системами исключения суперинфекции (Sie). Они включают набор белков, которые, собственно, предотвращают проникновение в бактерию фаговых ДНК. Эти белки встроены в клеточную мембрану или связаны с ней. Интересно, что белки системы Sie зачастую «неродные» для бактерий: они кодируются не их собственными генами, а профагами. И это дает повод предположить, что Sie изначально предназначены не столько для защиты микроорганизмов, сколько, чтобы помогать фагам не пускать внутрь «кормушки» конкурентов.
Так, у фага T4 есть две системы Sie, предотвращающие проникновение в клетку других T-чётных фагов после инфицирования: эти системы представлены белками imm и sp. Они действуют отдельно друг от друга и работают по-разному (рис. 5):
- imm изменяет конформацию (пространственную конфигурацию) белков в месте введения вирусной ДНК. Этот защитный белок связан с мембраной и, как полагают ученые, должен связаться с другим белком, чтобы эффективно выполнять свои функции.
- Sp — мембранный белок, подавляющий активность фермента, который находится на конце хвоста фага и проделывает отверстия в стенке клетки-хозяина [42].
Рисунок 5. Блокирование проникновения ДНК в бактериальную клетку. а — Обычное инфицирование E. coli фагом T4. Пептидогликановый слой разрушается, и белок внутренней мембраны участвует в проникновении ДНК в цитоплазму. б — Белок фага T4 imm блокирует проникновение ДНК в цитоплазму, тем самым предотвращая инфицирование другими T-четными фагами. в — Белок Sp, также кодируемый фагом Т4, предотвращает деградацию пептидогликана, останавливая фаговую ДНК между слоем пептидогликана и внешней мембраной.
Разрушение нуклеиновых кислот фага
Даже после того, как фаг сумел проникнуть внутрь бактериальной клетки, праздновать победу ему еще рано. Враждебная нуклеиновая кислота может быть разрушена еще до того, как успеет натворить бед. Для этого в клетках прокариот есть, на удивление, аналог иммунной системы животных и человека.
Например, бактерии многих, если не всех, родов обладают системами рестрикции-модификации. ДНК прокариот отличается от вирусной тем, что часто метилирована. Когда внутрь клетки попадает неметилированная ДНК фага, то она либо «разрезается» ферментами-рестриктазами (рестрикция), либо модифицируется — тоже метилируется (ферментами-метилазами — бактериальными или фаговыми), что запускает литический цикл (рис. 6). Судьба фагового генетического материала, а следовательно, и бактериальной клетки зависит от соотношения активности этих ферментов. Обычно «выигрывают» рестриктазы, в то время как метилирование обеспечивает защиту собственного генетического материала микроорганизма [42–44].
Рисунок 6. Схема работы системы рестрикции-модификации бактерий. Бактериальные рестриктазы «разрезают» ДНК фага, в то время как собственный генетический материал микроорганизма защищен метилированием.
Другая система защиты бактерий от чужеродного генетического материала носит название CRISPR/Cas. Это уже полноценный «иммунитет», способный специфически распознавать ДНК патогенов и «запоминать» новые фаги. В геноме бактерий есть особые участки — короткие палиндромные повторы, регулярно расположенные группами (Clustered Regularly Interspaced Short Palindromic Repeats, CRISPR) . Между этими повторами вставлены фрагменты ДНК фагов — как ориентировки в отделении полиции. Внутри клетки патрулируют «полицейские» — ферменты (Cas-белки), связанные с CRISPR-РНК. Если на их пути встречается фрагмент нуклеиновой кислоты, соответствующий CRISPR-РНК, Cas-белок его «разрезает» (рис. 7) [42], [45], [46].
Рисунок 7. Схема работы системы CRISPR/Cas. В хромосоме бактерии встроены участки, в которых содержатся фрагменты ДНК фагов. Они служат матрицами для синтеза CRISPR-РНК, которые затем связываются с ферментами Cas. Когда РНК распознает вирусную ДНК, фермент ее «разрезает».
На нашем сайте есть подробная статья о работе системы CRISPR/Cas — «Просто о сложном: CRISPR/Cas» [47]. Когда ученые узнали о замечательных свойствах этой системы, ее стали использовать в генной инженерии. На данный момент это один из самых быстрых и эффективных инструментов редактирования генома.
Системы абортивной инфекции
Эти системы предотвращают дальнейшее распространение фагов, уже заразивших клетку. Это единственный вид защиты, который предусматривает гибель инфицированной клетки, и он обеспечивается работой большого количества различных белков. Как правило, эти белки действуют на этапе репликации, транскрипции или трансляции фаговой ДНК. Используя подобные механизмы «самоубийства», бактериальное сообщество действует наподобие многоклеточных организмов, которые тоже обладают массой средств для уничтожения клеток, пораженных вирусами.
Арсенал противофаговых средств бактерий не изучен окончательно. Ученые постоянно открывают новые механизмы. Например, в 2018 году израильские исследователи обнаружили целых 10, ранее неизвестных. Мы рассказывали об этом в статье «Противофаговая линия Мажино в клетках прокариот: новые открытия» [48].
Кроме того, фаги и сами могут защищать своих жертв, и даже общаться между собой, посылая собратьям сообщение: «Эту клетку убивать не надо!». Об этом можно почитать в статье «Бактериофаг-1 Бактериофагу-2, приём!» [49].
На все ухищрения бактерий фагам есть что ответить, и они тоже постоянно совершенствуют свои механизмы преодоления бактериальной резистентности. Бактериофаги приобретают мутации, которые позволяют им прикрепляться к новым или изменившимся старым рецепторам, эффективнее получать к ним доступ, избегать разрушения ДНК, оказавшись внутри клетки. И ученые продолжают открывать новые механизмы. Об одном из таких открытий можно почитать в нашей статье «Белок Ocr — швейцарский нож бактериофага T7» [50].
То, что не убивает, — делает сильнее
Раньше ученые смотрели на бактериофаги исключительно как на хищников, безжалостно расправляющихся с бактериями. Современные взгляды сильно изменились. Хищник превратился в некое подобие программного кода. Он может оказаться не только вредителем, но и вполне полезным софтом.
Фаги могут способствовать адаптации бактерий четырьмя основными путями:
- Некоторые выступают в качестве «опорных точек» для перестройки генома.
- Умеренные фаги защищают бактериальные клетки от вирулентных.
- Вирулентные, в свою очередь, могут уничтожить конкурирующие микроорганизмы.
- Многие фаги могут вводить в геном бактерий новые полезные гены, которые повышают устойчивость к внешним факторам (в том числе антибиотикам), помогают эффективнее вызывать инфекции, вырабатывать токсины, адаптироваться к среде (некоторые подробности можно найти в нашей статье «Фаги-оруженосцы на службе у бактерий» [51]). Это происходит в рамках лизогенной конверсии и трансдукции [52].
При лизогенной конверсии умеренный фаг вставляет в ДНК бактерии гены, которые кодируют те или иные полезные (для самой бактерии) белки (рис. 8). Этот признак наследуется вместе с профагом, но только до тех пор, пока захватчик не решит прекратить мирное сосуществование и не запустит литический цикл. Обычно гены, ответственные за лизогенную конверсию, находятся в моронах и не имеют большого значения для самого фага [53], [54].
Рисунок 8. Схема лизогенной конверсии. Профаг может нести гены, которые кодируют белки, усиливающие адгезию к тканям хозяина, обладающие эффектами токсинов, разрушающие ткани хозяина, помогающие уклоняться от агрессии иммунной системы.
Самый яркий и известный пример лизогенной конверсии — выработка токсина дифтерийными палочками. На самом деле ген, кодирующий этот токсин, принадлежит не бактериям, а инфицирующему их умеренному β-фагу [55]. Некоторые другие полезные свойства, которыми фаги могут поделиться с бактериями, представлены в таблице.
| Название вещества | Фаг | Бактерия-хозяин |
|---|---|---|
| Экзотоксины — вещества, которые бактерии вырабатывают и выделяют во внешнюю среду | ||
| Дифтерийный токсин | β-фаг | C. diphtheriae (возбудитель дифтерии) |
| Нейротоксин (ботулотоксин) | С1 | C. botulinum (возбудитель ботулизма) |
| Шига-токсин | H-19B | E. coli (кишечные палочки, вызывающие диарею) |
| Энтеротоксины | φN315, φ13, φMu50A | S. aureus (золотистые стафилококки) |
| Холерный токсин (холероген) | CTXφ | V. cholerae (холерный вибрион — возбудитель холеры) |
| Белки, изменяющие антигенные свойства | ||
| Мембранные белки | Pnm1 | N. meningitidis (возбудитель менингита) |
| Гликозилирующие белки | ɛ34, P22 | S. enterica (возбудитель сальмонеллеза) |
| Глюкозилтрансфераза | SfII, SfV, SfX | S. flexneri (вызывает диарею) |
| Эффекторные белки, участвующие в инвазии (вторжении микроорганизмов в ткани) | ||
| Эффектор III типа | SopEΦ, GIFSY-2, GIFSY-3 | S. enterica |
| Ферменты | ||
| Супероксиддисмутаза | GIFSY-2, Fels-1 | S. enterica |
| Супероксиддисмутаза | Sp4, 10 | Кишечные палочки |
| Нейраминидаза | Fels-1 | S. enterica |
| Гиалуронидаза | H4489A | S. pyogenes |
| Лейкоцидин | φPVL | S. aureus |
| Стафилокиназа | φ13 | S. aureus |
| Фосфолипаза | 315.4 | S. pyogenes |
| ДНКаза/стрептодорназа | 315.6, 8232.5 | S. pyogenes |
| Сывороточная резистентность | ||
| OMPb, OMP | λ-фаг | E. coli |
| Белки адгезии для прикрепления бактерий к тканям хозяина | ||
| Vir | MAV1 | M. arthritidis |
| Белки оболочки фага | СМ1 | S. mitis |
| Другие соединения | ||
| Митогенный фактор | 370.1, 370.3, 315.3 | S. pyogenes |
| Митогенный фактор | Нет названия | P. multocida |
| Митогенный фактор | phisc 1 | S. canis |
| Вирулентность | GIFSY-2 | S. enterica |
| Антивирулентность | GIFSY-2, Fels-1 | S. enterica |
Иной механизм, с помощью которого фаги могут наделять бактерии полезными свойствами — трансдукция. В данном случае новый ген, позаимствованный у другого микроорганизма, не связан жестко с вирусной ДНК, а как бы приносится в дар бактерии и становится частью ее генома. Трансдукция бывает двух видов (рис. 9) [56], [57]:
- Общая — когда при сборке новых вирусных частиц в них случайно упаковываются кусочки бактериальной ДНК.
- Специфическая — когда профаг, индуцировавший литический цикл, неправильно вырезается из ДНК бактерии и захватывает ее фрагменты [3].
Рисунок 9а. Схематическое изображение общей (неспецифической) фаговой трансдукции. В вирусные частицы случайным образом упаковываются фрагменты ДНК клетки-хозяина.
Рисунок 9б. Схематическое изображение специфической фаговой трансдукции. Профаг захватывает соседние участки ДНК.
В частности, в ходе трансдукции микроорганизмы могут обмениваться генами, отвечающими за устойчивость к антибиотикам. Но значение этого явления выходит далеко за рамки индивидуальной пользы для отдельно взятой бактерии. Фаговая трансдукция помогает в целом обеспечивать разнообразие микробного мира, важна для его выживания.
Вирусный «микробиом» человека — виром
Организм человека населен микроорганизмами, составляющими его естественную микрофлору — об этом известно любому обывателю с тех пор, как реклама буквально из каждого утюга стала рассказывать о дисбактериозе и методах борьбы с ним. Но мало кому известно, что наше тело также является обиталищем огромного сообщества вирусов — вирома. Он включает примерно 1013 вирусных частиц (примерно как бактерий), и среди них есть:
- бактериофаги;
- вирусы, инфицирующие собственные клетки человека;
- фаги архей;
- вирусы эукариот, обитающих в составе микрофлоры;
- «временные пассажиры».
Считается, что большую часть от этого множества составляют хвостатые фаги.
По ряду причин изучать человеческий виром (еще иногда употребляют термин «фагом») сложнее, чем бактериальную микрофлору, но с появлением технологии секвенирования нового поколения дело пошло намного лучше [59], [60]. Один из наиболее известных современных проектов — «Микробиом человека». Когда ученые оценивают виром человека и животных, обычно они употребляют термин «вирусоподобные частицы». Это словосочетание означает, что генетический материал из тканей, биологических жидкостей и фекалий не всегда принадлежит жизнеспособным вирусам, способным заражать клетки [61–63].
Состав вирома различается в разных частях организма, а также зависит от возраста человека, питания, среды обитания, генетики, заболеваний, приема тех или иных лекарств и других факторов (рис. 10).
Рисунок 10. Вирусные сообщества в разных частях организма человека. Эта инфографика составлена на основе нескольких десятков научных обзоров. Будущие исследования наверняка приведут к тому, что списки этих виромов будут расширены.
Организм человека — не менее сложная «экосистема» для вирусов, чем, скажем, океан или почва. Тут на популяции микробов и вирусов влияют pH, иммунные механизмы, вещества, вырабатываемые в процессе жизнедеятельности человека (например, гидролипидная мантия на коже, желчь в кишечнике), доступность воды, питательных веществ и кислорода. В целом макроорганизм, бактерии и вирусы составляют сложную систему и постоянно взаимодействуют друг с другом [61], [63].
Пищеварительный тракт
Пищеварительный тракт — самая густонаселенная вирусами (в основном фагами) система человеческого организма, и ее виром изучен лучше всего. Тут обнаруживают в среднем 109 вирусоподобных частиц на каждый грамм кишечного содержимого. Наиболее распространены хвостатые фаги порядка Caudovirales.
Виром кишечника начинает формироваться с самого рождения. У детей на первом месяце жизни отмечается низкое разнообразие бактерий, но высокое — фагов. К двум годам картина меняется на противоположную: разновидностей бактерий становится много, а фагов — мало (вирусные сообщества в природе намного сложнее). Другое интересное свойство кишечной популяции фагов — ее большая вариабельность. Состав вирусоподобных частиц, которые получают от разных людей, зачастую сильно различается. Одно исследование показало, что ребенок «наследует» от матери 65% микрофлоры и только 15% вирома — остальная часть формируется в зависимости от условий окружающей среды и индивидуальных особенностей организма [61], [63], [64].
В норме в кишечнике преобладают умеренные фаги, а при многих заболеваниях увеличивается число вирулентных, чаще запускаются литические циклы. Триггерами могут стать не только патологические процессы, но и некоторые лекарства. Например, известно, что к индукции профагов приводят препараты из группы фторхинолонов — норфлоксацин и ципрофлоксацин. Лизис бактерий не проходит бесследно: он приводит к изменению состава микрофлоры. Вообще, при многих кишечных заболеваниях меняется структура не только микробиома, но и вирома [64].
| Заболевание | Исследованный материал | Изменения в вироме |
|---|---|---|
| Болезнь Крона и язвенный колит | кал* | Увеличение содержания Caudovirales |
| Ранняя стадия болезни Крона и язвенного колита | биоптант кишечника | Увеличение содержания Hepadnaviridae и Hepeviridae; уменьшение — Polydnaviridae, Tymoviridae и Virgaviridae |
| Колоректальный рак (злокачественные опухоли толстой и прямой кишки) | кал | Увеличение вирусного разнообразия |
| Сахарный диабет 1 типа | кал | Снижение вирусного разнообразия |
| Артериальная гипертония | кал | Обнаружены данные в пользу связи между увеличением числа фагов Erwinia ΦEaH2, Lactococcus 1706 и развитием артериальной гипертонии |
| Целиакия (непереносимость глютена) | кал | Увеличение содержания энтеровирусов |
| * — Важно понимать, что анализ кала не позволяет в полной мере оценить структуру микрофлоры и вирома пищеварительного тракта. В данном случае речь идет о микроорганизмах и вирусах, которые удается выделить в кале, — а в кишечнике они могут быть на самом деле представлены в меньшинстве. |
Кожа
Микрофлора кожи отличается относительно низкой численностью. К тому же кожа — орган, который постоянно контактирует с окружающей средой и подвергается всевозможным воздействиям. Из-за этого ее виром исследовать сложно, а генетический материал трудно отличить от случайных загрязнений. Тем не менее некоторые исследования были проведены. Во время одного из них 95% обнаруженных генетических последовательностей не удалось отнести ни к одному известному вирусу. Среди идентифицированного материала значительная часть принадлежала хвостатым фагам [61], [65].
Недавно провели исследование, авторы которого нашли новое неожиданное применение вирому кожи. Оказалось, что популяция вирусов у каждого человека настолько индивидуальна, что ее потенциально можно использовать для идентификации личности, если собственная ДНК по каким-то причинам недоступна для исследования. Возможно, в будущем удастся поставить вирусы на службу криминалистике , [66].
О криминалистических биотехнологиях во всех подробностях читайте в нашем спецпроекте «Криминалистика».
Ротовая полость
Как и в любой части организма, разнообразие бактериофагов в ротовой полости определяется разнообразием прокариот, а оно, в свою очередь, зависит от особенностей питания, вредных привычек, гигиены. Ротовая полость сама по себе неоднородна, и в ней есть разные «экологические ниши» (см. спецпроект «Биомолекулы» «Биология, медицина и косметология ротовой полости»). Если говорить о вироме, то тут, как и везде, преобладают хвостатые бактериофаги. В слюне содержится примерно 108 вирусоподобных частиц на мл, в зубном налете — 107 на мг.
Исследования показывают, что только небольшая часть вирусов в ротовой полости одинакова для разных людей. При этом у одного и того же человека со временем вирусное сообщество остается более-менее стабильным. Несомненно, фаги влияют на формирование микрофлоры рта, и их состав меняется при разных заболеваниях. В здоровой ротовой полости много умеренных бактериофагов, а при воспалительных процессах происходит сдвиг в сторону вирулентных. Изучение вирома ротовой полости играет важную роль в понимании развития различных патологий и может открыть новые подходы к лечению [61], [67], [68].
Дыхательные пути
Виром дыхательных путей, особенно нижних, исследован недостаточно хорошо. Этому вопросу посвящено мало научных работ, и в основном их проводили у детей с острыми респираторными заболеваниями. Раньше считалось, что микрофлора есть только в верхних дыхательных путях, а легкие стерильны. Более современные исследования показывают, что это не так. В легких здоровых некурящих людей есть небольшие бактериальные сообщества. Присутствуют в дыхательной системе и вирусы. Некоторые из них способны вызывать заболевания, некоторые безвредны. Есть тут и хвостатые фаги. Они попадают в легкие в основном из ротовой полости и верхних дыхательных путей [61], [69], [70].
Кровь
Даже святая святых организма человека — кровь, наша внутренняя среда, совсем не стерильна. В ней можно обнаружить как вирусы, так и фаги. В кровеносные и лимфатические сосуды бактериофаги проникают благодаря своей способности преодолевать слизистые оболочки из легких, печени, почек, головного мозга и главного резервуара — кишечника [61].
У фагов есть несколько возможностей проникнуть в кровоток. Самый простой способ — через повреждения на слизистой оболочке. Бактериофаги могут путешествовать внутри бактериальных клеток — в таком случае прокариоты играют роль «троянского коня». Но прячутся в таком «коне» вовсе не враги. Последствия проникновения фагов в кровь до конца не понятны, но считается, что они приносят пользу: помогают расправляться с опасными патогенами и стимулируют работу иммунной системы. Могут фаги путешествовать и путем эндоцитоза: когда клетка «прогибает» внутрь свою мембрану, и из нее получается пузырек с вирусной частицей внутри.
В 2017 году американские и австралийские ученые опубликовали результаты исследования, которое показало, что фаги путешествуют через плотно контактирующие клетки слизистых оболочек с помощью трансцитоза, и этот путь, видимо, имеет большое значение. Получается быстро и направленно: фаг перемещается по клетке в апикально-базальном направлении, то есть от верхушки к условно нижней части, прикрепленной к базальной мембране. При этом трансцитоз осуществляется через аппарат Гольджи. Исследователи наблюдали этот процесс на примере фага T4 в искусственно выращенных in vitro («в пробирке») клетках кишечника, легких, печени, почек и эндотелия головного мозга (рис. 11) [71].
Рисунок 11. Трансцитоз бактериофага T4 через клеточные слои в лабораторных условиях. а — Клетки, над которыми находится апикальная камера, а внизу — базальная камера («снизу» — там, где клетка прикрепляется к базальной мембране). Фаги T4 вносили в каждую из этих камер, чтобы проследить направление транспорта. б — Трансцитоз бактериофагов в базально-апикальном и апикально-базальном направлении. в — Трансцитоз фагов через клетки T84 (эпителий толстой кишки), CaCo2 (эпителий толстой кишки), A549 (эпителий легких), Huh7 (клетки печень — гепатоциты) и hBNec (эндотелиальные клетки головного мозга). Черные кружки отражают число фагов, загруженных в одну из камер, белые кружки — число фагов, обнаруженных в противоположной камере, которым удалось пройти через клетку. Видно, что транспорт носит апикально-базальный характер.
По подсчетам авторов этого исследования, ежедневно через слизистую оболочку кишечника в кровоток человека должно проникать около 31 миллиарда фаговых частиц.
Современные исследования показывают, что фаги есть не только в крови, но и в других средах организма, которые классически считались стерильными. Это заставило ученых выдвинуть новую концепцию «внутреннего фагома», и она находит всё больше сторонников. Взаимодействия в треугольнике «фаги — бактерии — клетки человека» сложны и не до конца изучены. Причем, бактериофаги не всегда враги бактериям и друзья нам. Например, они могут становиться резервуаром генов устойчивости микроорганизмов к антибиотикам.
Кроме того, фаги — резервуар генетической «темной материи». Есть мнение, что эти неисследованные гены могут экспрессироваться не только в бактериальных, но и в эукариотических клетках. Для этого потенциального механизма есть множество ограничений: сильные различия между сайтами транскрипции млекопитающих и вирусов, системы рестрикции и фосфорилирования, особенности кодонов, распределение транспортной РНК. Но даже с учетом этих ограничений нельзя исключить определенного прямого влияния фаговой ДНК на клетки человека, обмен веществ, иммунитет, состояние здоровья и развитие заболеваний. Это интересная область для будущих исследований [72].
Мочеполовая система
В моче человека содержится 107 вирусоподобных частиц на миллилитр. В большинстве случаев это фаги, но есть и вирусы эукариот — исследования показывают, что более чем у 90% испытуемых обнаруживаются вирусы папилломы человека. В мазках из влагалища у здоровых женщин обнаруживается в основном фаговая ДНК, и только 4% приходится на генетический материал вирусов эукариот. Семенная жидкость у мужчин тоже не стерильна [61].
Нервная система
Нервная система надежно защищена от микроорганизмов — она отгородилась от сосудистого русла баррикадой в лице гематоэнцефалического барьера [73]. Он пропускает даже не все лекарственные препараты. Тем не менее в спинномозговой жидкости фаги тоже есть — 104 вирусоподобных частиц на миллилитр. Что они тут делают — еще предстоит изучить [61].
***
Подводя итог, можно только повторить то, о чем мы упоминали в начале этого обзора: фаги — очень значимый фактор, оказывающий влияние на всё живое на нашей планете. И ученые смогли обратить этот фактор в ценный ресурс, возможности которого до сих пор далеко не исчерпаны. Фаги нашли применение в науке, пищевой промышленности, медицине, ветеринарии. Об этом пойдет речь в следующих статьях нашего спецпроекта.
- 12 методов в картинках: микроскопия;
- А.В. Летаров. (2020). История ранних исследований бактериофагов и рождение основных концепций вирусологии. БМ. 85, 1189-1212;
- Летаров А.В. Современные концепции биологии бактериофагов. М.: ТД «ДеЛи», 2019;
- Ивановский Д. И. (1892) Мозаичная болезнь табака, Труды Варшавского университета, 6, 49-72;
- Его Величество паразит;
- Манипулирование. I. Паразитное манипулирование;
- Паразит паразиту враг;
- Martha R.J. Clokie, Andrew D. Millard, Andrey V. Letarov, Shaun Heaphy. (2011). Phages in nature. Bacteriophage. 1, 31-45;
- Markus G. Weinbauer. (2004). Ecology of prokaryotic viruses. FEMS Microbiol Rev. 28, 127-181;
- Hans-W. Ackermann, Hans-W. Ackermann. (2011). The first phage electron micrographs. Bacteriophage. 1, 225-227;
- Пожиратели бактерий: убийцы в роли спасителей;
- Модельные организмы: фаг лямбда;
- Edel Stone, Katrina Campbell, Irene Grant, Olivia McAuliffe. (2019). Understanding and Exploiting Phage–Host Interactions. Viruses. 11, 567;
- Катер Э. и Сулаквелидзе А. Бактериофаги. Биология и практическое применение. М.: «Научный мир», 2012;
- Wessner D.R. (2010). The origins of viruses. Nature Education. 3(9): 37;
- Karin Moelling, Felix Broecker. (2021). Viroids and the Origin of Life. IJMS. 22, 3476;
- РНК у истоков жизни?;
- РНК: начало (мир РНК);
- Reyad A. Elbarbary, Bronwyn A. Lucas, Lynne E. Maquat. (2016). Retrotransposons as regulators of gene expression. Science. 351;
- Мобильные генетические элементы прокариот: стратификация «общества» бродяжек и домоседов;
- Маленький, да удаленький: самые маленькие клетки;
- James A. Kraemer, Marcella L. Erb, Christopher A. Waddling, Elizabeth A. Montabana, Elena A. Zehr, et. al.. (2012). A Phage Tubulin Assembles Dynamic Filaments by an Atypical Mechanism to Center Viral DNA within the Host Cell. Cell. 149, 1488-1499;
- Yana A. Danilova, Viktoriia V. Belousova, Andrey V. Moiseenko, Innokentii E. Vishnyakov, Maria V. Yakunina, Olga S. Sokolova. (2020). Maturation of Pseudo-Nucleus Compartment in P. aeruginosa, Infected with Giant phiKZ Phage. Viruses. 12, 1197;
- «Я в домике!»: бактериофаги, у которых есть ядра;
- Гиганты вирусного мира;
- Allan Campbell. (2003). The future of bacteriophage biology. Nat Rev Genet. 4, 471-477;
- Вирусные геномы в системе эволюции;
- Graham F Hatfull, Roger W Hendrix. (2011). Bacteriophages and their genomes. Current Opinion in Virology. 1, 298-303;
- Graham F Hatfull. (2008). Bacteriophage genomics. Current Opinion in Microbiology. 11, 447-453;
- David Botstein. (1980). A THEORY OF MODULAR EVOLUTION FOR BACTERIOPHAGES. Ann NY Acad Sci. 354, 484-491;
- Bethany N. Kent, Lisa J. Funkhouser, Shefali Setia, Seth R. Bordenstein. (2011). Evolutionary Genomics of a Temperate Bacteriophage in an Obligate Intracellular Bacteria (Wolbachia). PLoS ONE. 6, e24984;
- Adrián Cazares, Guillermo Mendoza-Hernández, Gabriel Guarneros. (2014). Core and accessory genome architecture in a group of Pseudomonas aeruginosa Mu-like phages. BMC Genomics. 15;
- Bacteria-infecting viruses. The lytic and lysogenic cycles. Khan Academy;
- Tomasz Olszak, Agnieszka Latka, Bartosz Roszniowski, Miguel A. Valvano, Zuzanna Drulis-Kawa. (2017). Phage Life Cycles Behind Bacterial Biodiversity. CMC. 24;
- 10.23750/abm.v91i13-S.10819;
- Rasmus Skytte Eriksen, Namiko Mitarai, Kim Sneppen. (2020). Sustainability of spatially distributed bacteria-phage systems. Sci Rep. 10;
- Korytowski D.A. and Smith H.L. (2016). Permanence and Stability of a Kill the Winner Model in Marine Ecology. Cornell University;
- Schwink S. (2018). Virus-bacteria coevolution solves diversity paradox by ‘Killing the Winner’. Illinois IGB;
- Sergei Maslov, Kim Sneppen. (2017). Population cycles and species diversity in dynamic Kill-the-Winner model of microbial ecosystems. Sci Rep. 7;
- Nana Yaw D Ankrah, Amanda L May, Jesse L Middleton, Daniel R Jones, Mary K Hadden, et. al.. (2014). Phage infection of an environmentally relevant marine bacterium alters host metabolism and lysate composition. ISME J. 8, 1089-1100;
- О, этот благодатный дождь из бактерий!;
- Simon J. Labrie, Julie E. Samson, Sylvain Moineau. (2010). Bacteriophage resistance mechanisms. Nat Rev Microbiol. 8, 317-327;
- Andjela Rodic, Bojana Blagojevic, Evgeny Zdobnov, Magdalena Djordjevic, Marko Djordjevic. (2017). Understanding key features of bacterial restriction-modification systems through quantitative modeling. BMC Syst Biol. 11, 1-15;
- Furuta Y. and Kobayashi I. Restriction-modification systems as mobile epigenetic elements. Austin (TX): Landes Bioscience, 2000-2013;
- Северинов К. (2016). Редактирование генома с CRISPR/Cas9. «Постнаука»;
- Frank Hille, Emmanuelle Charpentier. (2016). CRISPR-Cas: biology, mechanisms and relevance. Phil. Trans. R. Soc. B. 371, 20150496;
- Просто о сложном: CRISPR/Cas;
- Противофаговая линия Мажино в клетках прокариот: новые открытия;
- «Бактериофаг-1 Бактериофагу-2, приём!»;
- Белок Ocr — швейцарский нож бактериофага T7;
- Фаги-оруженосцы на службе у бактерий;
- Harald Brüssow, Carlos Canchaya, Wolf-Dietrich Hardt. (2004). Phages and the Evolution of Bacterial Pathogens: from Genomic Rearrangements to Lysogenic Conversion. Microbiol Mol Biol Rev. 68, 560-602;
- John W. Little. (2014). Lysogeny, Prophage Induction, and Lysogenic Conversion. Phages. 37-54;
- Malignant transformation. Britannica;
- Дифтерия: больная бактерия, способная убивать;
- Christine L. Schneider. (2017). Bacteriophage-Mediated Horizontal Gene Transfer: Transduction. Bacteriophages. 1-42;
- Yin Ning Chiang, José R. Penadés, John Chen. (2019). Genetic transduction by phages and chromosomal islands: The new and noncanonical. PLoS Pathog. 15, e1007878;
- Dana K Howe, Dee R Denver. (2008). Muller’s Ratchet and compensatory mutation in Caenorhabditis briggsae mitochondrial genome evolution. BMC Evol Biol. 8, 62;
- Sam Behjati, Patrick S Tarpey. (2013). What is next generation sequencing?. Arch Dis Child Educ Pract Ed. 98, 236-238;
- 12 методов в картинках: секвенирование нуклеиновых кислот;
- Guanxiang Liang, Frederic D. Bushman. (2021). The human virome: assembly, composition and host interactions. Nat Rev Microbiol. 19, 514-527;
- Ryuichi Kumata, Jumpei Ito, Kenta Takahashi, Tadaki Suzuki, Kei Sato. (2020). A tissue level atlas of the healthy human virome. BMC Biol. 18;
- Emma Guerin, Colin Hill. (2020). Shining Light on Human Gut Bacteriophages. Front. Cell. Infect. Microbiol.. 10;
- Marzanna Łusiak-Szelachowska, Beata Weber-Dąbrowska, Ewa Jończyk-Matysiak, Renata Wojciechowska, Andrzej Górski. (2017). Bacteriophages in the gastrointestinal tract and their implications. Gut Pathog. 9;
- Geoffrey D. Hannigan, Jacquelyn S. Meisel, Amanda S. Tyldsley, Qi Zheng, Brendan P. Hodkinson, et. al.. (2015). The Human Skin Double-Stranded DNA Virome: Topographical and Temporal Diversity, Genetic Enrichment, and Dynamic Associations with the Host Microbiome. mBio. 6;
- Ema H. Graham, Jennifer L. Clarke, Samodha C. Fernando, Joshua R. Herr, Michael S. Adamowicz. (2022). The application of the skin virome for human identification. Forensic Science International: Genetics. 57, 102662;
- April Martínez, Ryutaro Kuraji, Yvonne L. Kapila. (2021). The human oral virome: Shedding light on the dark matter. Periodontol 2000. 87, 282-298;
- Vicente Pérez-Brocal, Andrés Moya. (2018). The analysis of the oral DNA virome reveals which viruses are widespread and rare among healthy young adults in Valencia (Spain). PLoS ONE. 13, e0191867;
- Kristine M. Wylie. (2017). The Virome of the Human Respiratory Tract. Clinics in Chest Medicine. 38, 11-19;
- Raquel Nazareth, Maria-Jesus Chasqueira, Maria-Lúcia Rodrigues, Carolina Paulino, Catarina Conceição, et. al.. (2020). Respiratory viruses in mechanically ventilated patients: a pilot study. BMC Pulm Med. 20;
- Sophie Nguyen, Kristi Baker, Benjamin S. Padman, Ruzeen Patwa, Rhys A. Dunstan, et. al.. (2017). Bacteriophage Transcytosis Provides a Mechanism To Cross Epithelial Cell Layers. mBio. 8;
- Jeremy J. Barr. (2017). A bacteriophages journey through the human body. Immunol Rev. 279, 106-122;
- Blood-brain barrier. Связующее между двумя мирами — кровеносной и центральной нервной системами;
- N. Vander Elst, E. Meyer. (2018). Potential therapeutic application of bacteriophages and phage-derived endolysins as alternative treatment of bovine mastitis. VDT. 87, 181-187.
- История открытия вирусов
- Виды вирусных заболеваний
- Респираторные инфекции
- Желудочно-кишечные инфекции
- Экзантематозные инфекции
- Инфекции печени
- Неврологические инфекции
- Геморрагическая лихорадка
- Инфекции кожи или слизистых оболочек
- Вирусолог Дмитрий Ивановский
- Вирусолог Мартин Бейеринк
- Изучение вирусов, исследования
- Институт вирусологии имени Гамалеи
История открытия вирусов
Первую информацию о вирусах люди начали собирать тысячелетия назад. В древних медицинских трактатах и летописях встречаются описания симптомов заразных болезней (например, оспы), а в ботанических трудах зафиксированы «следы», которые вирусные инфекции оставляли на растениях. Например, именно пестролистность – вирусное заболевание – давала эффектную и непредсказуемую окраску тюльпанам, которая ценилась среди европейских цветоводов 30-х годах XVI века. Среди ученых это явление первым описал Карл Клузиус – профессор ботаники, основоположник голландской индустрии луковичных растений. В те годы не удалось выяснить, почему у одних тюльпанов одноцветные лепестки, а у других они словно причудливо раскрашены. Цветоводы только установили, что с большей вероятностью можно получить необычный цветок, если высадить луковицу рядом с пестрым тюльпаном. Много лет спустя стало ясно, что этот вирус переносят вместе с зараженным соком от больных растений здоровым тли, клещи, трипсы и другие насекомые-вредители.
Вирусология как наука начала развиваться в XIX веке, когда люди узнали – благодаря микробиологам Луи Пастеру и Роберту Коху, хирургу Джозефу Листеру, – что инфекционные заболевания вызываются микробами. О том, что не все из этих микробов – бактерии, стало известно не сразу. Можно было только предполагать, что, например, возбудитель бешенства – некий болезнетворный агент, который по какой-то причине проскакивает через бактериальный фильтр, не выращивается на питательной среде и не виден через световой микроскоп. А первый вирус, который человеку удалось выделить, все-таки был растительным: им стал вирус табачной мозаики. И обнаружил его российский ученый Дмитрий Ивановский.
Виды вирусных заболеваний
Сегодня, разрабатывая способы борьбы с вирусными болезнями, ученые руководствуются в том числе и типами этих заболеваний. Классификацию вирусов в соответствии с системой пораженных органов полезно знать и обычному человеку, чтобы своевременно помочь себе и своим близким. Вот краткий обзор заболеваний1, вызываемых разными вирусами.
Респираторные инфекции – это инфекции верхних дыхательных путей, с которыми мы сталкиваемся чаще всего. От человека к человеку они, как правило, передаются воздушно-капельным путем. К этой группе относятся вирусы гриппа, риновирусы, а также коронавирусы, один из которых стал причиной пандемии в 2020 году и сейчас продолжает распространяться по планете.
Желудочно-кишечные инфекции распространяются фекально-оральным путем, так что основная мера профилактики – личная гигиена. К таким вирусам относится ротавирус, норовирус, астровирус и т. д.
Экзантематозные инфекции. Экзантема – это сыпь на коже, которой себя проявляют корь, краснуха, скарлатина, брюшной и сыпной тифы, ветряная оспа, герпес и т. д. Некоторые вирусы, помимо поражения кожи, вызывают и системные проявления.
Инфекции печени. К ним относятся не только вирусные гепатиты (А, B, C, D, E), но и другие вирусы: цитомегаловирус, вирус желтой лихорадки, а даже вирусы герпеса, кори, краснухи и ветрянки.
Неврологические инфекции часто распространяются комарами или клещами: это, например, энцефалит.
Геморрагическая лихорадка, которая вызывает поражение сосудов, также распространяется москитами и клещами, а также зараженными животными – грызунами, летучими мышами, обезьянами.
Инфекции кожи или слизистых оболочек. К вирусам, которые вызывают такие заболевания, относится вирус папилломы человека.
Вирусолог Дмитрий Ивановский
С табачной мозаикой2 знакомы, наверное, все, кто выращивал овощи и фрукты или просто наблюдал, как они растут. Несмотря на название, Tobacco mosaic virus поражает не один лишь табак, а более 350 видов овощных, садовых, декоративных растений. Желтые пятна и разводы на листьях огурцов, помидоров, картофеля, молодых яблонь – все это табачная мозаика. Она создавала проблемы фермерам и в прошлые века, особенно для тех, кто выращивал табак на продажу. Пораженные листья были непригодны для дальнейшей обработки, так что снижение урожая из-за мозаики било по карманам и фермеров, и производителей табачной продукции. Инфекционную природу этой болезни доказал в 1886 году немецкий агрохимик Адольф Майер, однако он посчитал, что всему виной бактерия. Его опыты решил повторить петербургский студент Дмитрий Ивановский. В университете он учился на физико-математическом факультете, однако по окончании остался при кафедре ботаники, выбрав темой диссертации мозаичную болезнь табака – этой темой Ивановский заинтересовался еще студентом, бывая на Украине и в Молдавии.
Молодой исследователь тоже думал, что мозаику вызывают бактерии, а значит, их можно собрать на керамическом фильтре, профильтровав экстракт зараженных листьев, а затем вырастить в питательной среде и заразить здоровое растение. Ничего из этого не удалось, и ученый предположил, что неуловимый патоген – либо бактерия намного мельче всех известных, либо токсин, который она выделяет. Статью о своем исследовании, длившемся пять лет, он опубликовал в журнале «Сельское хозяйство и лесоводство» в 1892 году, затем в Бюллетене Санкт-Петербургской Императорской Академии Наук и в международных журналах. Новаторство Ивановского заключалось еще и в том, что ему удалось увидеть в световой микроскоп, описать и зарисовать скопления вирусов в клетках табачного листа. Они имели вид кристаллических структур (Tobacco mosaic virus – палочковидный), и в научном мире их стали называть «кристаллами Ивановского». В 1935 году их очистил, впервые выделил и исследовал американский вирусолог Уэнделл Стэнли (который спустя еще 20 лет выделил вирус полиомиелита).
Дмитрий Иосифович Ивановский в 1895 году успешно защитил магистерскую диссертацию, начал читать лекции в родном вузе, после стал профессором Варшавского университета, где создал свою лабораторию. Ученый внес большой вклад в исследование физиологии и анатомии растений, занимался почвенной микробиологией, был автором 180 научных публикаций.
Вирусолог Мартин Бейеринк
Хотя открытие Ивановского касалось в первую очередь фитопатологии, оно сыграло огромную роль в развитии биологии, медицины и ветеринарии. Еще при жизни вирусолога его данные о вирусах дополнил нидерландский микробиолог Мартин Бейеринк (Martin Beijerinck). В 1898 году он, еще не зная об исследованиях Ивановского, тоже экспериментировал с вирусом табачной мозаики и сделал похожие выводы – кроме одного: он предположил, что инфекционный агент – это патогенная молекула, способная репродуцироваться и распространяться в клетках зараженного хозяина. Таким образом, Бейеринк угадал неклеточную природу вирусов. Узнав впоследствии о работе Ивановского, который его опередил, голландский ученый не стал замалчивать его достижение и честно сослался на работу предшественника.
Изучение вирусов, исследования
Вирус табачной мозаики стал первым организмом из своего царства, который исследовали на электронном микроскопе (в 1939 году). До сих пор это один из популярных модельных организмов. Прежде всего ученым нужно было научиться воспроизводить вирусы. В 1939 году американский врач Эрнест Гудпасчер сумел вырастить в куриных яйцах вирус гриппа. Еще через десять лет вирусологи из США – Эндерс, Уэллер и Роббинс – впервые вырастили полиовирус не на тканях животных или яйцах, а на культуре клеток человеческого зародыша. Благодаря этому достижению была создана первая эффективная вакцина против полиомиелита.
Уже упомянутый Уэнделл Стэнли, изучая вирус табачной мозаики, воздействовал на сок больных листьев табака реагентами и получил белок, который после ночи в холодильнике превратился в кристаллы – это и был вирус. В 1946 году Стэнли получил Нобелевскую премию по химии «За приготовление ферментов и вирусных белков в чистом виде». В конце 1930-х годов исследователи получили первую рентгенограмму вируса, а в 1955 году ученый-рентгенограф Розалинд Франклин определила его структуру. Во второй половине ХХ века вирусология начала стремительно развиваться. Было открыто свыше 2 тыс. видов разнообразных вирусов, а также ключевые ферменты, позволяющие им проникать в клетки живых организмов и размножаться там. Стало ясно, что вирусы можно классифицировать по нескольким признакам – по типу хранения генома, по форме оболочки и ее особенностям.
Уже в наше время, в 2002 году был создан первый синтетический вирус. На данный момент описано несколько тысяч видов вирусов, однако ученые предполагают, что в реальности их миллионы. Это самые распространенные биологические объекты на Земле! Кстати, большая их часть не болезнетворна или даже приносит пользу человеку. Последнее относится к фагам – вирусам, паразитирующим на бактериях. Впервые их обнаружили в конце XIX века. Способность фагов уничтожать вредоносные бактерии активно изучалась в СССР, где разработали фаги против стрептококка, сальмонеллеза и т.д. Сегодня интерес к фагам возрождается: их можно использовать против бактерий, которые развили устойчивость к антибиотикам.
Институт вирусологии имени Гамалеи
Одно из крупнейших в мире научных учреждений, исследующих вирусы, – Национальный исследовательский центр эпидемиологии и микробиологии имени Н. Ф. Гамалеи (ФГБУ «НИЦЭМ им. Н. Ф. Гамалеи3» Минздрава России. Он основан в 1891 году как Частный химико-микроскопический и бактериологический кабинет врача Филиппа Марковича Блюменталя, а вскоре был преобразован в Частный химико-бактериологический институт. В 1904 году здесь началось изготовление бактериальных препаратов: противодифтерийной и противодизентерийной сывороток и т.д. В 1949 году институту присвоили имя почетного академика Николая Федоровича Гамалеи – выдающегося российского микробиолога и эпидемиолога, основателя отечественной микробиологии, одного из основоположников дезинфекционного дела. Он работал в лаборатории Пастера, в 1886 году открыл первую в России и вторую в мире бактериологическую станцию, боролся с эпидемиями чумы и оспы в российских регионах.
Сегодня основное направление деятельности Центра Гамалеи – решение фундаментальных проблем в области эпидемиологии, инфекционной иммунологии. Здесь изучают закономерности распространения и проявления инфекционных заболеваний; генетику, молекулярную биологию и экологию патогенных микроорганизмов; разрабатывают способы диагностики и профилактики инфекционных болезней. На базе института работают девять центров Минздрава России: по риккетсиозам, лептоспирозам, бруцеллезу, туляремии, легионеллезу, микоплазмозам, хламидиозам, клостридиозам, боррелиозам.
В 1990-е годы на базе НИИ эпидемиологии и микробиологии им. Гамалеи был разработан и внедрен в клиническую практику группой ведущих российских ученых под руководством д. б. н., профессора В.В. Малиновской противовирусный и иммуномодулирующий препарат ВИФЕРОН. В 2021 году препарат стал лауреатом4 премии Smartpharma Awards 2021 в номинации «Противовирусный препарат №1 для лечения и профилактики гриппа и ОРВИ у детей с первых дней жизни и беременных женщин».
В 2020 году именно в НИЦЭМ им. Н. Ф. Гамалеи была разработана первая в мире зарегистрированная вакцина для профилактики коронавирусной инфекции COVID-19 «Спутник V», а в 2021 году – однокомпонентная вакцина против COVID-19 «Спутник Лайт».
Справочно-информационный материал
Автор статьи
Шамшева Дарья Сергеевна
Врач-терапевт, кардиолог, к.м.н.
1 https://www.msdmanuals.com/
2 https://bigenc.ru/
3 https://www.gamaleya.org/
4 https://awards.smartpharma.ru/